微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 短周期主族元素A、B、C、D、E、的原子序数依次增大,A和B形成5个原子核的分子,A和C形成3个原子核的分子,且两种分子均含有10个电子。D的原子半径最大,A、B、D、E与C形成的化合物均有两种,其中E与C形成的化合物中的一种能使品红溶液褪色。
则由A、B、C三种元素组成的中学常见的化合物中:
①甲燃烧则其耗氧量与乙烯相同则甲的结构简式是?。
②若乙能发生银镜反应则乙的化学式或结构简式是?。
③若丙分子中的B、A、C最简个数比为1:2: 1且丙能与D发生反应,则丙的结构简式?
④若丁标况下蒸汽密度为3.93g/L,B%=54.5%,A%=9.1%,且丁能发生水解反应则丁的结构简式为?。
⑤若戊在同条件下密度为H2的22倍,4.4g该物质完全燃烧产物依次通过浓硫酸增重3.6g,碱石灰增重8.8g则戊的结构简式为?。
参考答案:①CH3CH2OH ②CH2OH(CHOH)4CHO、CH3CHO?③CH3COOH?
④CH3COOHCH2CH3、CH3CH2COOCH3、HCOOCH2CH2CH3、HCOOCH(CH3)?⑤CH3CHO
本题解析:常见5核10电子分子是甲烷,3核10电子的分子是水分子,所以A是H,B是C,C是O。短周期中原子半径增大的是钠,则D是Na。E与O形成的化合物中的一种能使品红溶液褪色,该化合物应该是SO2,所以E是硫元素。
①乙烯的分子式为C2H4,所以燃烧时耗氧量与乙烯相同的应该是乙醇,因为乙醇的分子式看作是C2H4・H2O,,乙醇的结构简式为CH3CH2OH。
②能发生银镜反应,说明含有醛基,因此乙可以是葡萄糖或乙醛,结构简式分别为
CH2OH(CHOH)4CHO、CH3CHO。
③丙分子中的B、A、C最简个数比为1:2: 1,则最简式是CH2O。又因为丙能与钠发生反应,所以丙是乙酸,结构简式为CH3COOH。
④标况下蒸汽密度为3.93g/L,所以相对分子质量是3.93×22.4=88。所以碳和氢的原子个数分别是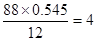 、
、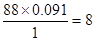 。因此氧原子的个数是
。因此氧原子的个数是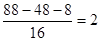 ,所以分子式为C4H8O2。又因为丁能发生水解反,所以丁可以是乙酸乙酯、丙酸甲酯或甲酸丙酯等。
,所以分子式为C4H8O2。又因为丁能发生水解反,所以丁可以是乙酸乙酯、丙酸甲酯或甲酸丙酯等。
⑤戊在同条件下密度为H2的22倍,所以相对分子质量是22×2=44,所以4.4g戊是0.1mol。燃烧产物依次通过浓硫酸增重3.6g,碱石灰增重8.8g,则水是3.6g,物质的量是0.2mol。CO2是8.8g,物质的量是0.2mol。所以分子中碳、氢原子的个数分别是4和2,因此氧原子的个数是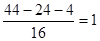 ,所以分子式为C2H4O,因此是乙醛
,所以分子式为C2H4O,因此是乙醛
本题难度:一般
2、填空题 (8分)由以下一些微粒:136C、3919K、4020Ca、126C、147N、4018Ar。其中:
小题1:互为同位素的是________和________;
小题2:质量数相等,但不能互称同位素的是_________和__________;
小题3:中子数相等,但质子数不相等的是_________和_________; _________和_________。
参考答案:
小题1:136C?126C;
小题2: 4020Ca?4018Ar;
小题3: 3919K?4020Ca ;136C?147N
本题解析:考查同位素的概念和原子的组成以及表示方法等。同位素是指质子数相同而中子数不同的同一种元素的不同核素。在表示原子组成时,在元素符号的左下角表示质子数,左上角表示的质量数。质子数和中子数的之和是质量数,所以6种微粒的中子数分别为7、20、20、6、7、22。
本题难度:简单
3、填空题 (21分)下表是元素周期表的一部分,回答有关问题。
?
| ?ⅠА
| ?ⅡА
| ?ⅢА
| ?ⅣА
| ?ⅤА
| ⅥА
| ?ⅦА
| ? 0
|
? 2
| ?
| ?
| ?
| ?
| ?①
| ?
| ?②
| ?
|
? 3
| ?③
| ?④
| ?⑤
| ?⑥
| ?
| ?⑦
| ?⑧
| ?⑨
|
? 4
| ?⑩
| ? 11
| ?
| ?
| ?
| ?
| ? 12
| ?
|
(1)在这些元素中,最活泼的金属元素是(均用元素名称填写)?―、最活泼的非金属元素是?、最不活泼的元素是?
(2)在这些元素的最高价氧化物对应的水化物中,酸性最强的是(均用化学式填写)?、碱性最强的是?,呈两性的氢氧化物是?,写出三者之间两两相互反应的离子方程式?
(3)在这些元素中,原子半径最大的是?―、原子半径最小的是?(均用元素符号填写)
(4)写出②与④形成化合物的电子式?;写出①单质的电子式?;
参考答案:(1)钾?氟?氩(每空1分)
(2)HClO4? KOH? Al(OH)3 ?
H+ + OH -= H2O? 3H+ + Al(OH)3 ?=? Al3+ + H2O?
OHˉ+ Al(OH)3 ?=? [Al(OH )4]ˉ(每空2分)
(3)? K? F (每空1分)
(4)氟化镁的电子式;氮气的电子式(每空2分)
本题解析:(1)题可以根据元素周期律,同周期从左到右元素金属性逐渐减弱,非金属性逐渐增强,同主族元素从上到下元素金属性逐渐增强,非金属性逐渐减弱,得出相应答案。
(2)题可以由最高价氧化物对应水化物的酸性和碱性强弱的判断依据,即非金属性越强酸性越强,金属性越强碱性越强。
(3)依据电子层数越多半径越大,电子层数相同时,原子序数越大半径越小得出答案。
(4)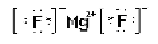 ?
?
本题难度:一般
4、选择题 下列提纯方法正确的是
A.提取碘水中的碘单质:萃取
B.提纯氢氧化铁胶体:过滤
C.除去氯化钠固体中的氯酸钾:加热
D.除去盐酸中的水制备氯化氢气体:蒸馏
参考答案:A
本题解析:
本题难度:一般
5、填空题 (8分)由以下一些微粒: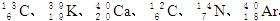 。其中:
。其中:
(1)互为同位素的是________和________;
(2)质量数相等,但不能互称同位素的是________和__________;
(3)中子数相等,但质子数不相等的是______和____ _、______和___? _。
参考答案:(1) (每空1分)
(每空1分)
本题解析:略
本题难度:一般