微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 A2+B2===2AB的反应历程可以看作如下(△H表示该过程的能量变化):
Ⅰ.A2==="A" +A?△H 1 ?Ⅱ.B2==="B" +B?△H 2 ?Ⅲ.A+B===AB?△H 3
则下列说法中正确的是( )
A.当△H3+(△H1+△H2) >0时,该反应是吸热反应;
B.当 2△H3+(△H1+△H2) > 0时,该反应是放热反应;
C.当 2△H3+(△H1+△H2 ) <0时,该反应是放热反应;
D.当1/2△H3+(△H1+△H2)<0时,该反应是吸热反应;
参考答案:C
本题解析:根据盖斯定律可知,I+Ⅱ+Ⅲ×2即得到反应A2+B2===2AB,所以该反应的反应热是△H= 2△H3+(△H1+△H2 )。因此选项C正确,答案选C。
点评:在根据多个热化学方程式计算有关的反应热时,盖斯定律是最重要的定律,需要熟练掌握并能灵活运用。
本题难度:一般
2、选择题 下列热化学方程式中,正确的是
A.甲烷的燃烧热为890.3 kJ・mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H=-890.3 kJ・mol-1
B.由N2(g)+3H2(g) 2NH3(g)△H=-92.4 kJ・mol-1热化学方程式可知, 当反应中转移6NA电子时,反应放出的热小于92.4 kJ
2NH3(g)△H=-92.4 kJ・mol-1热化学方程式可知, 当反应中转移6NA电子时,反应放出的热小于92.4 kJ
C.HCl和NaOH反应的中和热△H="-57.3" kJ・mol-1,则H2SO4和Ca(OH)2反应的中和热△H=2×(-57.3)kJ・mol-1
D.在101 kPa时,2gH2完全燃烧生成液态水,放出285.8kJ热量,氢气燃烧的热化学方程式表示为2H2(g)+O2(g)=2H2O(1)△H=-571.6 kJ・mol-1
参考答案:D
本题解析:A、甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)=CO2(g)+2H2O(l)?△H=-890.3 kJ・mol-1,错误;B、反应放出的热等于92.4 kJ,错误;C、有CaSO4沉淀生成,错误。
本题难度:一般
3、选择题 据人民网报道,有一集团拟在太空建立巨大的激光装置,把太阳光变成激光用于分解海水制氢气,其反应式可表示为:2H2O 2H2↑+O2↑。有下列几种说法:①水的分解反应是放热反应;②氢气是一级能源;③使用氢气作燃料有助于控制温室效应;④若用生成的氢气与空气中多余的二氧化碳反应生成甲醇储存起来,可改善人类的生存环境。以上叙述中正确的是
2H2↑+O2↑。有下列几种说法:①水的分解反应是放热反应;②氢气是一级能源;③使用氢气作燃料有助于控制温室效应;④若用生成的氢气与空气中多余的二氧化碳反应生成甲醇储存起来,可改善人类的生存环境。以上叙述中正确的是
A.①②
B.②③
C.③④
D.①②③④
参考答案:C
本题解析:①水的分解反应是吸热反应;②氢气是二级能源;温室效应主要是二氧化碳气体产生的;利用多余二氧化碳与氢气,生成甲醇,可以做能源,即变废为宝。故:③④是正确的。选C。
点评:氢气与氧气反应属于放热反应;根据盖斯定律水的分解反应是吸热反应;能源可分为一级能源和二级能源,自然界中直接提供的为一级能源,需要消耗其它能源的能量间接获取的能源为二级能源。
本题难度:简单
4、选择题 与离子方程式Fe3++3OH-====Fe(OH)3↓相对应的化学方程式是(? )
A.FeSO4+2NaOH====Fe(OH)2↓+Na2SO4
B.2Fe(NO3)3+3Mg(OH)2====2Fe(OH)3↓+3Mg(NO3)2
C.Fe2(SO4)3+3Ba(OH)2====2Fe(OH)3↓+3BaSO4↓
D.Fe2(SO4)3+6NaOH====2Fe(OH)3↓+3Na2SO4
参考答案:D
本题解析:表示可溶性铁盐与可溶性碱反应生成Fe(OH)3沉淀和可溶性盐。
本题难度:简单
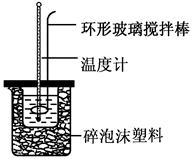
5、实验题 (共6分)实验室用50 mL 0.50 mol・L-1盐酸、50 mL 0.55 mol・L-1 NaOH溶液和如图所示装置,进行测定中和热的实验,得到表中的数据:
实验次数
| 起始温度t1/℃
| 终止温度t2/℃
|
盐酸
| NaOH溶液
|
1
| 20.2
| 20.3
| 23.7
|
2
| 20.3
| 20.5
| 23.8
|
3
| 21.5
| 21.6
| 24.9
|
完成下列问题:
(1)实验时不能用铜丝搅拌棒代替环形玻璃搅拌棒的理由是?。
(2)在操作正确的前提下,提高中和热测定准确性的关键是?。
(3)根据上表中所测数据进行计算,则该实验测得的中和热ΔH=?[盐酸和NaOH溶液的密度按1 g・cm-3计算,反应后混合溶液的比热容(c)按4.18 J・(g・℃)-1计算]。如用0.5 mol/L的盐酸与NaOH固体进行实验,则实验中测得的“中和热”数值将?(填“偏大”、“偏小”、 “不变”)。
(4)若某同学利用上述装置做实验,有些操作不规范,造成测得中和热的数值偏低,请你分析可能的原因是?
A.测量盐酸的温度后,温度计没有用水冲洗干净
B.把量筒中的氢氧化钠溶液倒入小烧杯时动作迟缓
C.做本实验的当天室温较高
D.将50mL0.55mol/L氢氧化钠溶液取成了50mL0.55mol/L的氨水
E.在量取盐酸时仰视计数
F.大烧杯的盖板中间小孔太大
参考答案:(6分) (1)? Cu传热快,热量损失大? (2)提高装置的保温效果
(3) -56.8 kJ・mol-1?偏大 氢氧化钠固体溶于水放热?(4)ABDF
本题解析:中和热测定实验的关键是确保装置的保温效果,防止热量的流失。
(3)由题给数据可知△H= ―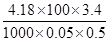 =-56.8 kJ・mol-1
=-56.8 kJ・mol-1
(4)误差分析:
A:温度计上的酸未用水冲洗干净,再去测碱溶液温度,残留的酸与碱反应,放热散失,所以导致后来实验中反应放出的热量减少,因此结果是偏低
B:把量筒中的氢氧化钠溶液倒入小烧杯时动作迟缓,会导致热量的损失
C:做本实验的当天室温较高,比较有利于实验的成功;
D:将50mL0.55mol/L氢氧化钠溶液取成了50mL0.55mol/L的氨水,弱碱在电离中需要消耗能量,会导致结果偏低;
E:在量取盐酸时仰视计数导致量取的盐酸偏多,造成中和热数值偏高。
F.大烧杯的盖板中间小孔太大,会导致热量的损失
本题难度:一般