微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列说法正确的是? ( )
A.离子化合物的熔点一定比共价化合物的高
B.二氧化碳分子中存在共价键和分子间作用力
C.非极性键也可以存在于化合物中
D.甲烷、氨和水都是由极性键结合而成的极性分子
参考答案:C
本题解析:若共价化合物是原子晶体,如SiO2的熔点比一般的离子化合物的熔点要高,故A错;分子间作用力不存在于分子内,只存在于分子间,B错;H2O2中存在非极性键,故C正确;甲烷是非极性分子,故D错。
本题难度:一般
2、选择题 R、Q为短周期中的两种元素,R元素原子的最外层电子数与次外层电子数之差的绝对值等于电子层数;Q元素的原子比R元素的原子多2个核外电子,则下列叙述中肯定不正确的是
A.R和Q可形成离子化合物
B.R和Q可形成共价化合物RQ3
C.原子半径:R>Q
D.R和Q可形成非极性分子RQ2
参考答案:A
本题解析:略
本题难度:一般
3、选择题 下列化学式对应的结构式从成键情况看不合理的是
[? ]
A.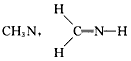
B.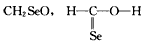
C.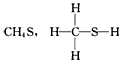
D.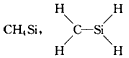
参考答案:D
本题解析:
本题难度:一般
4、选择题 X、Y、Z均为第三周期元素,X的第一电离能在同周期中最小,Y的电负性在同周期中最大,Z的离子半径在同周期中最小,下列关于X、Y、Z叙述不正确的是( )
A.元素Y形成的气态氢化物极易溶于水,水溶液呈强酸性
B.元素X与元素Y能形成离子化合物
C.元素Z最高价氧化物对应水化物既能与强酸反应,又能与强碱
D.原子序数和原子半径大小顺序均为:X<Y<Z
参考答案:X、Y、Z均为第三周期元素,X的第一电离能在同周期中最小,X为Na元素,Y的电负性在同周期中最大,Y为Cl元素,Z的离子半径在同周期中最小,Z为Al元素,
A、Y为Cl元素,其气态氢化物是HCl,极易溶于是,溶于水呈强酸性,故A正确;
B、X为Na元素,Y为Cl元素,二者形成的化合物是氯化钠,属于离子化合物,故B正确;
C、Z为Al元素,其最高价氧化物对应水化物羧基氢氧化铝,氢氧化铝是两性氢氧化物,既能与强酸反应,又能与强碱反应,故C正确;
D、原子序数Na<Al<Cl,同周期随原子序数增大,原子半径减小,原子半径Na>Al>Cl,故D错误;
故选D.
本题解析:
本题难度:简单
5、选择题 下列物质的电子式书写正确的是( )
A.NaCl
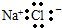
B.H2S
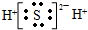
C.-CH3
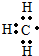
D.NH4I
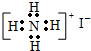
参考答案:C
本题解析:
本题难度:一般