微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列物质只含共价键,不含离子键的是( ? )
A.Ca(OH)2
B.CO2
C.MgCl2
D.NH4Cl
参考答案:B
本题解析:
本题难度:简单
2、简答题 现有下列短周期元素性质的数据:
?元素编号
元素性质 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧
原子半径
(10-10m)
0.74
1.02
1.52
1.10
0.99
1.86
0.75
1.43
|
最高或最
低化合价
+6
+1
+5
+7
+1
+5
+3
-2
-2
-3
-1
-3
|
回答下列问题:
(1)元素③在周期表中位置是______;?元素④与元素⑦相比较,气态氢化物较稳定的是______(填化学式);
(2)元素①是______(写元素符号),元素⑥是______(写元素符号),二者按照原子个数比为1:1形成的化合物与水反应的化学方程式为______;
(3)元素⑤与元素②的非金属性强弱顺序为______(写元素符号),元素⑤的单质加入到元素②的氢化物的水溶液中,反应的化学方程式为______;
(4)用电子式表示元素①氢化物的形成过程______;写出元素⑦氢化物的电子式______;写出实验室制元素⑤单质的化学反应方程式______.
参考答案:+1价的③、⑥,一定是碱金属Li和Na,而原子半径⑥>③,故③应为IA族第二周期的Li,⑥为三周期的Na元素;④和⑦最高正价均为+5,负价一致,故为VA族元素,因原子半径④>⑦,故④为第三周期第VA族的P元素,⑦为N元素;从化合价可推出⑤属于卤素,由于短周期F元素无正价,故⑤为氯元素,位于第VIIA族第三周期;⑧最高正价+3价,无负价,只能是IIIA族元素,而原子半径⑧>④,故⑧只能是位于第三周期第IIIA族的Al元素;①②的最低负价为-2价,①无正价,则①应为第二周期的O元素,②最高正价+6价,为第三周期的S元素,则
(1)③为Li元素,原子序数为3,核外有2个电子层,最外层电子数为1,位于周期表第二周期ⅠA族,非金属性:N>P,则氢化物较稳定的是?NH3,
故答案为:第二周期ⅠA族;NH3;
(2)①为Na元素,⑥为O元素,二者按照原子个数比为1:1形成的化合物为Na2O2,与水反应生成NaOH和O2,反应的方程式为2Na2O2+2H2O=4NaOH+O2↑,
故答案为:O;?Na;2Na2O2+2H2O=4NaOH+O2↑;
(3)同周期元素从左到右元素的非金属性逐渐增强,则非金属性Cl>S,Cl2通入H2S的水溶液中发生氧化还原反应生成HCl和S,反应的方程式为Cl2+H2S=2HCl+S↓,
故答案为:Cl>S;Cl2+H2S=2HCl+S↓;
(4)①的氢化物为H2O,用电子式表示的形成过程为
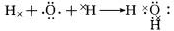
,⑦的氢化物为,属于共价化合物NH3,电子式为
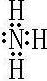
,实验室由浓盐酸和MnO2在加热条件下发生反应制备氯气,反应的化学方程式为MnO2+4HCl(浓)?△?.?MnCl2+Cl2↑+2H2O,
故答案为:
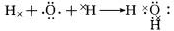
;
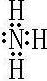
;MnO2+4HCl(浓)?△?.?MnCl2+Cl2↑+2H2O.
本题解析:
本题难度:一般
3、选择题 下列有关金属键的叙述中错误的是
[? ]
A.金属键没有饱和性和方向性
B.金属键是金属阳离子和自由电子之间存在的强烈的静电吸引作用
C.金属键中的电子属于整块金属
D.金属的性质和金属固体的形成都与金属键有关
参考答案:B
本题解析:
本题难度:简单
4、填空题 (14分)甲、乙、丙为常见单质,乙、丙两元素在周期表中位于 同一主族。X、A、B、C、D、E、F、G均为常见的化合物,其中A和X的摩尔质量相同,A、G的焰色反应为黄色。在一定条件下,各物质相互转化关系如右图。请回答:
同一主族。X、A、B、C、D、E、F、G均为常见的化合物,其中A和X的摩尔质量相同,A、G的焰色反应为黄色。在一定条件下,各物质相互转化关系如右图。请回答:
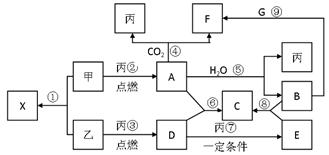
(1)写化学式:丙_____??E________
(2)X的电子式为_____________。
(3)写出反应⑥的化学反应方程式:?。
(4)写出B与G溶液反应生成F的离子方程式:?。
(5)在上图的反 应中,不属于氧化还原反应的是(填序号)____________________。
应中,不属于氧化还原反应的是(填序号)____________________。
(6)将8 g乙在足量丙中燃烧,所得气体D通入100mL 3.5mol・L-1的B溶液中,完全吸收 后,溶液中的溶质及其物质的量分别为?;若同体积的气体D通入100mL 2.5mo
后,溶液中的溶质及其物质的量分别为?;若同体积的气体D通入100mL 2.5mo l・L-1的B溶液中,完全吸收后,溶液中所含离子的物质的量浓度由大到小的顺序为??。
l・L-1的B溶液中,完全吸收后,溶液中所含离子的物质的量浓度由大到小的顺序为??。
参考答案:(1) O2 ?SO3?(2)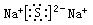 ?(3) 2Na
?(3) 2Na 2O2 + 2H2O="=4NaOH" + O2↑
2O2 + 2H2O="=4NaOH" + O2↑
(4) HCO3- + OH-==CO32- + H2O?(5)⑧⑨?(每题2分)
(6)0.1 5mol NaHSO3和0.1 mol Na2SO3
c(Na+)>c(HSO )>c(H+)>c(SO
)>c(H+)>c(SO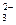 )>c(OH-)
)>c(OH-)
本题解析:略
本题难度:简单
5、填空题 下表是元素周期表的一部分。表中所列的字母分别代表一种化学元素。
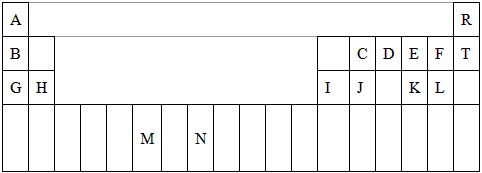
|
试回答下列问题
(1)请写出G的淡黄色化合物与二氧化碳反应的方程式________________________。
(2)D的气态氢化物的VSEPR模型为__________,其中心原子的杂化类型为__________________。
(3)G、H和I的第一电离能数值由大到小的顺序为:______________________(用元素符号作答)。
(4)由A、C、D形成的ACD分子中,含有__________个σ键,__________个π键。
(5)元素M的化合物(MO2Cl2)在有机合成中可作氧化剂或氯化剂,能与许多有机物反应。
请回答下列问题
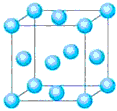
①与M同周期的所有元素的基态原子中最外层电子数与M原子相同的元素还有_______________(填元素符号),其中一种金属的晶胞结构如图所示,该晶胞中含有金属原子的数目为_______________。
②MO2Cl2常温下为深红色液体,能与CCl4、CS2等互溶,据此可判断MO2Cl2是__________(填“极性”或“非极性”)分子。
③在C2H4、CH3Cl、CH2O、CS2、CCl4五种有机化合物中,碳原子采取sp2杂化的分子有___________________________(填分子式)。
参考答案:(1)2Na2O2+2CO2=2Na2CO3+O2
(2)四面体;sp3
(3)Mg>Al>Na
(4)2;2
(5)①K、Cu;4;②非极性;③ C2H4、CH2O
本题解析:
本题难度:一般