微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列物质中,可用作冶炼镁的原料的是( )
A.冰晶石
B.光卤石
C.萤石
D.高岭石
参考答案:B
本题解析:
本题难度:简单
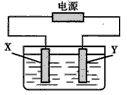
2、填空题 在如下图所示装置中,X和Y均为石墨电极。
I.
(1)若电解液为滴有酚酞的饱和食盐水,电解反应的离子方程式为 ____,____极(填“阴”或“阳”)附近会出现红色。
Ⅱ.若电解液为500mL,含溶质的某蓝色溶液,电解一段时间,观察到X电极表面有红色的固态物质生成,Y电极有无色气体生成;溶液中原有溶质完全电解后,停止电解,取出X电极,洗涤、干燥、称量,电极增重1. 6g。
(2)电解后溶液的H+浓度为____(假设电解前后溶液的体积不变),要使电解后溶液恢复到电解前的状态,需加入一定量的____(填加入物质的化学式)。
(3)请你推测原溶液中所含的酸根离子可能是____。设计实验验证你的推测,写出实验的操作步骤、现象和结论_____________________________________。
参考答案:(1) 2Cl-+2H2O 2OH-+2Cl2↑+H2↑; 阴
2OH-+2Cl2↑+H2↑; 阴
(2)0.1mol/L; CuO(或CuCO3)
(3)硫酸根离子; 取少量待测溶液于试管中,滴加盐酸无明显现象,继续加入氯化钡溶液,若有白色沉淀产生,则证明是硫酸根离子。(或:硝酸根离子取待测液于试管中,加热浓缩后滴加浓硫酸和铜粉,若有红棕色气体产生,则证明是硝酸根离子)
本题解析:
本题难度:一般
3、选择题 对于铁、铜、金的冶炼,下列说法错误的是( )
A.工业上用铝单质与Fe2O3反应来大规模制备生铁
B.可用焦碳与氧化铜高温反应制备铜
C.古代“沙里淘金”是将金单质富积
D.工业上由生铁炼钢以及由粗铜(含杂质较多的铜)制备纯铜都是进一步除去里面杂质
参考答案:A
本题解析:
本题难度:一般
4、简答题 工业上以海水为原料可获得金属镁及其多种化合物.其中Mg(OH)2是制备镁盐、耐火材料和阻燃剂等的重要原料.已知:①25℃时,Mg(OH)2的溶度积Ksp=5.6×10-12;
②Mg(OH)2(s)=MgO(s)+H2O(g)△H=+81.5kJ?mol-1.试回答下列问题:
(1)下列叙述正确的是______.(填字母序号)
A.从海水中获得Mg(OH)2工业上选择?NaOH作沉淀剂
B.Mg(OH)2能用作阻燃剂主要因为分解吸热且生成MgO覆盖可燃物
C.工业上由Mg(OH)2制金属镁的流程如下:

(2)已知酸碱指示剂百里酚蓝变色的pH范围如下:
| pH | <8.0 | 8.0~9.6 | >9.6
颜色
黄色
绿色
蓝色
|
25℃时,Mg(OH)2的饱和溶液中滴加2滴百里酚蓝指示剂,溶液所呈现的颜色为______.
(3)达喜是中和胃酸的常用药物,其有效成分是铝和镁的碱式碳酸盐(可能带有结晶水).现进行如下实验确定化学式:
实验一:取该碱式盐3.01g充分灼烧至恒重,测得固体质量减少了1.30g;
实验二:再取该碱式盐3.01g使其溶于足量的盐酸中,产生CO2的体积为112mL(标准状况);
实验三:向实验二的溶液中加入足量的NaOH溶液得到1.74g白色沉淀.
①达喜中Mg2+与Al3+的物质的量之比为______.
②计算达喜的化学式,写出必要的计算过程.
参考答案:(1)A、从海水中获得Mg(OH)2工业上选择?NaOH作沉淀剂,不符合生产的经济效益,故A不符合;
B、分解吸热且生成MgO难溶会覆盖可燃物,故B符合;
C、氯化镁溶液应在氯化氢气流中蒸发结晶,故C不符合;
故答案为:B;?
(2)25℃时,Mg(OH)2的溶度积Ksp=5.6×10-12;c(Mg2+)c2(OH-)=5.6×10-12;Mg(OH)2(s)?Mg2++2OH-;c(OH-)=2c(Mg2+)=x,得到0.5x×x2=5.6×10-12;
计算得到x=2.24×10-4mol/L;c(H+)=10-142.24×10-4=4.5×10-11mol/L,pH=10.4>9.6,所以溶液呈蓝色,
故答案为:蓝色;
(3)①实验一:取该碱式盐3.01g充分灼烧至恒重,测得固体质量减少了1.30g;减少的是二氧化碳气体和水蒸气的质量;灼烧得到固体为氧化铝和氧化镁的混合物;
实验二:再取该碱式盐3.01g使其溶于足量的盐酸中,产生CO2的体积为112mL(标准状况);可以计算碳元素物质的量;
实验三:向实验二的溶液中加入足量的NaOH溶液得到1.74g白色沉淀.判断不是沉淀为氢氧化镁沉淀;
可得n(CO2)=n(CO32-)=0.112L22.4L/mol=0.005mol,
3.01g碱式碳酸盐中,含:n(Mg2+)=n[Mg(OH)2]=1.74g58g/mol=0.03mol
依据Al2O3和MgO质量为3.01g-1.30g=1.71g;依据元素守恒计算得到:n(Al3+)=2n(Al2O3)=2×(3.01-1.30-0.03×40)÷102=0.01mol;
得到n(Mg2+):n(Al3+)=0.03mol:0.01mol=3:1,
故答案为:3:1;
②3.01g碱式碳酸盐中,含:n(Mg2+)=n[Mg(OH)2]=1.74g58g/mol=0.03mol,依据Al2O3和MgO质量为3.01g-1.30g=1.71g,依据元素守恒计算得到
n(Al3+)=2n(Al2O3)=2×(3.01-1.30-0.03×40)102=0.01mol,
n(CO32-)=n(CO2)=0.005mol,
n(OH-)=(0.03×2+0.03×3-0.005×2)=0.08mol,
n(H2O)=(1.30-0.04×18-0.005×44)18=0.02mol,
所以n(Al3+):n(Mg2+):n(OH-):n(CO32-):n(H2O)=0.01mol:0.03mol:0.08mol:0.005mol:0.02mol=2:6:16:1:4,
即碱式碳酸盐的化学式为:Al2Mg6(OH)16CO3?4H2O,
答:达喜的化学式为Al2Mg6(OH)16CO3?4H2O.
本题解析:
本题难度:一般
5、选择题 下列描述中正确的是
[? ]
A.电解法制镁时一般是用熔融态的氯化镁进行电解,但也可用氯化镁溶液
B.电解法生产铝时,可用钢网代替碳棒作阳极增大接触面积
C.我国第五套人民币中的一元硬币材料为钢芯镀镍,在硬币制作时,钢芯应做阴极
D.用电解法制备高纯度的镍,粗镍做阴极,精镍作阳极,阳极质量的减少与阴极质量的增加相等
参考答案:C
本题解析:
本题难度:一般