微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 已知强酸与强碱在稀溶液里反应的中和热可表示为:
H+(aq)+OH-(aq)===H2O(l) ΔH=-57.3 kJ/mol,对下列反应:
CH3COOH(aq)+NaOH(aq)===CH3COONa(aq)+H2O(l) ΔH=-Q1 kJ/mol[
H2SO4(浓)+NaOH(aq)===Na2SO4(aq)+H2O(l) ΔH=-Q2 kJ/mol
HNO3(aq)+NaOH(aq)===NaNO3(aq)+H2O(l)? ΔH=-Q3 kJ/mol
上述反应均在溶液中进行,则下列Q1、Q2、Q3的关系正确的是
A.Q2>Q3>Q1
B.Q2>Q1>Q3
C.Q1=Q2=Q3
D.Q2=Q3>Q1
参考答案:A
本题解析:CH3COOH(aq)+NaOH(aq)===CH3COONa(aq)+H2O(l) 为弱酸与强碱反应,弱酸电离出H+时要吸热热量,所以该反应放出热量较57.3 kJ少;H2SO4(浓)+NaOH(aq)===Na2SO4(aq)+H2O(l) 反应中,浓硫酸稀释会热,其能量最终释放的最多,即大于57.3 kJ;HNO3(aq)+NaOH(aq)===NaNO3(aq)+H2O(l)属于强酸与强碱反应,释放的热量为57.3 kJ;
所以,其关系为:Q2>Q3>Q1?即选项A正确。
本题难度:一般
2、选择题 天然气燃烧过程中的能量转化方式为
A.热能转化为化学能
B.化学能转化为电能
C.化学能转化为热能
D.化学能转化为机械能
参考答案:C
本题解析:天然气是一种燃料,具备化学能,燃烧过程中主要转化为热能,应该为化学能转化为热能,C选项正确。A.热能转化为化学能的实例---太阳光分解水;B.化学能转化为电能的实例原电池装置;D.化学能转化为机械能最典型的实例就是内燃机工作原理。故选C。
点评:本题考查能量转化方式。难度不大,记住以上几种转化形式,可以迎刃而解。
本题难度:一般
3、选择题 下列说法正确的是(?)
A 化学键断裂过程中放出热量?
B 化学键形成过程中需要吸收热量?
C 在一个确定的化学反应中,反应物的总能量与生成物的总能量可能相等
D 化学反应除了生成新的物质外,还伴随着能量的变化
参考答案:D
本题解析:考查化学反应中能量变化的原因。从宏观的角度分析,若反应物的总能量高于生成物的总能量,则反应是放热反应,反之是吸热反应。从微观的角度分析,如果断键吸收的能量高于形成化学键所放出的能量,则反应是吸热反应,反之是放热反应。所以选项D是正确的。
本题难度:一般
4、填空题 请参考题中图表,已知E1=134 kJ・mol-1、E2=368 kJ・mol-1,根据要求回答问题:
 ?
?
(1)图Ⅰ是1 mol NO2(g)和1 mol CO(g)反应生成CO2和NO过程中的能量变化示意图,若在反应体系中加入催化剂,反应速率增大,E1的变化是?(填“增大”、“减小”或“不变”,下同),ΔH的变化是?。请写出NO2和CO反应的热化学方程式:?。
(2)甲醇质子交换膜燃料电池中将甲醇蒸汽转化为氢气的两种反应的热化学方程式如下:
①CH3OH(g)+H2O(g)===CO2(g)+3H2(g)? ΔH=+49.0 kJ・mol-1
②CH3OH(g)+O2(g)===CO2(g)+2H2(g)? ΔH=-192.9 kJ・mol-1
又知③H2O(g)===H2O(l) ΔH=-44 kJ・mol-1,则甲醇蒸汽燃烧为液态水的热化学方程式为?。
(3)如表所示是部分化学键的键能参数:
化学键
| P―P
| P―O
| O===O
| P===O
|
键能/kJ・mol-1
| a
| b
| c
| x
|
?
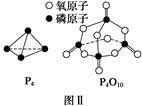
已知白磷的燃烧热为d kJ・mol-1,白磷及其完全燃烧的产物的结构如图Ⅱ所示,则表中x=??kJ・mol-1(用含a、b、c、d的代表数式表示)。
参考答案:(1)减小 不变 NO2(g)+CO(g)===CO2(g)+NO(g) ΔH=-234 kJ・mol-1
(2)CH3OH(g)+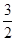 O2(g)===CO2(g)+2H2O(l) ΔH=-764.7 kJ・mol-1
O2(g)===CO2(g)+2H2O(l) ΔH=-764.7 kJ・mol-1
(3)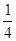 (d+6a+5c-12b)
(d+6a+5c-12b)
本题解析:(1)观察图像,E1应为反应的活化能,加入催化剂反应的活化能降低,但是ΔH不变;1 mol NO2(g)和1 mol CO(g)反应生成CO2和NO的反应热数值即反应物和生成物的能量差,因此该反应的热化学方程式为NO2(g)+CO(g)===CO2(g)+NO(g) ΔH=-234 kJ・mol-1。
(2)观察方程式,利用盖斯定律,将所给热化学方程式作如下运算:②×3-①×2+③×2,即可求出甲醇蒸汽燃烧的热化学方程式。
(3)白磷燃烧的化学方程式为P4+5O2 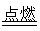 P4O10,结合图Ⅱ中白磷及其完全燃烧产物的结构,根据“反应热=反应物键能总和-生成物键能总和”与燃烧热概念可得等式:6a+5c-(4x+12b)=-d,据此可得 x=
P4O10,结合图Ⅱ中白磷及其完全燃烧产物的结构,根据“反应热=反应物键能总和-生成物键能总和”与燃烧热概念可得等式:6a+5c-(4x+12b)=-d,据此可得 x=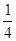 (d+6a+5c-12b)。
(d+6a+5c-12b)。
本题难度:一般
5、选择题 已知(l)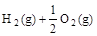 ?=H2O(g)?ΔH1=a kJ・
?=H2O(g)?ΔH1=a kJ・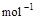
(2)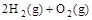 ?=2H2O(g)?ΔH2=b kJ・
?=2H2O(g)?ΔH2=b kJ・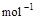
(3)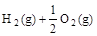 =H2O(l)?ΔH3=c kJ・
=H2O(l)?ΔH3=c kJ・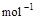
(4)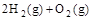 ?=2H2O(l)?ΔH4=d kJ・
?=2H2O(l)?ΔH4=d kJ・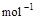
下列关系式中正确的是
A. a<c <0
B.b>d>0
C.2a=b<0
D.2c=d>0
参考答案:C
本题解析:氢气与氧气反应生成水是放热反应,所以ΔH的值是小于0的,故BD错误,H2O(l)变成H2O(g)需要吸收能量,即a大于c,所以A错误,答案为C。
点评:本题考查了反应热的比较,注意要理解ΔH的意义,才能选择出正确的选项。
本题难度:简单