微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列物质在水溶液中电离,其电离方程式错误的是( )
A.Al2(SO4)3=2Al3++3(SO4)2-
B.NaHSO4=Na++H++SO42-
C.MgCl2=Mg2++Cl2-
D.Ba(OH)2=Ba2++2OH-
参考答案:AC
本题解析:
本题难度:简单
2、选择题 下列电离方程式中书写正确的是?
[? ]
A.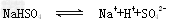
B.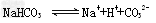
C.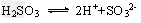
D.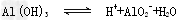
参考答案:D
本题解析:
本题难度:一般
3、选择题 下列各项表述正确的是?
[? ]
A.次氯酸的电子式: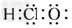 ?
?
B.表示中和热的热化学方程式:NaOH(aq)+HF(aq)= NaF(aq)+H2O(l)?△H=-57.3?kJ/mol
C.H2S的电离方程式为H2S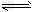 2H++S2- ?
2H++S2- ?
D.标准状况下,1.12?L16O2和1.12?L18O2均含有0.1NA个氧原子
参考答案:D
本题解析:
本题难度:简单
4、填空题 (10分)现有常温下的五份溶液:
①0.01 mol・L-1 CH3COOH溶液; ②0.01 mol・L-1 HCl溶液;
③pH=12的氨水; ④pH=12的NaOH溶液;
⑤0.01 mol・L-1 HCl溶液与pH=12的NaOH溶液等体积混合所得溶液。
(1)其中水的电离程度最大的是______(填序号,下同),水的电离程度相同的是______;
(2)若将②、③混合后所得溶液pH=7,则消耗溶液的体积:②________③(填“>”、“<”或“=”);
(3)将前四份溶液同等稀释10倍后,溶液的pH:
①________②,③________④ (填“>”、“<”或“=”);
参考答案:(1)⑤ ②③④ (2)> (3)> >
本题解析:(1)⑤0.01 mol・L-1 HCl溶液与pH=12的NaOH溶液等体积混合,恰好反应,所得溶液是氯化钠溶液,强酸强碱盐,对水的电离没有影响,①②③④属于酸或碱,对水的电离其抑制作用,所以其中水的电离程度最大的是⑤;②③④溶液是强酸、弱碱、强碱,溶液中氢离子和氢氧根离子浓度相同,对水的电离抑制程度相同,则水的电离程度相同的是②③④;(2 ) ②③若等体积混合后溶液呈碱性,若使溶液pH=7,则消耗溶液的体积:②>③ ;(3) 同浓度醋酸和盐酸稀释相同倍数,浓度仍然相同,但醋酸存在电离平衡,醋酸溶液中氢离子浓度小于盐酸溶液中的氢离子浓度,酸性越弱,pH越大,所以溶液PH①>②,PH值相同的氨水和氢氧化钠,稀释相同的倍数,氨水继续电离,溶液中氢氧根离子浓度大于氢氧化钠溶液中氢氧根离子,pH值③>④。
考点:考查弱电解质的电离平衡。
本题难度:一般
5、选择题 常温下,某溶液中由水电离产生的c(H+)=1×10-11mol・L-1,则该溶液的pH可能是
[? ]
A.3
B.7
C.8
D.11
参考答案:AD
本题解析:
本题难度:一般