��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ʵ���� (18��)ij��ѧ��һ������ȤС��Ϊ̽��ͭ������ķ�Ӧ������������ͼ��ʾװ�ý����й�ʵ�顣

��1���ȹرջ���a����6.4gͭƬ��12 mLijŨ�ȵ�Ũ�������Բ����ƿ�й�������Ӧ��ϣ�������ƿ�л���ͭƬʣ�ࡣ�ٴ���a���������е�������������Բ����ƿ�����ͭƬ��ȫ��ʧ��
��д��������������ƿ�ڷ����Ļ�ѧ����ʽ���رջ���a?��
����a?��
��B�������ռ�ʵ���в����������װ�ã�������δ��ȫ��������ͼ�аѵ��ܲ���������
��ʵ�������װ��C�е���Һ�п��ܺ��е�������?��
��2����С���ͬѧ�ԡ���μ���SO2�л�������CO2���������ܸ���Ȥ������A��ͭƬ����ľ̿�ۣ�����A��B֮������������װ�ã�

�Լ���a. NaOH��Һ? b. Ʒ����Һ? c. ����KMnO4��Һ? d. Ca(OH)2��Һ
��ش�
�ٸ�ͬѧ��ʵ��װ��A�з����Ļ�ѧ����ʽ? ?��
?��
����Ҫ�ﵽ��Ŀ�ģ������ڣ�(�����ṩ�Լ����)
D���?��E���?��F���?��
��3����ʵ֤ʵ���ڣ�1����ͭƬ��ȫ��ʧ����������ʣ�࣬��ͬѧ���ⶨ��������ʵ���Ũ�ȣ����跴Ӧǰ����Һ����仯���Բ��ƣ�����Ӧ����Һ�м��뺬����a mol ��NaOH��Һ�պ�ʹ��Һ��Cu2+ȫ���������ݴˣ����������������ʵ���Ũ�������ܣ���д���������ʵ���Ũ�ȵı���ʽ��?mol/L(
��NaOH��Һ�պ�ʹ��Һ��Cu2+ȫ���������ݴˣ����������������ʵ���Ũ�������ܣ���д���������ʵ���Ũ�ȵı���ʽ��?mol/L( �ú�a�Ĵ���ʽ��������ܣ��ÿղ���)��
�ú�a�Ĵ���ʽ��������ܣ��ÿղ���)��
�ο��𰸣�
��1����Cu+2H2SO4(Ũ)  CuSO4+SO2?+2H2O����2�֣�
CuSO4+SO2?+2H2O����2�֣�
2Cu+O2+2H2SO4 2CuSO4+2H2O ��2��
2CuSO4+2H2O ��2�� ��
��
(��ֲ�д�ɣ�2Cu+O2=2CuO��CuO+H2SO4=CuSO4+H2O��Ҳ��)
��
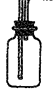 ? (2��)
? (2��)
��NaOH? Na2SO3? Na2SO4?��3�֣�
��2����C+2H2SO4��Ũ�� ?CO2?+2SO2?+2H2O?��3�֣�
?CO2?+2SO2?+2H2O?��3�֣�
��? c? b? d?��3�֣�
��3��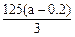 ?��3�֣������������ʽ���ɣ�
?��3�֣������������ʽ���ɣ�
�����������
�����Ѷȣ���
2��ʵ���� (10��)ij�о���ѧϰС��Ϊ̽��Cu(OH)2���ȷֽ���P�������ʣ��������ʵ�顣
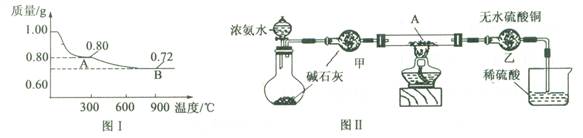
(1)ȡ0��98 g Cu(OH)2������ȣ��������¶ȱ仯��������ͼ1��ʾ������A��B�Ļ�ѧʽ�ֱ�Ϊ?��?��
(2)ȡ��������B����������ϡ���ᣬ�õ���ɫ��Һ��ͬʱ�۲쵽�����л��к�ɫ������ڣ��÷�Ӧ�����ӷ���ʽΪ?��
(3)Ϊ֤������A�ڼ���ʱ����NH3��Ӧ��ijͬѧ�������ͼ��(�г�װ��δ����)��ʾʵ��װ�á�
�ټ�������װ�������Եķ���?��
��ʵ������й۲쵽������������ iֱ�������й����ɺ�ɫ��Ϊ��ɫ��iiװ�����й����ɰ�ɫ��Ϊ��ɫ����֤������A��NH3�����˷�Ӧ���ж����ݵ���?(��ѡ����ĸ)��
a��ֻ��i����? b��ֻ��ii����? c��i��ii������
�ο��𰸣���1��CuO? Cu2O
��2��Cu2O + 2H+ = Cu2+ + Cu + H2O
��3������ͼ����װ�ã��رշ�Һ©����������ĩ�˵��ܽ���ˮ�У�����ë����ס��ƿ�ײ��������ܿ�����������ð����������ë������ȴ�����º����γ�һ��Һ���ҳ������䣬��֤��װ�����������á�
��b
�����������1��������ˮ��ļ�Cu(OH)2�ɼ�����ˮ��Cu(OH)2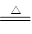 CuO��H2O���ɷ�Ӧǰ�����������ʵ�������Ϊ98��80��1.00��0.80�ɲ²��A����ΪCuO
CuO��H2O���ɷ�Ӧǰ�����������ʵ�������Ϊ98��80��1.00��0.80�ɲ²��A����ΪCuO
ͭ����������CuO��Cu2O��CuO��������������С�����ݷ�Ӧ��4CuO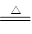 2Cu2O+O2���ɿ�������Ӧǰ�����������ʵ�������Ϊ80��72���������⣬�ʿ�֪B����ΪCu2O
2Cu2O+O2���ɿ�������Ӧǰ�����������ʵ�������Ϊ80��72���������⣬�ʿ�֪B����ΪCu2O
��2��Cu2O������������������ͭ���ʼ�����ͭ����᪻���Ӧ��Cu2O + 2H+ = Cu2+ + Cu + H2O
��3���ٹرշ�Һ©����������ĩ�˵��ܽ���ˮ�У�����ë����ס��ƿ�ײ��������ܿ�����������ð����������ë������ȴ�����º����γ�һ��Һ���ҳ������䣬��֤��װ�����������á�
��������֪����CuO���ȿɷֽ����ɺ�ɫ��Cu2O���ʡ�ֱ�������й����ɺ�ɫ��Ϊ��ɫ��������˵��������CuO�μ��˷�Ӧ��
���ڰ������������ˮ��õ���ˮ�İ���������ˮ����ͭ������˵����ˮ���ɣ������е���Ԫ��ֻ�������ڰ������ʴ��������Ϊ�����μӷ�Ӧ������
bѡ���������
�����Ѷȣ���
3������� ����A��B��C��D��E����������ˮ��ǿ����ʣ������������������(�������Ӳ��ظ�)��
������
| H+��NH4+��Mg2+��Ba2+��Al3+
|
������
| OH-��Cl-��HCO3-��NO3-��SO42-
|
��֪����0.1 mol/L? A��Һ��pH <1���ڽ�B��Һ�ֱ�������������Һ��ϣ����а�ɫ�������ɣ�
��C��Һ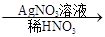 ��ɫ��������ش��������⣺
��ɫ��������ش��������⣺
��1��д���������ʵĻ�ѧʽ��A______________��B______________��
��2��д����C��Һ ��ɫ�������йط�Ӧ�����ӷ���ʽ____________________________��
��ɫ�������йط�Ӧ�����ӷ���ʽ____________________________��
��3��D��E���������б���һ����_______________��д�������������ʵ���Һ�μӵ�B��Һ�з�Ӧ�����ӷ���ʽ___________________________________________________________________��
��4���������ʵ��ȷ��C����һ��δ֪�����ʲô���ʡ�(ֻ����A��E��ѡ������Լ�)
ʵ�鲽��
| Ԥ������ͽ���
|
ȡ����C����Һ���Թ��У�?��?
?��
| Ԥ������ͽ���1��?��?��
Ԥ������ͽ���2��?��?��
�ο��𰸣�(14��)(1)����H2SO4? B��Ba(OH)2? (2)Ag+��Cl����AgCl��?����2�֣���6�֣�
(3) NH4HCO3? NH4����HCO3����Ba2����2OH����BaCO3����NH3��H2O��H2O?����2�֣���4�֣�
(4) �������м���������Ba(OH)2��Һ��?��2�֣�
������ʼ�а�ɫ�������ɣ������������ɣ���CΪAlCl3��
������ʼ�����а�ɫ�������ɣ���CΪMgCl2?����1�֣���2�֣�
(�������м�����ҺNH4HCO3�����������������а�ɫ�������ɣ���CΪAlCl3���������κ�������CΪMgCl2��? (����������ȷҲ����)
�����������1��0.1 mol/L A��Һ��pH��1����˵��AӦ���Ƕ�Ԫǿ�ᣬ����A�����ᡣ��B��Һ�ֱ�������������Һ��ϣ����а�ɫ�������ɣ���˵��B�к���OH����Ba2������B��������������һ������������炙��Ȼ�李�
��2��C��Һ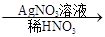 ��ɫ������˵��C�к��������ӣ���Ӧ�����ӷ���ʽ��Ag+��Cl����AgCl���� ��ɫ������˵��C�к��������ӣ���Ӧ�����ӷ���ʽ��Ag+��Cl����AgCl����
��3������ΪHCO3����Al3�����ܴ������棬��һ������������炙��Ȼ�泥�����D��E���������б���һ����NH4HCO3�������������ʵ���Һ�μӵ�B��Һ�з�Ӧ�����ӷ���ʽNH4����HCO3����Ba2����2OH����BaCO3����NH3��H2O��H2O��
��4���������Ϸ�����֪��C���Ȼ������Ȼ�þ��������һ������������þ������������˿��Ը����������������Խ��м��飬����Ҫ����C�ijɷ֣���ȷ�IJ���Ӧ���Ǣ������м���������Ba(OH)2��Һ��������ʼ�а�ɫ�������ɣ������������ɣ���CΪAlCl3��������ʼ�����а�ɫ�������ɣ���CΪMgCl2��
(�������м�����ҺNH4HCO3�����������������а�ɫ�������ɣ���CΪAlCl3���������κ�������CΪMgCl2��)
�����������ۺ���ǿ���ѶȽϴ�ѧ����˼ά����Ҫ��ߣ�ѧ�����÷֡�������ע�ض�ѧ������֪ʶ���̺ͼ����ͬʱ�����ض�ѧ�����������������ͽ��ⷽ����ָ����ѵ��������������ѧ���������������淶�Ͻ���ʵ���������������������ѧ����ѧ�����������ѧ����ѧϰЧ�ʺ�ѧϰ�����ԡ�ע�����֪ʶ�Ļ��ۡ��ܽ�����á�
�����Ѷȣ�һ��
4��ʵ����
(13��)����Ҫ��������и�С��ʵ��Ŀ�ġ���a��bΪ���ɼУ����ȼ��̶�װ������ȥ��
����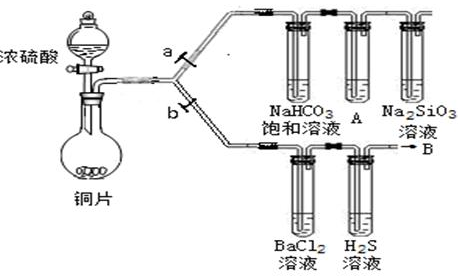
������1����֤̼����ǽ����Ե����ǿ��������֪���ԣ������̼�ᣩ
��������������������װ�������ԡ���ҩƷ��a�ر�b��Ȼ�����Ũ���ᣬ���ȡ�
������ͭ��Ũ���ᷴӦ�Ļ�ѧ����ʽ��___________________________��װ��A���Լ���________________��
��������˵��̼�ķǽ����Աȹ�ǿ��ʵ��������________________________________________________��
������2����֤SO2�������ԡ���ԭ�Ժ������������ͨ�ԡ�
�������ڣ�1���ٲ������b���ر�a��
������H2S��Һ����dz��ɫ���dz��֣���ѧ����ʽ��______________________________________��
������BaCl2��Һ��������������ֳ����ݣ��ֱ�μ�������Һ���������ij����Ļ�ѧʽ�����±���Ӧλ�á�����
�μӵ���Һ
| ��ˮ
| ��ˮ
| �����Ļ�ѧʽ
| ��
| ��
|
д������SO2��ʾ��ԭ�Բ����ɳ��������ӷ���ʽ__________________________________��
�����ܽ�KOH��Ca(OH)2�Ļ����1.3gȫ������һ����ˮ���γ�ϡ��Һ���ٻ���ͨ��һ������B���壬ʵ������пɵõ��������������Ϊ1.2g��
�����Լ��㣺ԭ�������KOH������Ϊ_____________g�����ɳ�������Ϊ���ʱ������B���壨��״���£��������V����Χ�ǣ�_____________________________________��
�ο��𰸣���1���� Cu + 2H2SO4(Ũ)  ��CuSO4 + SO2��+ 2H2O���� KMnO4��Һ ��CuSO4 + SO2��+ 2H2O���� KMnO4��Һ
������A��KMnO4��Һû����ȫ��ɫ��ʢ��Na2SiO3��Һ���Թ��г��ְ�ɫ����
������2����2H2S + SO2 =" 3S��" + 2H2O
������
��
��
��
?
BaSO4
BaSO3
?
����Ba2+ + SO2 + Cl2 + 2H2O ="=" BaSO4��+ 4H+ + 2Cl��
������0.56g���� 224mL �� V �� 448mL
�����������ע���������غ������IJ��֣�
��1���� Cu + 2H2SO4(Ũ)  ��CuSO4 + SO2��+ 2H2O���� KMnO4��Һ ��CuSO4 + SO2��+ 2H2O���� KMnO4��Һ
������A��KMnO4��Һû����ȫ��ɫ��ʢ��Na2SiO3��Һ���Թ��г��ְ�ɫ����
������2����2H2S + SO2 =" 3S��" + 2H2O
������
��
��
��
?
BaSO4
BaSO3
?
����Ba2+ + SO2 + Cl2 + 2H2O ="=" BaSO4��+ 4H+ + 2Cl��
������0.56g���� 224mL �� V �� 448mL
CO2ͨ��KOH��Ca(OH)2�Ļ����Һ�У���һ����ӦΪ
Ca��OH��2+CO2 CaCO3��+H2O,Ca(OH)2ǡ�÷�Ӧ��ʱ�����������ʱ����0.01 mol CO2����Ca(OH)2��CaCO3�����ʵ���Ϊ0.01 mol���ڶ�����ӦΪKOH+CO2 CaCO3��+H2O,Ca(OH)2ǡ�÷�Ӧ��ʱ�����������ʱ����0.01 mol CO2����Ca(OH)2��CaCO3�����ʵ���Ϊ0.01 mol���ڶ�����ӦΪKOH+CO2 KHCO3,KOH������Ϊ��1.3-0.01��74��g="0.56" g������n(KOH)="0.01" mol,�ڶ������ĵ�CO2ҲΪ0.01 mol ��������CaCO3+CO2+H2O KHCO3,KOH������Ϊ��1.3-0.01��74��g="0.56" g������n(KOH)="0.01" mol,�ڶ������ĵ�CO2ҲΪ0.01 mol ��������CaCO3+CO2+H2O Ca(HCO3)2,������0.01 mol CO2�����һ������ڶ�����Ӧ����������������䣬����CO2��ֵΪ0.01mol�D0.02mol֮�䣬���Ϊ224mL �� V �� 448mL�� Ca(HCO3)2,������0.01 mol CO2�����һ������ڶ�����Ӧ����������������䣬����CO2��ֵΪ0.01mol�D0.02mol֮�䣬���Ϊ224mL �� V �� 448mL��
�����Ѷȣ�һ��
5��ʵ���� ��5�֣�ijʵ��С����������װ�ã����̶ֹ�װ���ԣ��Ʊ�������(Ca3N2)����̽����ʵ��ʽ��
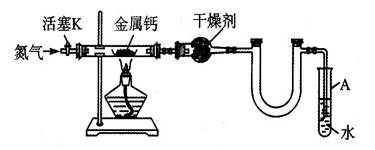
��1����ͼ���Ӻ�ʵ��װ�ã����װ�õ������Եķ�������������������������������
��2����Ӧ������ĩ�˵��ܱ���ʼ�ղ����Թ�A��ˮ�У�Ŀ������������������������
��3���Ʊ������ƵIJ��������Ǣٴ���K��ͨ��N2���ڵ�ȼ�ƾ��ƣ����з�Ӧ��
�۷�Ӧ���������������������ܲ��װ�ã�ȡ�����
��4�����ݼ�¼���£�
ֱ��������m0/g
| ֱ������Ƶ�����m1/g
| ֱ��������������m2/g
| 14.80
| 15.08
| 15.15
|
�ټ���õ�ʵ��ʽCaxN2������x����������������
����ͨ���N2�л�������O2����Ƚ�x��3�Ĵ�С���������ж����ݣ�
������������������������������������������������������������
�ο��𰸣���5�֣�
��1���رջ���K������ֱ���ܣ������ܿڴ��������ݣ�ֹͣ���Ⱥ������γ�һ��Һ���������������á�
��2����ֹ��Ӧ�����п������뷴Ӧ�ܣ����ڹ۲�N2����
��3��Ϩ��ƾ��ƣ�����Ӧ����ȴ�����£�ֹͣͨN2�����رջ���K
��4����2.80
��x��3������O2��N2���������Ca��Ӧ������CaO��������Ca3N2�����¼������n(N)ƫ��
������������ڽ�����Ϊ�ر���õĽ�����������ȡCa3N2�Ĺ����У����뱣֤ϵͳ���������������壬��֤���������ã�ʵ��ǰ��ͨ�뵪�����ټ��ȣ�ʵ�����ʱ����ֹͣ���ȡ���ȴ����ֹͣͨ����
��2����ֹ������װ���Ҷ˽���װ���ڣ�����ͨ���۲�������������������
��4�������������ݿ�֪�Ƶ�����Ϊ��15.08-14.80=0.28g����Ԫ�ص�����Ϊ��15.15-15.08=0.07g������Ԫ�ص�ԭ�Ӹ�����Ϊ��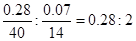 ����x=0.28 ����x=0.28
��O2��N2���������Ca��Ӧ������CaO��������Ca3N2�����¼������n(N)ƫ��x<3(����ü�ֵ�������ǣ�������ȫ��Ϊ����ʱ���õ�������ΪCaO����Ca2O2������ȫ��Ϊ����ʱ�õ���ΪCa3N2����ͨ���N2�л�������O2ʱ���������ʵķ���ʽ��x<3)
�����Ѷȣ�һ��
|