微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列物质中不含有氯离子的是
A.氯水
B.漂粉精
C.盐酸
D.液氯
参考答案:D
本题解析:分析:含有氯离子的化合物属于离子化合物,是由离子构成,注意混合物中可含氯离子,而液氯为单质,由分子构成,不含氯离子,以此来解答.
解答:A.氯水为混合物,含盐酸电离生成的氯离子,故A不选;
B.漂白精为混合物,含氯化钙,存在氯离子,故B不选;
C.盐酸为混合物,在水溶液中电离出氯离子,故C不选;
D.液氯为单质,由分子构成,不含氯离子,故D选;
故选D.
点评:本题考查物质的构成及电离,注意混合物的成分及物质的构成,液氯为单质,注意氯水与液氯的差别,题目难度不大.
本题难度:一般
2、选择题 与3-甲基-1-戊烯同属烯烃且主链为4个碳的同分异构体共有
A.3种
B.4种
C.5种
D.6种
参考答案:B
本题解析:可参见下面的碳链图示:
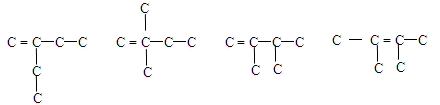
本题难度:困难
3、选择题 下列叙述不正确的是
A.CH4与C4H10互为同系物
B.C5H12有三种同分异构体
C.甲烷与氯气在三溴化铁催化下发生取代反应
D.苯分子中的碳碳键是介于单键和双键之间的独特的键
参考答案:C
本题解析:甲烷和氯气的取代反应,需要光照,选项C不正确,其余都是正确的,答案选C。
本题难度:简单
4、选择题 常温下,下列各组离子在指定溶液中一定能大量共存的是
A.能使甲基橙变黄的溶液中:Na+、K+、SO42-、AlO2-
B.加铝粉放出大量H2的溶液中:Na+、NH4+、SO42-、CO32-
C.c(OH-)/c(H+)=10-12的溶液中:NH4+、Cu2+、NO3-、Cl-
D.0.1mol?L-1NaHCO3溶液中:K+、Ba2+、OH-、Cl-
参考答案:C
本题解析:分析:A、能使甲基橙变黄的溶液可能为酸性,H+与AlO2-反应;
B、加铝粉放出大量H2的溶液,可能为酸或碱的溶液,H+与CO32-反应,NH4+、OH-反应;
C、c(OH-)/c(H+)=10-12的溶液为酸溶液,酸性溶液中离子之间不反应;
D、OH-、HCO3-反应,生成的碳酸根离子与Ba2+结合生成沉淀.
解答:A、能使甲基橙变黄的溶液可能为酸性,H+与AlO2-反应生成氢氧化铝沉淀,若为碱性溶液,能大量共存,则不一定大量共存,故A错误;
B、加铝粉放出大量H2的溶液,可能为酸或碱的溶液,若为酸溶液,则H+与CO32-反应生成二氧化碳和水,若为碱溶液,
NH4+、OH-反应生成一水和氨,则一定不能共存,故B错误;
C、c(OH-)/c(H+)=10-12的溶液中c(H+)=0.1mol/L,酸性溶液中离子之间不反应,则一定大量共存,故C正确;
D、0.1mol?L-1NaHCO3溶液中OH-、HCO3-、Ba2+结合生成碳酸钡沉淀和水,则一定不能大量共存,故D错误;
故选C.
点评:本题考查离子的共存问题,明确信息来分析溶液的酸性和碱性及溶液为酸碱溶液是解答本题的关键,难度不大.
本题难度:一般
5、选择题 下列离子方程式正确的是
A.氢氧化铁溶于氢碘酸中:Fe(OH)3+3H+=Fe3++3H2O
B.明矾溶液中加入氢氧化钡溶液,使其产生沉淀的物质的量达最大值:Al3++2SO42-+2Ba2++4OH-=2BaSO4↓+AlO2-+2H2O
C.Mg(HCO3)2溶液中加入过量石灰水:Mg2++2HCO3-+Ca2++2OH-=CaCO3↓+2H2O+MgCO3↓
D.向100?mL?0.1?mol/L的FeBr2溶液中通入0.012?mol?Cl2:10Fe2++14Br-+12Cl2=10Fe3++7Br2+24Cl-
参考答案:D
本题解析:分析:A.发生氧化还原反应,生成碘化亚铁、碘、水;
B.产生沉淀的物质的量达最大值,钡离子、铝离子均转化为沉淀;
C.Mg(HCO3)2完全反应,生成氢氧化镁沉淀、碳酸钙沉淀、水;
D.亚铁离子全部被氧化,溴离子部分被氧化.
解答:A.发生氧化还原反应,生成碘化亚铁、碘、水,离子反应为2Fe(OH)3+2I-+6H+=2Fe2++I2+6H2O,故A错误;
B.产生沉淀的物质的量达最大值,钡离子、铝离子均转化为沉淀,则离子反应为2Al3++3SO42-+3Ba2++6OH-=3BaSO4↓+2Al(OH)3↓,故B错误;
C.Mg(HCO3)2完全反应,生成氢氧化镁沉淀、碳酸钙沉淀、水,则离子反应为Mg2++2HCO3-+2Ca2++4OH-=2CaCO3↓+2H2O+Mg(OH)2↓,故C错误;
D.向100?mL?0.1?mol/L的FeBr2溶液中通入0.012?mol?Cl2,亚铁离子全部被氧化,溴离子部分被氧化,离子反应为10Fe2++14Br-+12Cl2=10Fe3++7Br2+24Cl-,故D正确;
故选D.
点评:本题考查离子反应方程式的书写,明确发生的化学反应是解答本题的关键,题目难度较大,注意D中电子守恒,C中应生成氢氧化镁为学生解答的易错点.
本题难度:简单