微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 用芒硝(Na2SO4 °10H2O)制备纯碱、明矾铵[(NH4)2Al(SO4)2°12H2O]的生产工艺流程如下图:
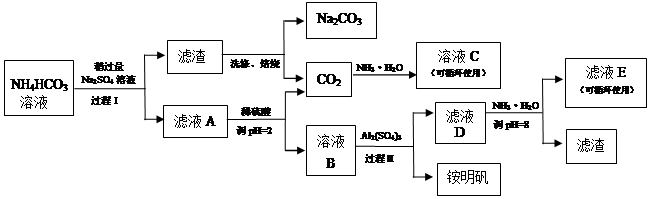
(1)溶液C中的溶质主要是_____________
(2)明矾铵的溶液呈_____性,明矾铵可用于净水,用离子方程式说明其原理______________________
(3)过程Ⅰ中的反应温度不能超过40℃,其原因是______________________________
(4)运用化学平衡原理解释Na2SO4稍过量的原因?
(5)若将Al2(SO4)3加入到A中会产生大量的沉淀和气体,导致明矾铵的产量降低,请用离子方程式解释产生该现象的原因是___________________________________________
(6)溶液E中的溶质离子为__________________
(7)已知明矾铵的溶解度随着温度的升高而增大,过程Ⅱ中得到明矾铵的系列实验操作是:?、?、过滤、洗涤、干燥。
参考答案:
(1) NH4HCO3
(2)酸? Al3+?+? 3H2O Al(OH)3? +? 3H+
Al(OH)3? +? 3H+
(3)NH4HCO3易受热分解
(4)HCO32―(aq)+? Na+(aq) NaHCO3(s),Na+浓度增大平衡向正反应方向移
NaHCO3(s),Na+浓度增大平衡向正反应方向移
(5)Al3+?+ 3HCO32―?=Al(OH)3↓ +? 3CO2↑
(6)NH4+ ?、SO42―
(7)蒸发浓缩、冷却结晶
本题解析:该题为工业流程题,经过一系列反应,提纯、结晶得到。(1)CO2与氨水反应生成NH4HCO3或(NH4)2CO3;(2)由于Al3+ 与NH4+水解使溶液呈现酸性,明矾铵可用于净水,是因为铝离子水解产生氢氧化铝胶体所致,Al3+?+? 3H2O Al(OH)3? +? 3H+;(3)NH4HCO3易受热分解,故反应应控制温度;(4)在平衡体系中增加一种反应物的浓度,反应正向进行,提高另外反应物的转化率;(5)双水解反应;(6)A为(NH4)2SO4和剩余的硫酸盐和碳酸盐,B主要为NH4HSO4,D主要为剩余的NH4HSO4、Al2(SO4)3,E为(NH4)2SO4;(7)明矾铵的溶解度随着温度的升高而增大,故采用降温结晶的方法分离,因滤液浓度低,所以需要浓缩,方法为蒸发浓缩、降温结晶(冷却结晶)。
Al(OH)3? +? 3H+;(3)NH4HCO3易受热分解,故反应应控制温度;(4)在平衡体系中增加一种反应物的浓度,反应正向进行,提高另外反应物的转化率;(5)双水解反应;(6)A为(NH4)2SO4和剩余的硫酸盐和碳酸盐,B主要为NH4HSO4,D主要为剩余的NH4HSO4、Al2(SO4)3,E为(NH4)2SO4;(7)明矾铵的溶解度随着温度的升高而增大,故采用降温结晶的方法分离,因滤液浓度低,所以需要浓缩,方法为蒸发浓缩、降温结晶(冷却结晶)。
本题难度:困难
2、选择题 下列有关能源叙述不正确的是
A.沼气是不可再生能源
B.太阳能是新能源
C.石油是化石燃料
D.风能是一次能源
参考答案:A
本题解析:略
本题难度:简单
3、选择题 有关材料用途的说法中不正确的是?
[? ]
A.氧化铝陶瓷可用做高压钠灯的灯管
B.氮化硅陶瓷可用做陶瓷发动机的材料
C.光导纤维可用做遥测遥控、照明等
D.氧化铝陶瓷可用做半导体材料
参考答案:D
本题解析:
本题难度:简单
4、填空题 古希腊流传这样一个传奇故事:一批运纯碱的商船停泊在江边的沙岸旁,商人找不到石头来搭灶,就把船上的大块纯碱搬来,放在沙地上垫锅做饭,饭熟后商人们惊奇地发现“灶”变成了晶莹透明的固体。这固体是______,沙子的主要成分是______。
参考答案:玻璃;SiO2
本题解析:
本题难度:一般
5、选择题 海水是重要的资源。可以制备一系列物质
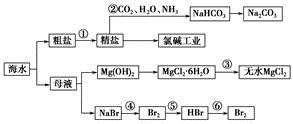
下列说法正确的是
A.步骤②中,应先通CO2,再通NH3
B.步骤③可将MgCl2・6H2O晶体在空气中直接加热脱水
C.步骤④、⑤、⑥反应中,溴元素均被氧化
D.除去粗盐中的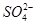 、Ca2+、Mg2+等杂质,加入试剂及相关操作顺序可以是:NaOH溶液→BaCl2溶液→Na2CO3溶液→过滤→盐酸
、Ca2+、Mg2+等杂质,加入试剂及相关操作顺序可以是:NaOH溶液→BaCl2溶液→Na2CO3溶液→过滤→盐酸
参考答案:D
本题解析:A项,步骤②为侯氏制碱法,由于NH3的溶解度比CO2大,故应先通NH3,再通CO2溶液中才能含有大量的碳元素,才能得到大量的NaHCO3,错误;MgCl2・6H2O直接加热脱水时,Mg2+水解生成HCl挥发出去,促进水解进行到底,得到Mg(OH)2。所以晶体加热脱水必须不断通入HCl,抑制水解,B项错;C项,步骤⑤中,Br化合价降低,被还原,错;D项,加NaOH能除去Mg2+,加Ba2+能除去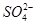 ,再加入Na2CO3可以除去Ca2+以及过量的Ba2+,过滤后加入盐酸可以除去多余的
,再加入Na2CO3可以除去Ca2+以及过量的Ba2+,过滤后加入盐酸可以除去多余的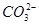 和OH-,正确。
和OH-,正确。
本题难度:一般