��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� (10�֣�
2006����������ӵ���ܲ�������25��ֻ��﮵���������Բ��������Ľ�����Դ���������൱��ġ��������ӵ�ػ��վ�����Ҫ���壬������Ҫ�ص���յ����������ϣ�����Ҫ�ɷ�Ϊ����ﮣ�LiCoO2����������Ȳ��(һ��̿�ڣ��������Լ��л�ճ�Ӽ���ij���չ����������£�
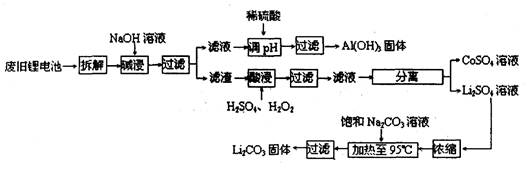
��1���������ջ��յ��IJ�����?
��2��Liԭ�ӵ�������������?���Ͼɵ�ؿ������ڷŵ粻��ȫ��������ԭ��̬��ﮣ�Ϊ�˰�ȫ�Բ�����Ҫ����___________________________________________
��3�����ʱ��Ҫ��Ӧ�Ļ�ѧ����ʽΪ?��
��4�����һ������Ӧ���ȹ��ˣ�ԭ����?
2��ʵ���� (16��)����TiO2��Ϳ�ϡ��������ױƷ���������ż���㷺��Ӧ�á�
��1���Ʊ�����TiO2�ķ���֮һ��TiCl4ˮ������TiO2��x H2O����ˮ�ⷴӦ�Ļ�ѧ����ʽΪ?���پ����ˡ�ˮϴ��ȥ���е�Cl�C���ٺ�ɡ����ճ�ȥˮ�ֵõ�����TiO2������TiO2��xH2O��Cl�C�Ƿ����ķ�����?��
��2����������ԭ�ζ����ⶨTiO2������������һ�������£���TiO2�ܽⲢ��ԭΪTi3+������KSCN��Һ��ָʾ������NH4Fe(SO4)2����Һ�ζ�Ti3+��ȫ������Ti4+��
��ش��������⣺
������NH4Fe(SO4)2����Һʱ������һ����H2SO4��ԭ����?��
�ڵζ��յ��������?��
�۵ζ�����ʱ����ȡTiO2��Ħ������ΪM g��mol��1������w g������c mol��L��1 NH4Fe(SO4)2����ҺV mL����TiO2������������ʽΪ?��
�����в�����TiO2���������ⶨ�����Ӱ�죨�ƫ�ߡ�����ƫ�͡�����Ӱ�족��
�������Ʊ���Һ�����У��ձ��е�NH4Fe(SO4)2��Һ������������ʹ�ⶨ���?��
���ڵζ��յ��ȡ�ζ��̶ܿ�ʱ�����ӱ�ҺҺ�棬ʹ�ⶨ���?��
3������� (1)���з�Ӧԭ�������Ϲ�ҵұ������ʵ���������(����)��
A��2HgO 2Hg+O2��
2Hg+O2��
B��Fe3O4+4CO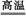 3Fe+4CO2
3Fe+4CO2
C��2MgO 2Mg+O2��
2Mg+O2��
D��2Ag2O 4Ag+O2��
4Ag+O2��