微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (14分)无水AlCl3易升华,可用作有机合成的催化剂等。工业 上由铝土矿(A12O3、Fe2O3)为原料制备无水AlCl3的工艺流程如下。
上由铝土矿(A12O3、Fe2O3)为原料制备无水AlCl3的工艺流程如下。
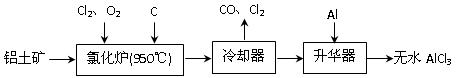
(1)氯化炉中Al2O3、C12和C反应的化学方程式为?▲?。
(2)用Na2SO3溶液可除去冷却器排出尾气中的Cl2,此反应的离子方程式为?▲ ?。
(3)升华器中主要含有AlCl3和FeCl3,需加入少量Al,其作用是?▲?。
(4)为测定制得的无水AlCl3产品(含杂质FeCl3) 的纯度,称取16.25 g无水AlCl3样品,溶于过量的NaOH溶液,过滤出沉淀物,沉淀物经洗涤、灼烧、冷却、称重,残留固体质量为0.32 g。
的纯度,称取16.25 g无水AlCl3样品,溶于过量的NaOH溶液,过滤出沉淀物,沉淀物经洗涤、灼烧、冷却、称重,残留固体质量为0.32 g。
①写出除杂过程中涉及的离子方程式? ▲?、? ▲?。
②AlCl3产品的纯度为?▲ ?。
(5)工业上另一种由铝灰为原料制备无水AlCl3工艺中,最后一步是由AlCl3・6H2O脱水制备无水AlCl3,实现这一步的方法是? ▲?。
2、填空题 使用某些有机物材料给环境造成“白色污染”,后果严重。最近研究的一些分解性塑料,有良好的生物适应性和分解性,能自然腐烂分解。如:
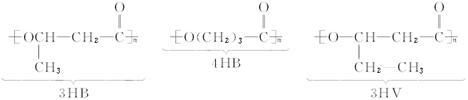
已知3HB的单体叫3羟基丁酸,则:
(1)4HB的名称是_______________,3HV的名称是_______________________。
(2)两分子4HB的单体脱水时,生成的环酯的结构简式为____________________。
3、填空题 磷酸亚铁锂LiFePO4是一种新型汽车锂离子电池的电极材料。某化工厂以铁红、锂辉石LiAl(SiO3)2(含少量Ca2+、Mg2+的盐)、碳粉等原料来生产磷酸亚铁锂。其主要工艺流程如下:
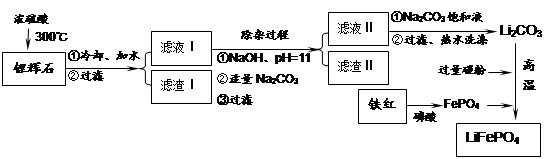
已知:2LiAl(SiO3)2 + H2SO4(浓) 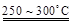 ?Li2SO4 + Al2O3・4SiO2・H2O↓
?Li2SO4 + Al2O3・4SiO2・H2O↓
温度/℃
| 20
| 40
| 60
| 80
|
溶解度(Li2CO3)/g
| 1.33
| 1.17
| 1.01
| 0.85
|
溶解度(Li2SO4)/g
| 34.2
| 32.8
| 31.9
| 30.7
|
?
(1)从滤渣Ⅰ中可分离出Al2O3,如下图所示。请写出生成沉淀的离子方程式?。
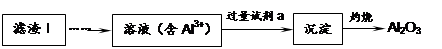
(2)滤渣Ⅱ的主要成分是:?(填化学式)。
(3)向滤液Ⅱ中加入饱和Na2CO3溶液,过滤后,用“热水洗涤”的原因是?
?。
(4)写出在高温下生成磷酸亚铁锂的化学方程式?。
(5)磷酸亚铁锂电池总反应为:FePO4+Li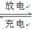 LiFePO4,电池中的固体电解质可传导Li+。试写出该电池放电时的正极反应:?。若用该电池电解饱和食盐水(电解池电极均为惰性电极),当电解池两极共有4480mL气体(标准状况)产生时,该电池消耗锂的质量为?。
LiFePO4,电池中的固体电解质可传导Li+。试写出该电池放电时的正极反应:?。若用该电池电解饱和食盐水(电解池电极均为惰性电极),当电解池两极共有4480mL气体(标准状况)产生时,该电池消耗锂的质量为?。
4、选择题 在炼铁、制玻璃、制水泥三种工业生产中,都需要的原料是( )
A.纯碱
B.石灰石
C.石英
D.粘土
5、填空题 (16分)NiSO4・6H2O是一种绿色易溶于水的晶体,广泛用于化学镀镍、生产电池等,可由电镀废渣(除含镍外,还含有:Cu、Zn、Fe、Cr等杂质)为原料获得。操作步骤如下:
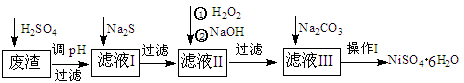
(1)加Na2S的目的是除去铜、锌等杂质,请写出除去Cu2+的离子方程式__________ __________
(2) 加6%的H2O2时,温度不能过高,其目的是: _____? ________?。
(3) 除铁方法:用H2O2充分氧化后,再用NaOH控制pH值2~4范围内生成氢氧化铁沉淀。在上述方法中,氧化剂可用NaClO3代替,请写出用氯酸钠氧化Fe2+的离子方程式为:______________________________________________________
(4)上述流程中滤液Ⅲ的主要成分是: ? 。
(5)操作Ⅰ包括以下过程:过滤,用?(填试剂化学式)溶解,蒸发浓缩,冷却结晶,洗涤获得产品。