��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ��Դ��Ӱ��ȫ�ú��������Ҫ���ء�Ŀǰ�����ѿ��������õ���Դ�У�������������������Դ֮һ����֪��Ӧ��2H2��O2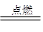 2H2O���Իش��������⡣
2H2O���Իش��������⡣
(1)�÷�ӦΪ ��Ӧ������ȡ����ȡ�����
(2) 1������8g H2Oʱ��H2O�����ʵ����� ������ĸ���ţ���
A��1mol B��1mol/L C��1g/mol
�ο��𰸣�(1)���� (2)A
���������(1)����ȼ���Ƿ��ȷ�Ӧ�����Ը÷�ӦΪ���ȷ�Ӧ��
(2) 1������8g H2Oʱ��H2O�����ʵ���Ϊ1mol,��ѡA
�����Ѷȣ�һ��
2��ѡ���� �����£���0.100 mol/L NaOH ��Һ�ֱ�ζ�20.00 mL 0.100 mol/L������ʹ��ᣬ�ζ���������ͼ��ʾ������˵����ȷ���ǣ�?��
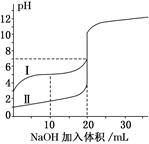
A����ֱ��ʾ����ʹ���ĵζ�����
B��V(NaOH)��10.00 mL ʱ��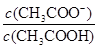 ��1
��1
C��pH��7ʱ������������NaOH��Һ��������
D��V(NaOH)��20 .00 mL ʱ��c(Cl��)��c(CH3COO��)
�ο��𰸣�B
���������������������ʣ�0.100 mol/L������ʹ��ᣬ���ߵ�pH�����������ж�A����ȷ��V(NaOH)��10.00 mL ʱ����Һ�е�����CH3COOH��CH3COONa��������ˮ��͵���ʱ�����ߵ����ʵ�����Ϊ1��1����ͬ�¶Ⱥ�Ũ��ʱ��CH3COOH�ĵ������CH3COO����ˮ�⣬B��ȷ��pH��7ʱ����������NaOH��Һ�������C����ȷ��V(NaOH)��20 .00 mL ʱ������Һ�е����ʷֱ���NaCl��CH3COONa���Ҷ��ߵ����ʵ�����ȣ�����CH3COO��ˮ�⣬��c(Cl��)��c(CH3COO��)��D����ȷ��
�����Ѷȣ�һ��
3������� ��10�֣�ij�¶�(t��)ʱ��ˮ�����ӻ�ΪKW��1��10-13������¶�(����ڡ�����С�ڡ����ڡ�)________25�档�������¶���pH��11�Ŀ�������Һa L��pH��1��ϡ����b L���(���Ϻ���Һ�����С�仯���Բ���)����ͨ��������д���²�ͬ���ʱ������Һ������ȣ�
�������û��ҺΪ���ԣ���a��b��________������Һ�и������ӵ�Ũ���ɴ�С����˳����________________?��
�������û��Һ��pH��2����a��b��________������Һ�и������ӵ�Ũ���ɴ�С����˳����_______?_��
�ο��𰸣�
���ڣ���10:1��c(Na+)>c(SO42-)>c(H+)=c(OH-)����9:2��c(H+)> c(SO42-) > c(Na+) > c(OH-)
�����������
�����Ѷȣ�һ��
4�������� ��8�֣�ij�¶ȣ�t�棩ʱ��ˮ��KW=10-13������¶ȣ�����ڡ����ڻ�С�ڣ�
��1��_____25�棬������_________________________________________________�������¶���pH=11��NaOH��ҺaL��pH=1��H2SO4��ҺbL��ϣ�
��2�������û����ҺΪ���ԣ���a��b=_________��
��3�������û����ҺpH=2����a��b=__________��
�ο��𰸣���1�����ڣ�ˮ�ĵ������ȣ������¶ȣ��ٽ�ˮ�ĵ��룬KW����
��2��10��1?��3��2��9
�����������1��25��ʱˮ�����ӻ�������10��14�����ˮ��KW=10-13�����¶�һ������25��.��Ϊ���������ȵģ����Լ��ȴٽ�ˮ�ĵ��룬���ӻ���������
��2�����¶���pH=11��NaOH��Һ��Ũ����0.01mol/L�����û����ҺΪ���ԣ�˵�������ӵ����ʵ�����OH�����ʵ�����ȣ���a��10��2��b��10��1�����a�Ub��10�U1��
��3�����û����ҺpH=2��˵�������ǹ����ģ����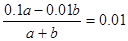 �����a�Ub��2�U9��
�����a�Ub��2�U9��
�����Ѷȣ�һ��
5������� (12��)���¶�T ���£�ijBa(OH)2ϡ��Һ��c(H��)��10��amol/L��c(OH��)��10��bmol/L����֪a��b��12�������Һ����μ���pH��b�����ᣬ��û����Һ�IJ���pH���±���ʾ��
���
| �������������/mL
| ��������/mL
| ��Һ��pH
|
��
| 22.00
| 0.00
| 8
|
��
| 22.00
| 18.00
| 7
|
��
| 22.00
| 22.00
| 6
|
(1)���������жϣ�T ��________25 ��(����ڡ�����С�ڡ����ڡ�)�����¶���ˮ�����ӻ�KW��________��
(2)b��________��ԭBa(OH)2ϡ��Һ�����ʵ���Ũ��Ϊ________��
(3)���¶��£���1 L�����������ƵĻ����Һ�м���3 L��Ba(OH)2��ϡ��Һʱ���������ô����ֵ����������Һ��ȡ��4 mL����ˮϡ����20 mL�������Һ��pHΪ7����ԭ�����������ƻ����Һ��pHΪ________������Na2SO4�����ʵ���Ũ��Ϊ________��
�ο��𰸣�(12��)(ÿ��2��)��(1)���ڡ�1��10��12��? 2)4��5��10��5mol/L? (3)4��1��10��4mol/L
�����������1��Kw=c(H+)c(OH-)=10-a��10-b=10-(a+b)=10-12�����¶ȴ���25�棻
��2��pH=8��c(OH-)==10-4mol/L��������������Ũ��Ϊ5��10-5mol/L��
��3��pH=7���ڸ��¶�����Һ�ʼ��ԣ�c��4ml=10-5��20ml��c=5��10-5mol/L������Ϊc=��c(H+)=10-4mol/L��pH=4��
�����Ѷȣ�һ��