��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ��ش��������⣺
��1���ִ���ҵ��ú̿�������ȿ������ȼ�ϵ������ʡ�����CO��SO2�ȵ��ŷţ��ֿ�������ˮú���Ĺ㷺��;��
����֪��2C��s��+O2��g��=2CO��g������H1��2H2��g��+O2��g��=2H2O��g������H2��
��ӦC��s��+H2O��g��?CO��g��+H2��g������H=______�����ú���H1����H2�Ĵ���ʽ��ʾ��
��CO��H2��һ�������ºϳɼ״��ķ�ӦΪ��CO��g��+2H2��g��?CH3OH��g������H3�������ݻ���Ϊ1L��a��b��c��d��e����ܱ������зֱ����1mol?CO��2mol?H2�Ļ�����壬���£�����ʵ�飬��������������ͼ1��ͼ2��
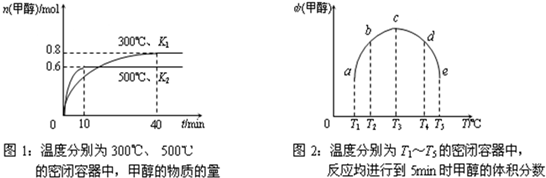
a���÷�Ӧ�ġ�H3______0��ѡ���������������=������ͬ����K1______K2��
b��������d�е�ƽ��״̬ת�䵽����c�е�ƽ��״̬���ɲ�ȡ�Ĵ�ʩ��______��
��2��ijȼ�ϵ��������̬K2CO3Ϊ����ʣ�һ��ͨ��CO����һ��ͨ�������CO2�Ļ�����壮��֪��ȼ�ϵ��������ӦΪ2CO2+O2+4e-=2CO32-�����为���ĵ缫��ӦʽΪ______��
��3��ͼ3Ϊij�¶��£�Fe��OH��3��s����Mg��OH��2��s���ֱ�����Һ�дﵽ�����ܽ�ƽ��ı���Һ��pH������������Ũ�ȱ仯�������ͼ������
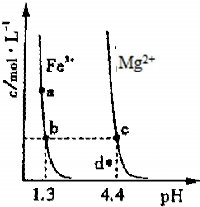
���¶��£��ܶȻ������Ĺ�ϵΪ��Ksp[Fe��OH��3]______Ksp[Mg��OH��2]
�������=������������������ɵ�Mg��OH��2��Һ�е���������Fe3+����ɫ������ȫ��ת��Ϊ���ɫ������ԭ����
______��
2��ѡ���� ��֪��Ӧ��
H2��g����?1/2O2��g����H2O��g��?��H1 ?
1/2N2��g����O2��g����NO2��g��?��H2? ?
1/2N2��g����3/2H2��g����NH3��g��?��H3?
��Ӧ2NH3��g����?O2��g����2NO2��g����3H2O��g���ġ�HΪ
[? ]
A.?2��H1��2��H2��2��H3?
B.?��H1����H2����H3
C.?3��H1��2��H2��2��H3?
D.?3��H1��2��H2��2��H3
3������� ��ú��Ϊȼ�Ͽ�ͨ����������;����
;��I��úֱ��ȼ��C��s��+O2?��g���TCO2��g����H1��0?��
;��II�����Ƴ�ˮú����C��s��+H2O��g���TCO��g��+H2��g����H2��0?��
��ȼ��ˮú����2CO��g��+O2��g���T2CO2��g����H3��0?��
2H2��g��+O2?��g���T2H2O��g����H4��0?��
��ش��������⣺
��1��ȼ�յ�����ú��;��I�ų�������______������ڡ������ڡ���С�ڡ���;��II�ų���������������������______��
��2����H1����H2����H3����H4����ѧ��ϵʽ��______��
4������� ��֪�����Ȼ�ѧ����ʽ��
��H2(g)��1/2O2(g)��H2O(l)����H����285.8 kJ��mol-1
��H2(g)��1/2O2(g)��H2O(g)����H����241.8 kJ��mol-1
��C(s)��1/2O2(g)��CO(g)����H����110.5 kJ��mol-1
��C(s)��O2(g)��CO2(g)����H����393.5 kJ��mol-1
�ش��������⣺
��1��������Ӧ�����ڷ��ȷ�Ӧ����____________��
��2��H2��ȼ����Ϊ____________��C��ȼ����Ϊ____________��
��3��ȼ��10g H2����Һ̬ˮ���ų�������Ϊ____________��
��4��д��COȼ�յ��Ȼ�ѧ����ʽ__________________________________��
5�������&nb sp; ��1����֪���淴Ӧ��M��g��+N��g��?P��g��+Q��g������H��0����ش��������⣮
����Ҫ����M��ת���ʣ��������������������¿��Բ�ȡ�Ĵ�ʩΪ______������ţ���
A������һ����M?B�����ͷ�Ӧ�¶�?C�����߷�Ӧ�¶�
D����С�������?E���������?F�������һ����P
����ij�¶�����ʼ��Ӧ���Ũ�ȷֱ�Ϊ��c��M��=1mol?L-1��c��N��=2.4mol?L-1���ﵽƽ���M��ת����Ϊ60%����ʱN��ת����Ϊ______���������¶Ȳ��䣬��ʼ��Ӧ���Ũ�ȸ�Ϊ��c��M��=4mol?L-1��c��N��=a?mol?L-1���ﵽƽ���c��P��=2mol?L-1����a=______mol?L-1��
��2����˹�����������Ϳ�ѧ�о����к���Ҫ�����壮�Ը�������3���Ȼ�ѧ��Ӧ����ʽ��
��Fe2O3��s��+3CO��g��=2Fe��s��+3CO2��g����H=-24.8kJ?mol-1
��3Fe2O3��s��+CO��g��=2Fe3O4��s��+CO2��g����H=-47.2kJ?mol-1
��Fe3O4��s��+CO��g��=3FeO��s��+CO2��g����H=+640.5kJ?mol-1
д��CO���廹ԭFeO����õ�Fe?�����CO2������Ȼ�ѧ��Ӧ����ʽ��______��
��3��һ���¶��£���Na2CO3��Һ�м���BaCl2��K2SO4�������ֳ�������ʱ��c��CO32-����c��SO42-��=______��
[��֪Ksp��Ba?SO4��=1.3��10-10��Ksp��BaCO3��=2.6��10-9]��