|
高考化学知识点总结《电解池原理》高频考点特训(2017年练习版)(二)
2017-07-27 11:17:12
来源:91考试网
作者:www.91exam.org 【 大 中 小】
|
微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 如图装置电解一段时间,当某极析出0.32gCu时,I、Ⅱ、Ⅲ中溶液pH分别为(溶液足量,体积均为100mL且电解前后溶液体积变化及气体的溶解忽略不计)
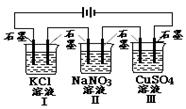
A.13、7、1
B.12、7、2
C.1、7、13
D.7、13、1
|
参考答案:A
本题解析:Ⅲ中阴极析出单质铜,Cu2++2e=Cu,0.32gCu的物质的量为0.005mol,该电极放电0.01mol,I中用惰性电极电解KCl溶液,电解总反应为2KCl+2H2O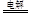 2KOH+H2↑+Cl2↑转移电子2e-,生成KOH 0.01mol,c(OH-)=0.01mol/0.1L=0.1mol/L,溶液的PH=13,Ⅱ中NaNO3溶液属于强酸强碱盐,溶液的PH=7,Ⅲ中用惰性电极电解CuSO4溶液,电解总反应为2CuSO4 +2H2O 2KOH+H2↑+Cl2↑转移电子2e-,生成KOH 0.01mol,c(OH-)=0.01mol/0.1L=0.1mol/L,溶液的PH=13,Ⅱ中NaNO3溶液属于强酸强碱盐,溶液的PH=7,Ⅲ中用惰性电极电解CuSO4溶液,电解总反应为2CuSO4 +2H2O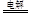 2Cu+2H2SO4 +O2↑,转移电子4e-,生成H2SO4 0.005mol,c(H+)=0.01mol/0.1L=0.1mol/L,溶液的PH=1,选A。 2Cu+2H2SO4 +O2↑,转移电子4e-,生成H2SO4 0.005mol,c(H+)=0.01mol/0.1L=0.1mol/L,溶液的PH=1,选A。
考点:考查电解的工作原理及PH值的计算。
本题难度:一般
2、填空题 工业上利用铬铁矿(FeO Cr2O3)冶炼铬的工艺流程如下: Cr2O3)冶炼铬的工艺流程如下:
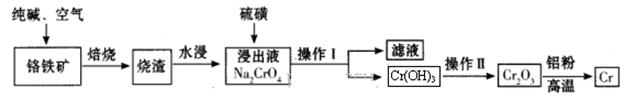
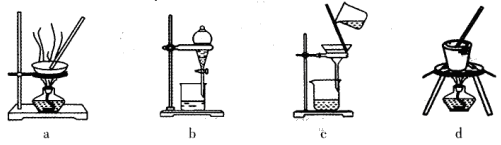
(1)实验室焙烧铬铁矿可选用的装置是__________(填序号)。
(2)完成下列化学方程式(在横线上填写物质的化学式及计量数):4CrO42-+6S+7H2O=4Cr(OH)3↓+3S2O32-+_____________。
(3)操作I包括过滤与洗涤,简述实验室中洗涤沉淀的操作:__________________。
(4)Cr(OH)3和Al(OH)3类似,也是两性氢氧化物,写出Cr(OH)3溶于浓氢氧化钠溶液的离子方程式________________________________。
(5)由Cr2O3冶炼Cr的化学方程式为____________________________。
(6)目前有一种采用以铬酸钠(Na2CrO4)为原料,用电化学法制备重铬酸钠(Na2Cr2O7)的实验装置如下图所示(已知:2CrO42-+2H+ Cr2O72-+H2O)。 Cr2O72-+H2O)。

①写出阴极的电极反应式为________________________________________。
②电解一段时间后,测得阳极区溶液中Na+物质的量由a mol变为b mol,则此时铬酸钠的转化率为___。
参考答案:(1)d (2分,大写字母不得分)?(2)2OH- (2分,计量数写错、化学式写错均不得分)
(3)将蒸馏水沿玻璃棒慢慢倒入漏斗中浸没沉淀(1分),待水流尽后,再重复操作2~3次(1分)? (共2分,合理答案即可)
(4)Cr(OH)3 + OH- = CrO2- + 2H2O (2分,化学式写错、不配平均不得分,写化学方程式不得分)
(5)Cr2O3 + 2Al 2Cr + Al2O3?(2分,不写反应条件不扣分,化学式写错、不配平不得分) 2Cr + Al2O3?(2分,不写反应条件不扣分,化学式写错、不配平不得分)
(6)①2H+ + 2e- = H2↑(或2H2O+2e-=2OH-+H2↑)(2分,化学式写错、不配平均不得分)(2分)
②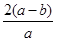 ×100% (2分,合理答案即可) ×100% (2分,合理答案即可)
本题解析:(1)固体灼烧需要在巩固中完成,根据装置图可知,a、b、c分别是蒸发、分液与过滤,d装置是坩埚,因此实验室焙烧铬铁矿可选用的装置是d。
(2)根据电荷守恒可知,该生成物是带负电荷的。根据原子守恒可知,该微粒石油氢原子和氧原子组成的,所以应该是OH-,计量数是2。
(3)过滤后得到的沉淀必须在过滤器中完成,所以实验室中洗涤沉淀的操作将蒸馏水沿玻璃棒慢慢倒入漏斗中浸没沉淀,待水流尽后,再重复操作2~3次;
(4)Cr(OH)3和Al(OH)3类似,也是两性氢氧化物。氢氧化铝与氢氧化钠溶液反应生成偏铝酸钠和水,因此Cr(OH)3溶于浓氢氧化钠溶液反应生成的是NaCrO2和水,反应的离子方程式为Cr(OH)3 + OH- = CrO2- + 2H2O。
(5)Cr的冶炼一般是通过铝热反应,所以由Cr2O3冶炼Cr的化学方程式为Cr2O3 + 2Al 2Cr + Al2O3。 2Cr + Al2O3。
(6)①电解池中阴极得到电子,发生还原反应。所以惰性电极电解铬酸钠溶液时阴极是溶液中的氢离子放电,反应的电极反应式为2H+ + 2e- = H2↑。
②电解一段时间后,测得阳极区溶液中Na+物质的量由a mol变为b mol。所以根据电荷守恒可知,阴极区生成氢氧化钠的物质的量是(a-b)mol,属于消耗氢离子的物质的量是(a-b)mol,所以根据方程式2CrO42-+2H+ Cr2O72-+H2O可知,消耗铬酸钠的物质的量是(a-b)mol。反应前铬酸钠的物质的量是0.5amol,所以铬酸钠的转化率是 Cr2O72-+H2O可知,消耗铬酸钠的物质的量是(a-b)mol。反应前铬酸钠的物质的量是0.5amol,所以铬酸钠的转化率是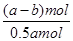 ×100%= ×100%=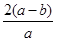 ×100%。 ×100%。
本题难度:困难
3、选择题 Li~SO2电池具有输出功率高且低温性能好的特点,其电解质为LiBr,溶剂是碳酸丙烯酯和乙腈,Li+可在其中移动。电池总反应式为:2Li +2SO2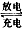 Li2S2O4。下列有关电池的说法正确的是 Li2S2O4。下列有关电池的说法正确的是
[? ]
A.该电池总反应为可逆反应
B.充电时阴极反应式为:Li+ +e-=Li
C.放电时Li+向负极移动
D.该电池电解质溶液可换成LiBr水溶液
参考答案:B
本题解析:
本题难度:一般
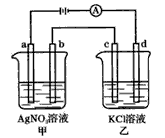
4、选择题 如图所示,a.b、c均为石墨电极,d为碳钢电极,通电进行电解。假设在电解过程中产生的气体全部逸出,下列说法正确的是
[? ]
A.甲烧杯中溶液的pH降低
B.乙烧杯中的d电极反应式为Fe-2e-=Fe2+
C.当电解一段时间后,将甲、乙两溶液混合,一定会产生沉淀
D.当b极增重5. 4g时,d极产生的气体为2.24L(标准状况)
参考答案:A
本题解析:
本题难度:一般
5、选择题 有关下图的说法正确的是
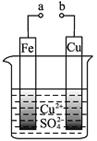
A.构成原电池时Cu极反应为: Cu
|