��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ����ˮ����ȡ�壬���з����������˵���
A������
B������
C����ȡ
D���ᾧ
�ο��𰸣�C
������������������л��ܼ����ܽ�Ƚϴɲ�ȡ��ȡ�ķ�������ˮ����ȡ
�����Ѷȣ���
2������� ��һ��������X�����ܺ����Ȼ��ơ�̼��ء��������ơ�����������ʽ̼��þ��̼�����Ƶ����ʡ�Ϊ̽��X�ijɷ֣���Ʒ���������������ʵ�飺
I����X��ĩ��ּ��ȣ������������
��ȡһ����X��ĩ����������������ˮ����ĩȫ���ܽ⣬ �õ���ɫ��Һ��
�õ���ɫ��Һ��
���ò�˿պȡ��������������Һ���ڻ��������գ�������ɫ���棻����ɫ�ܲ����۲죬����ɫ���档
��.ȡ������ɫ��Һ������KMnO4������Һ���Ϻ�ɫ����ȥ��
V��ȡ������Һ���ö��Ե缫��⣬��ʼʱ����������������ʹ
ʪ��ĵ��۵⻯����ֽ����ɫ���������в����ҺpH�仯��
��ͼ��ʾ��
��1������ʵ������жϣ�һ�������ڵ�������_________?��
��2��X�ijɷ���_________ ?���ѧʽ����
��3��ʵ��V�У�0~tʱ���ڣ������ĵ缫��ӦʽΪ��_________����ܷ�Ӧ�����ӷ���ʽ_________?
��4��0��t1ʱ���ڣ���ҺpH���߱Ƚϻ�����ԭ���ǣ�_________?���û�ѧ����ʽ��ʾ����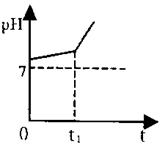
�ο��𰸣�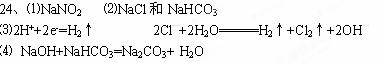
�����������
�����Ѷȣ�һ��
3��ʵ���� ��̼����(2Na2CO4��3H2O)��һ������Ч����Ư��ɱ������������������������Ⱦ���ص㣬������Ӧ����ϴ�ӡ�ӡȾ����֯����ֽ��ҽҩ�����������С����д���Ʊ���̼���ƿɽ��������ɱ����������������£�
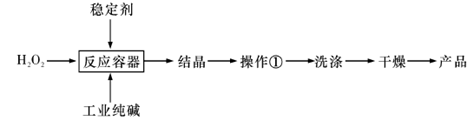
�Իش��������⣺
��1����̼��������ˮ��������Һ��?(����ԡ��������ԡ������ԡ�)���������ӷ���ʽ��ʾ��______________________��
��2����������Ҫ�IJ���������?(��д��������)��
��3����ҵ�����г���������NaCl��ijУ��ѧ����С�������ͼ��ʾװ�ã��ⶨ��ҵ�� ����Na2CO3�ĺ�����
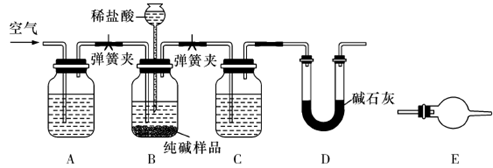
��Ҫ���鹤ҵ���������ʵĴ��ڣ����ѡ�������Լ��е�__________(ѡ�����)��
a. ����������Һ?b. ϡ����? c. ���軯����Һ?d. ��������Һ
�ڼ���װ��B�����Եķ����ǣ�����������©���������������н����ɼк�©��ע��һ������ˮ��ʹ©���ڵ�ˮ�����ƿ�ڵ�ˮ�棬ֹͣ��ˮ�����۲쵽?˵��װ�ò�©����
��װ��A��������?��װ��C�е��Լ�Ϊ?��
��ijͬѧ��Ϊ��Dװ�ú�Ӧ������Eװ��(װ���ʵ��Լ�)������Ϊ�Ƿ��Ҫ??(ѡ���Ҫ������Ҫ��)���жϵ�������?��
�ο��𰸣���1�� ����(1��)? CO42�C + H2O  ?HCO4�C + OH�C
?HCO4�C + OH�C
��2��©��(1��)?�ձ�(1��)?������(1��)
��3�� ��bd?��©���ڵ�ˮ�����ƿ�ڵ�ˮ�棬�ұ���һ��ʱ�䲻��?�����տ����е�CO2��������ţ�������װ��������������?Ũ����(1��)?�ܱ�Ҫ(1��)?��������е�CO2����Dװ�ã����ʵ���ȷ��
�����������1����̼���ƴ�������ϴ�ӣ����Ʋ����Լ��ԣ���Ϊ��̼�������ˮ��ʼ��ԣ�CO42�C + H2O  ?HCO4�C + OH�C����2������Һ�з�������壬��ʵ����Ӧ���ù��˵ķ��������˲�����Ҫ�IJ�������©�����ձ�������������3���ټ��鴿�����Ƿ�����NaCl���ʣ�Ӧ�ȼ���AgNO3��Һ���ټ��������ϡHNO3�������а�ɫ��Һ��˵����Һ�к���Cl�C����ѡbd����©���ڵ�ˮ�����ƿ�ڵ�ˮ�棬�ұ���һ��ʱ�䲻�䣬��˵��װ�ò�©�����۱�ʵ�����ԭ��Ϊͨ���ⶨ���ɵ�CO2������ȷ��������Na2CO3�ĺ���������Bװ��������������Ӧ�ܱ�Dװ���еļ�ʯ�ҳ�����գ����Aװ�õ�Ŀ�ľ���ͨ�������������Bװ�������������壬���ֲ����ÿ����е�CO2Ӱ��ⶨ��������Aװ������ʢ��Һ�����ܳ�ȥ�����е�CO2�����Cװ�õ�Ŀ���dz�ȥCO2�л�ϵ�ˮ��������װ��A�������ǣ����տ����е�CO2��������װ�������������壬װ��C�е��Լ�Ϊ��Ũ����ܶ���ʵ��Ӧ������ȷ����С��ʵ������Ҫ��������ʵ��ǰ��Dװ�õ���������������е�CO2����Dװ�û����ʵ����Ӱ��ʵ��ľ�ȷ�ȣ�����Dװ�ú��������һ��Eװ�á�
?HCO4�C + OH�C����2������Һ�з�������壬��ʵ����Ӧ���ù��˵ķ��������˲�����Ҫ�IJ�������©�����ձ�������������3���ټ��鴿�����Ƿ�����NaCl���ʣ�Ӧ�ȼ���AgNO3��Һ���ټ��������ϡHNO3�������а�ɫ��Һ��˵����Һ�к���Cl�C����ѡbd����©���ڵ�ˮ�����ƿ�ڵ�ˮ�棬�ұ���һ��ʱ�䲻�䣬��˵��װ�ò�©�����۱�ʵ�����ԭ��Ϊͨ���ⶨ���ɵ�CO2������ȷ��������Na2CO3�ĺ���������Bװ��������������Ӧ�ܱ�Dװ���еļ�ʯ�ҳ�����գ����Aװ�õ�Ŀ�ľ���ͨ�������������Bװ�������������壬���ֲ����ÿ����е�CO2Ӱ��ⶨ��������Aװ������ʢ��Һ�����ܳ�ȥ�����е�CO2�����Cװ�õ�Ŀ���dz�ȥCO2�л�ϵ�ˮ��������װ��A�������ǣ����տ����е�CO2��������װ�������������壬װ��C�е��Լ�Ϊ��Ũ����ܶ���ʵ��Ӧ������ȷ����С��ʵ������Ҫ��������ʵ��ǰ��Dװ�õ���������������е�CO2����Dװ�û����ʵ����Ӱ��ʵ��ľ�ȷ�ȣ�����Dװ�ú��������һ��Eװ�á�
�����Ѷȣ�����
4��ѡ���� ���и��������У����÷�Һ©�����з������
A������CCl4
B�����CCl4
C���ƾ���ˮ
D�����ͺ�ˮ
�ο��𰸣�D
���������A���������Ȼ�̼���ܣ������÷�Һ©�����з��룬A����ȷ��B���嵥���������л��ܼ��У������÷�Һ©�����з��룻C���ƾ���ˮ���ܣ������÷�Һ©�����з��룻D�����Ͳ�����ˮ����ˮ���ϲ㣬�����÷�Һ©�����з��룬D��ȷ����ѡD��
�����Ѷȣ���
5������� ������ͼװ�ã�д����ȥ���������е����ʵķ�������д����ѧ����ʽ�������ڵ�����Ϊ���ʣ���
(1) CO2(SO2)___________����ѧ����ʽ___________________��
(2) SO2(SO3������SO3Ϊ����)______________����ѧ����ʽ__________________��
�ο��𰸣�(1)���������ͨ�뵽����NaHCO3��Һ�У�SO2+2NaHCO3 = 2CO2��+Na2SO3+H2O
(2)���������ͨ�˵�ʢ�б���NaHSO3��Һ�У�SO3+2NaHSO3 = 2SO2��+Na2SO4+H2O
���������
�����Ѷȣ�һ��