微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、推断题 A-G及X、Y均是中学化学常见物质,其中B、D、E、F、G在常温下为气体且B为红棕色,C是红色的金属单质。它们之间有如下转化关系(其中反应③④⑦的产物中的水已略去)。
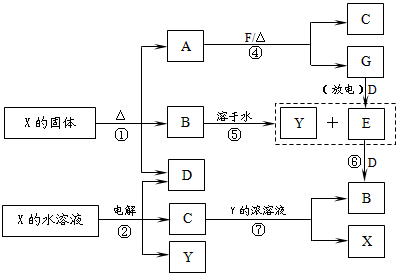
试填空
(1)写出G分子的电子式____________。
(2)写出反应⑦的离子方程式_____________________。
(3)写出电解X溶液的阳极反应式______________________。
(4)写出反应④的化学方程式______________________。
(5)若使F按下列途径完全转化为Y。

则参加反应的F与整个过程中消耗D的物质的量之比为:___________。
参考答案:(1) (2)Cu+4H++2NO3-=Cu2++2NO2↑+2H2O
(2)Cu+4H++2NO3-=Cu2++2NO2↑+2H2O
(3)4OH--4e-=O2↑+2H2O (或2H2O-4e- =O2↑+2H+ )
(4)2NH3+3CuO N2+3Cu+3H2O
N2+3Cu+3H2O
(5)1:2
本题解析:
本题难度:一般
2、推断题 A、B、C、D是按原子序数由小到大排列的第二、三周期元素的单质。B、E均为组成空气的成分。F的焰色反应呈黄色。在G中,非金属元素与金属元素的原子个数比为1:2。在一定条件下,各物质之间的相互转化关系如图(图中部分产物未列出)

请填写下列空白
(1)A是___________,F的电子式是___________。
(2)H与盐酸反应生成E的化学方程式是______________________。
(3)E与F反应的化学方程式是______________________。
(4)F与G的水溶液反应生成I和D的离子方程式是______________________。
参考答案:(1)碳(或C);
(2)Na2CO3+2HCl=2NaCl+H2O+CO2↑
(3)2CO2+2Na2O2=2Na2CO3+O2
(4)Na2O2+S2-+2H2O=4OH-+S↓+2Na+
本题解析:
本题难度:一般
3、简答题 已知A、B、C、D、E、F、G、H、I九种物质,A、B、D、E焰色反应均为紫色(透过蓝色钴玻璃),G是一种单质,I是一种化合物,H是一种淡黄色固体,它们的转化关系如图所示.请回答下列问题:
(1)B、D、I的化学式是B______?D______?I______
(2)写出H的一种用途______
(3)写出A受热分解的化学方程式______
(4)若H与C反应固体增重4.2g,则参加反应的C气体在标准状况下的体积为______?L.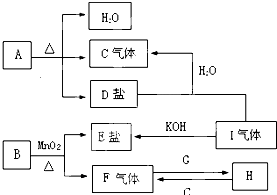
参考答案:A、B、D、E焰色反应均为紫色,说明都含有K元素,其中B能与二氧化锰在加热条件下反应生成气体F,应为KClO3的分解反应,则B为KClO3,E为KCl,F为O2,H是一种淡黄色固体,应为Na2O2,则G为Na,C为气体,能与过氧化钠反应生成氧气,则应为CO2,则A为KHCO3,D为K2CO3,I应为HCl,则
(1)由以上分析可知B为KClO3,D为K2CO3,I为HCl,故答案为:KClO3;K2CO3;HCl;
(2)H为Na2O2,可与水或二氧化碳反应生成氧气,可用于呼吸面具中和潜水艇里作为氧气的来源,具有氧化性,可用于漂白织物,
故答案为:可用于呼吸面具中和潜水艇里作为氧气的来源(或用于漂白织物等);
(3)KHCO3分解生成K2CO3、H2O和CO2,反应的方程式为2KHCO3?△?.?K2CO3+H2O+CO2↑,
故答案为:2KHCO3?△?.?K2CO3+H2O+CO2↑;
(4)根据反应的方程式计算:2Na2O2+2CO2=2Na2CO3+O2↑△m
? 156g?44.8L?212g? 56g
?V? 4.2g
则V=44.8L×4.2g56g=3.36L,
故答案为:3.36.
本题解析:
本题难度:一般
4、填空题 (13分).下图每一方框中的字母代表一种反应物或生成物:
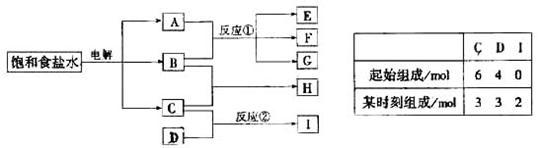
物质A跟B反应生成物质E、F和G;物质C跟D反应生成气体I,I中含有植物生长必须的元素之一,请填写下列空白:
(1)物质H的分子式是___________,气体I的分子式是____________
(2)写出电解饱和食盐水的化学方程式,并标出电子转移的方向和数目。
___________________________________________该反应中的 还原剂是___________
还原剂是___________
(3)反应①的化学方程式是_________________________________________。
参考答案:(1)HCl、NH3(2)?、NaCl(3)Cl2+2 NaOH =" NaCl+NaClO+" H2O。
本题解析:略
本题难度:一般
5、简答题 如图所示反应Ⅰ、反应Ⅱ和反应Ⅲ均是工业生产中常见的反应.其中A、B为化合物,C是温室气体之一,D和K均可用做干燥剂,H常温下为液态化合物,J是一种具有漂白作用的盐,反应Ⅲ和E与G反应的原理相同.
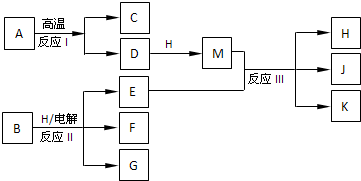
(1)C与J的水溶液反应后生成的含氧酸的电子式是______.
(2)E与G反应的离子方程式是______.
(3)J久置后,即便不接触水、空气,本身也逐渐分解生成K,并放出气体,该反应的化学方程式是______.
(4)工业上测定反应III产品的有效成分J的含量,先将一定量的产品的溶液加入过量的KI溶液和稀硫酸中,使之反应生成I2,然后用Na2S2O3标准溶液滴定I2,计算出结果.
①用Na2S2O3标准溶液滴定I2时选用的指示剂是______.
②生成I2的反应的离子方程式是______.
参考答案:反应I、反应II和反应III均是工业生产中常见的反应,A、B为化合物,C是温室气体之一为CO2,D和K均可用做干燥剂结合反应条件判断为D为CaO,A为CaCO3,H常温下为液态化合物推断为H2O,M为Ca(OH)2,J是一种具有漂白作用的盐推断为Ca(ClO)2,K为CaCl2,E为Cl2,反应III和E与G反应的原理相同,说明G为碱,结合反应条件,可以推断B为NaCl,电解溶液反应生成产物G为NaOH,F为H2;
(1)C(CO2)与J(Ca(ClO)2)的水溶液反应生成碳酸钙和含氧酸次氯酸,次氯酸的电子式是:
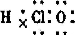
;故答案为:
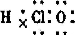
;
(2)E(Cl2)与G(Ca(OH)2)反应的离子方程式:Cl2+2OH-=Cl-+ClO-+H2O,故答案为:Cl2+2OH-=Cl-+ClO-+H2O;
(3)J(Ca(ClO)2)久置后,即便不接触水、空气,本身也逐渐分解生成K(CaCl2),并放出气体氧气,该反应的化学方程式:Ca(ClO)2=CaCl2+O2↑,故答案为:Ca(ClO)2=CaCl2+O2↑;
(4)①用Na2S2O3标准溶液滴定I2时选用的指示剂淀粉,随着Na2S2O3标准溶液的滴入,蓝色褪去;
②生成I2的反应的离子方程式为:ClO-+2I-+2H+=Cl-+I2+H2O;
故答案为:淀粉溶液;ClO-+2I-+2H+=Cl-+I2+H2O.
本题解析:
本题难度:一般