微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 现有下列几种常见的物质:
①N2 ②NaCl ③Ca(OH)2 ④金刚石⑤SiC ⑥NH3 ⑦NH4Cl ⑧CO2。其中,(以下空格均填写序号)
(1)含有非极性键的分子晶体是__________;
(2)含有极性键的分子晶体是__________;
(3)只含离子键的离子晶体是__________;
(4)含有极性共价键的原子晶体是__________;
(5)既含有离子键,又含有极性共价键和配位键的离子晶体是____________________。
参考答案:(1)①
(2)⑥⑧
(3)②
(4)⑤
(5)⑦
本题解析:
本题难度:一般
2、选择题 下列各组物质的性质判断不正确的是( )
A.键角:H2O>NH3
B.共价键极性:HF>H2O
C.碳碳键的键能:苯>CH3CH3
D.碳碳键的键长:CH2=CH2>CH≡CH
参考答案:A.H2O中O-H之间的夹角为104.4℃;NH3分子为三角锥形分子,是极性分子,键角是107°18′,故A错误;
B.成键的两原子电负性差别越大,极性越大,F的电负性最大,则跟氢原子形成最强极性键,故B正确;
C.键长越短键能越大,碳碳键的键能:苯>CH3CH3,故C正确;
D.碳碳键的键长:CH2=CH2<CH≡CH,故D正确.
故选A.
本题解析:
本题难度:简单
3、选择题 下列化学用语正确的是( )
A.Cl-离子的结构示意图:

B.8个中子的碳原子的核素符号:14C
C.硝酸铁的化学式:Fe(NO3)2
D.N2的电子式:

参考答案:A、Cl-离子的质子数为17,核外电子数为18,有3个电子层,最外层电子数为8,离子结构示意图为
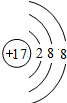
,故A错误;
B、C原子的质子数为6,8个中子的C原子的质量数为8+6=14,8个中子的C原子的核素符号614C或14C,故B正确;
C、硝酸铁中铁元素化合价为+3价,化学式为Fe(NO3)3,选项中Fe(NO3)2为硝酸亚铁的化学式,故C错误;
D、N原子没有成键的孤对电子对没有标出,氮气分子中N原子之间形成3对共用电子对,电子式为
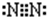
,故D错误.
故选:B.
本题解析:
本题难度:一般
4、选择题 下列物质中,属于含有非极性键的共价化合物的是
[? ]
A.N2
B.Na2O2
C.C2H4(乙烯)?
D.CH4
参考答案:C
本题解析:
本题难度:简单
5、选择题 实验测得BeCl2为共价化合物,两个Be-Cl键间的夹角为180°,由此可判断BeCl2属于
[? ]
A.由极性键形成的极性分子
B.由极性键形成的非极性分子
C.由非极性键形成的极性分子
D.由非极性键形成的非极性分子
参考答案:B
本题解析:
本题难度:简单