微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 写出下列盐溶液的水解离子方程式:
(1)Fe(NO3)3 ;
(2)NaF ;
(3)K2CO3 ; ;
参考答案:(1)Fe3+ +3H2O 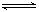 Fe(OH)3 + 3H +
Fe(OH)3 + 3H +
(2)F- +H2O 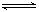 HF + OH-
HF + OH-
(3)CO32-+H2O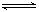 HCO3-+ OH- ;
HCO3-+ OH- ;
HCO3-+H2O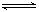 H2CO3+ OH-
H2CO3+ OH-
本题解析:(1)多元弱碱阳离子一步水解
(3)多元弱酸的酸根离子要分多步水解
本题难度:一般
2、填空题 (共10分)常温下,如果取0.1 mol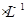 HA溶液与0.1mol
HA溶液与0.1mol 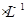 NaOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的pH=8,试回答以下问题:
NaOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的pH=8,试回答以下问题:
(1)混合溶液的pH=8的原因:____(用离了方程式表示)。
(2)混合溶液中由水电离出的c(OH-)=____
(3)求出混合溶液中下列算式的精确计算结果(填具体数值):
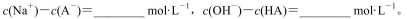
(4)己知NH4A 溶液为中性,又知HA溶液加到Na2CO3溶液中有气体放出,试推断(NH3)2CO3溶液的pH_____7(填“>”、“<”或“=”);
参考答案:(每空2分,共10分)
(1)A-+H2O HA+OH- (2) 1.0×10-6mol・L-1
HA+OH- (2) 1.0×10-6mol・L-1
(3)9.9×10-7 1.0×10-8 (4) >
本题解析:
(1)等物质的量的一元酸和一元碱恰好反应生成盐和水,生成的盐溶液呈碱性说明该酸是弱酸, 生成的盐能水解导致溶液中OH-浓度大于H+浓度,溶液的pH值大于7,水解的离子方程式为A-+H2O HA+OH-
HA+OH-
(2)该盐含有弱根离子能促进水的电离,溶液显碱性,溶液中的OH-都是由水电离所得,该溶液的PH=8,POH=6,则混合溶液中由水电离出的c( OH-)= 1.0×10-6mol・L-1
(3)由电荷守恒可知,c(Na+)-c(A-)=c(OH-)-c(H+)=10-6-10-8=9.9×10-7mol/L;0.1mol/L HA溶液与0.1mol/L NaOH溶液等体积混合生成NaA溶液;测得混合溶液的pH=8,c(H+)=10-8mol/L;溶液显碱性,说明A-离子水解,溶液中存在质子守恒:c(OH-)=c(H+)+c(HA),则c(OH-)-c(HA)=c(H+)=10-8mol/L;
(4)将HA溶液加到Na2CO3溶液中有气体放出,说明HA的酸性比碳酸的强,NH4A溶液为中性,说明相同条件下,氨水和HA的电离程度相同,所以(NH4)2CO3中铵根离子的水解程度小于碳酸根离子的水解程度,所以溶液的pH>7。
考点:考查盐类的水解,酸碱混合时的守恒关系及有关PH的计算等知识。
本题难度:一般
3、选择题 下列实验不能达到预期目的的是:
序号
| 实验操作
| 实验目的
|
A
| 配制FeCl2溶液时,向溶液中加入少量Fe和稀盐酸
| 抑制Fe2+水解和防止Fe2+被氧化
|
B
| 将饱和FeCl3溶液滴入沸水中,溶液变红褐色
| 制备Fe(OH)3胶体
|
C
| 测定等浓度的Na2CO3和Na2SO3 溶液的pH,前者pH比后者的大
| 比较S、C的非金属性强弱
|
D
| 将充满NO2的密闭玻璃球浸泡在热水中
| 研究温度对化学平衡移动的影响
|
参考答案:C
本题解析:A. Fe2+有还原性,容易被空气中的氧气氧化为Fe3+,所以配制溶液时,应该加入少量的Fe粉;FeCl2是强酸弱碱盐,容易发生水解反应使溶液变浑浊,为了防止盐水解,应该向溶液中加入少量的稀盐酸,正确;B.盐的水解反应是吸热反应,升高温度会促进盐的水解,将饱和FeCl3溶液滴入沸水中,溶液变红褐色,正确;C.由于酸性H2SO3>H2CO3,酸的酸性越强,其相应的盐水解程度就越小,所以测定等浓度的Na2CO3和Na2SO3 溶液的pH,前者pH比后者的大,可以比较溶液的酸性强弱,但是由于S、C的非金属性强弱应该看元素的最高价的含氧酸的酸性强弱,H2SO3不是最高价的含氧酸,因此不能比较其非金属性强弱,错误;D.在充满NO2的密闭玻璃球中存在可能反应:2NO2 N2O4,该反应的正反应是放热反应,将充满NO2的密闭玻璃球浸泡在热水中,根据平衡移动原理:平衡向吸热反应方向移动,产生更多的NO2,因此可以用于研究温度对化学平衡移动的影响,正确。
N2O4,该反应的正反应是放热反应,将充满NO2的密闭玻璃球浸泡在热水中,根据平衡移动原理:平衡向吸热反应方向移动,产生更多的NO2,因此可以用于研究温度对化学平衡移动的影响,正确。
考点:考查化学实验操作即完成实验目的的关系的知识。
本题难度:一般
4、填空题 某盐或“类盐”的化学式为XmYn最简结构,将一定量的该盐溶于足量的水时:
(1)若m≠n,测得溶液的pH为5,则该盐与水反应的离子方程式可能为__________________。
(2)若m≠n,测得该盐溶液的pH为9,则该盐与水反应的离子方程式可能为__________________。
(3)若m≠n,X、Y为同周期的短周期元素,XmYn溶于水时,既有白色沉淀,又有无色气体放出,则溶于水的化学方程式为__________________。
(4)若m≠n,X、Y为不同周期的短周期元素,XmYn溶于水时,既有白色沉淀,又有无色气体放出,则溶于水的化学程式为。__________________。
(5)若X、Y为同主族元素,且m=n,则该物质溶于水的化学方程式为__________________。溶于水后溶液呈碱性,如__________________;溶于水后溶液呈酸性,如__________________。
参考答案:
(1)Xn++nH2O X(OH)n+nH+
X(OH)n+nH+
(2)Ym-+H2O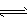 HY(m-1)-+OH-
HY(m-1)-+OH-
(3)Al2S3+6H2O=2Al(OH)3↓+3H2S↑
(4)Mg3N2+6H2O=3Mg(OH)2↓+2NH3↑ ,Al4C3+12H2O=4Al(OH)3↓+3CH4↑
(5)NaH+H2O=NaOH+H2↑,KH+H2O=KOH+H2↑,BrCl+H2O=HBrO+HCl,
IBr+H2O=HIO+HBr ;NaH、KH;BrCl、IBr
本题解析:
本题难度:一般
5、选择题 下列说法正确的是
A.明矾水解形成的Al(0H)3胶体能杀菌消毒,可用于水的净化
B.镀锡的铁制品比镀锌的铁制品耐用
C.乙醇和乙酸都能溶于水,都是电解质
D.分别与等物质的量的HC1和CH3COOH恰好中和时,消耗NaOH的物质的量相同