微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 今有浓度均为0.1mol/L的醋酸、盐酸和硫酸三种稀溶液,按下列题示回答问题(回答时用“>”、“<”或“=”连接a、b、c):
(1)设三种溶液的pH分别为a、b、c,则大小关系为 。
(2)若取等质量的锌分别跟这三种溶液反应,使锌恰好完全反应时,所消耗三种酸的体积分别为a、b、c,则其大小关系为 。
(3)取上述三种溶液各10mL,分别跟0.1mol/LNaOH溶液10mL混合,当反应结束后,三种混合液的pH分别为a、b、c ,则其大小关系为 。
参考答案:(1)a>b>c(2)a=b>c(3)a>b>c
本题解析:(1)醋酸是一元弱酸。在溶液中存在电离平衡:CH3COOH CH3COO-+H+。c(CH3COOH)>c(H+),盐酸和硫酸都是强酸,完全电离,盐酸是一元强酸,硫酸是二元强酸,电离方程式为: HCl=H++Cl-.H2SO4=2H++SO42-。所以c(H+)硫酸>盐酸>醋酸。c(H+)越大,溶液的pH越小。故设三种溶液的pH分别为a、b、c,则大小关系为a>b>c 。(2)(2)若取等质量的锌分别跟这三种溶液反应,使锌恰好完全反应时,所消耗三种酸的体积分别为a、b、c,假设Zn的物质的量为1mol,则消耗的三种酸的物质的量为2mol、2mol、1mol.由于三种酸的物质的量浓度相等,所以消耗的三者的体积大小关系为a=b=2c(或a=b>c)。(3)取上述三种溶液各10mL,分别跟0.1mol/LNaOH溶液10mL混合,当反应结束后,得到的物质分别NaAc、NaCl、NaHSO4。NaAc是强碱弱酸盐,水解使溶液显碱性;NaCl是强酸强碱盐,不水解,溶液显中性;NaHSO4是强酸的酸式盐,电离产生H+使溶液显酸性。若三种混合液的pH分别为a、b、c ,则其大小关系为a>b>c。
CH3COO-+H+。c(CH3COOH)>c(H+),盐酸和硫酸都是强酸,完全电离,盐酸是一元强酸,硫酸是二元强酸,电离方程式为: HCl=H++Cl-.H2SO4=2H++SO42-。所以c(H+)硫酸>盐酸>醋酸。c(H+)越大,溶液的pH越小。故设三种溶液的pH分别为a、b、c,则大小关系为a>b>c 。(2)(2)若取等质量的锌分别跟这三种溶液反应,使锌恰好完全反应时,所消耗三种酸的体积分别为a、b、c,假设Zn的物质的量为1mol,则消耗的三种酸的物质的量为2mol、2mol、1mol.由于三种酸的物质的量浓度相等,所以消耗的三者的体积大小关系为a=b=2c(或a=b>c)。(3)取上述三种溶液各10mL,分别跟0.1mol/LNaOH溶液10mL混合,当反应结束后,得到的物质分别NaAc、NaCl、NaHSO4。NaAc是强碱弱酸盐,水解使溶液显碱性;NaCl是强酸强碱盐,不水解,溶液显中性;NaHSO4是强酸的酸式盐,电离产生H+使溶液显酸性。若三种混合液的pH分别为a、b、c ,则其大小关系为a>b>c。
考点:考查等浓度的醋酸、盐酸和硫酸三种稀溶液的pH、与Zn、NaOH等发生反应时溶液的体积及pH的关系的知识。
本题难度:一般
2、选择题 图像可直观地描述化学反应的进程或结果,下列图像正确的是
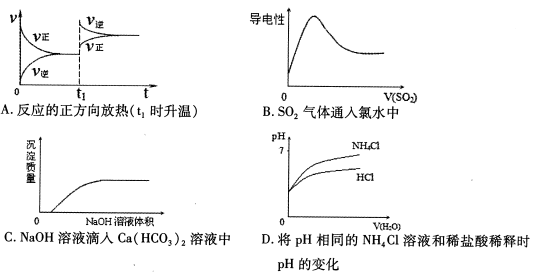
参考答案:A
本题解析:A、正反应放热,升高温度正逆反应速率均增大,但逆反应速率增大的程度大于正反应速率增大的程度,平衡向逆反应方向移动,A正确;B、SO2气体通入氯水中发生反应:SO2+Cl2+2H2O=H2SO4+2HCl,溶液的导电性始终增强,B错误;C、氢氧化钠滴入碳酸氢钙溶液中立即产生碳酸钙沉淀,C错误;D、稀释氯化铵溶液促进铵根水解,盐酸是强酸,因此盐酸溶液的pH变化大,D错误,答案选A。
考点:考查外界条件对反应速率和平衡状态的影响、溶液导电性、离子反应以及pH变化判断等图像分析
本题难度:一般
3、选择题 向10mL pH = 2的NaOH溶液中加入10 mL某酸,再滴入几滴甲基橙,则溶液呈红色。这种酸可能是 ( )
A.pH = 2的硫酸
B.pH = 2的醋酸
C.0.01 mol/L甲酸
D.0.01 mol/L硝酸