��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ���ֶ���������Ԫ��A��B��C��D��E��F��ԭ������������������A��E�����壬B��Fͬ���壮��֪�����µ���A��E��״̬��ͬ��D�ĺ˵������B��������������2��������F��һ����Ҫ�İ뵼����ϣ��������ƶ���ȷ���ǣ�������
A����A��C��D����Ԫ����ɵĻ�����һ���ǹ��ۻ�����
B��ԭ�Ӱ뾶�ɴ�С��˳���ǣ�E��F��C��D
C��B��C��E��F����Ԫ�ص�����������Ӧ��ˮ����������ǿ����B��������ǿ����E
D��Ԫ�صķǽ�������ǿ������˳���ǣ�D��C��F��B
�ο��𰸣�B
���������
�����Ѷȣ���
2��ѡ���� X��Y��Z��W���ֶ�����Ԫ�أ�����X����������Y�����Ӿ�����ͬ�ĵ��Ӳ�ṹ����W�������ӵ�������ǿ��ͬ������ȵ������X�������ӵ������ԣ���Z�������Ӱ뾶����ͬ������ȵ�ɵ�Y�����Ӱ뾶����������Ԫ�ص�ԭ�����ɴ�С��˳��Ϊ��������
A��W��Y��X��Z
B��Z��Y��W��X
C��X��Y��Z��W
D��Z��X��Y��W
�ο��𰸣�D
���������
�����Ѷȣ�һ��
3������� X��Y��Z��R��W����Ԫ�طֲ���������ͬ�Ķ����ڣ����ǵ�ԭ��������������YR2����Ҫ���������壬W�Ƕ������н�������ǿ��Ԫ�أ�����W������������ˮ�������X��Z��ɵ�������
��1��ZԪ�������ڱ���λ�ڵ�2���ڣ���______�壮
��2�����еĻ�ѧ����______��
��3���Ƚ�Y��R��Wԭ�Ӱ뾶�Ĵ�С��______��______��______��
��4��һ�������£�X���ʺ�R�����ڼ�Ũ��Һ�п����γ�ȼ�ϵ�أ���ȼ�ϵ�ص������ķ�Ӧʽ��______��
��5����ҵ�������ҵ����˵ķ�Ӧ������______�ͽϸߵ��¶ȣ���ÿ����amol��ʱ�ų�bkJ��������÷�Ӧ���Ȼ�ѧ����ʽΪ______��
��6���������������ֻ����ﶼֻ��X��Y��R����Ԫ����ɣ���һ��������������ת����ϵ��

�������ճ������г��õ����Ե�ζƷ�������ϱ����ɶ��Ļ�ѧ����ʽΪ��______��
�ο��𰸣�YR2����Ҫ���������壬ӦΪCO2����YΪCԪ�أ�RΪOԪ�أ�Y��Z��Rԭ����������������ZΪNԪ�أ�W�Ƕ������н�������ǿ��Ԫ�أ�ӦΪNaԪ�أ�X��Y��Z��R��W����Ԫ�طֲ���������ͬ�Ķ����ڣ���XӦΪ��һ����Ԫ��H������W������������ˮ���ӦΪNaOH������X��Z��ɵ�������ӦΪNH3����
��1��ZΪNԪ�أ�ԭ������Ϊ7��ԭ�Ӻ�����2�����Ӳ㣬����������Ϊ5��λ�����ڱ��ڶ�����VA�壬�ʴ�Ϊ��VA��
��2����ΪNaOH��Ϊ���ӻ�����������Ӽ���NaOH��O-HΪ���ۼ����ʴ�Ϊ�����Ӽ������ۼ���
��3��O��Cλ��ͬһ���ڣ�Cԭ�Ӱ뾶����O��Naλ�ڵ������ڣ���O��C����һ�����Ӳ㣬ԭ�Ӱ뾶�����������ԭ�Ӱ뾶��С��ϵΪ��Na��C��O���ʴ�Ϊ��O��C��Na��
��4����������ȼ�ϵ���У�����������������ԭ��Ӧ����OH-���缫��ӦʽΪO2+2H2O+4e-=4OH-���ʴ�Ϊ��O2+2H2O+4e-=4OH-��
��5����ҵ�ϳɰ��ڸ��¡���ѹ�����������½��У���ÿ����amolNH3ʱ�ų�bkJ������������1molNH3�ų�bakJ�����������Ժϳɰ����Ȼ�ѧ����ʽΪN2��g��+3H2��g�� 2NH3��g����H=-2bakJ?mol-1��
2NH3��g����H=-2bakJ?mol-1��
�ʴ�Ϊ�����ʵĴ�������ѹ��N2��g��+3H2��g�� 2NH3��g����H=-2bakJ?mol-1��
2NH3��g����H=-2bakJ?mol-1��
��6�������ճ������г��õ����Ե�ζƷ��ӦΪCH3COOH�����ΪCH3CH2OH����ΪCH3CHO�������ɶ��ķ�ӦΪ2CH3CH2OH+O2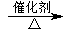 2CH3CHO+2H2O��
2CH3CHO+2H2O��
�ʴ�Ϊ��2CH3CH2OH+O2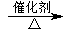 2CH3CHO+2H2O��
2CH3CHO+2H2O��
���������
�����Ѷȣ�һ��
4������� X��Y��Z��W��Ԫ�����ڱ�ǰ�������е����ֳ���Ԫ�أ������Ϣ�����
Ԫ��
�����Ϣ
X
X���⻯������к�10�����ӣ�����������ṹ
Y
Y��Xͬ���ڣ�������������Ӧ��ˮ������һ��ǿ��������
Z
��������Ԫ���У�Z�縺����С
W
W�Ļ�̬ԭ�Ӻ���M�ܲ��������˵��ӣ�N�ܲ�ֻ��1������