��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ��Ϊ�˳�ȥKCl��Һ��������Mg2����SO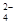 ����ѡ��Ba(OH)2��HCl��K2CO3�����Լ��������²��������
����ѡ��Ba(OH)2��HCl��K2CO3�����Լ��������²��������
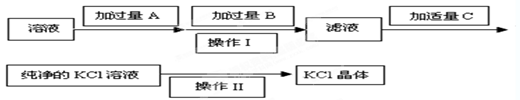
��1�������Լ��У� B��?��C��?��
(2)�������������?��
(3)�ӹ���Aʱ�����йط�Ӧ�����ӷ���ʽΪ ??��??��
��һ����ɫϡ��Һ�п��ܺ���Na+��Fe3+��H+��Mg2����CO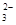 ?��OH����HCO
?��OH����HCO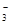 ��Cl���������е������֡�Ϊ��ȷ����Һ����ɣ����������²�����
��Cl���������е������֡�Ϊ��ȷ����Һ����ɣ����������²�����
����ʯ����ֽ����Һ������ԣ���ֽ����ɫ��
��ȡ2������Һ���ȼ�����ϡ�����ữ��������������ټ��Ȼ�����Һ���м��飬û����������
��1��ԭ��Һ��һ�����ڵ�������?��һ�������ڵ�������?��
��2�������������������ܿ϶��Ƿ���ڵ�������?���������һ����ʵ�鷽�����ж��Ƿ�����������ӡ�?
�ο��𰸣���(1)K2CO3��1�֣��� HCl��1�֣���? (2)�����ᾧ��1�֣���
��3��Mg2++2OH��=Mg(OH)2����2�֣�;Ba2++SO42��=BaSO4����2�֣���
��1��Na+,CO32��,OH����2�֣���Fe3+,H+,Mg2+,HCO3����2�֣�����ȫ�Ե�2�֣�©д��1�֣��д����÷֣�
(2)Cl����1�֣��� ȡ����ԭ��Һ����������ϡ�����ữ���ٵμ�����AgNO3,���а�ɫ��������������Cl��,����û�С���2�֣�
���������
��(1�������������Խ�MgCl2��MgSO4�е����������������ȥ������ʱ��ÿһ�����ӵ��Լ����ǹ����ģ�������������������̼��س�ȥ���������̼���������������ȥ�����Լ�A��B��C������Ba��OH��2��K2CO3��HCl��
��2��Һ��������ķ����ǹ��ˣ����ò���������©�������������ձ������ʵ���Һ��þ���ķ����������ᾧ��
��3�������������Խ�MgCl2��MgSO4�е����������������ȥ������ʽ�ֱ�Ϊ��MgCl2+Ba��OH��2�TBaCl2+Mg��OH��2����MgSO4+Ba��OH��2�TBaSO4��+Mg��OH��2����
��1����ʯ����ֽ����Һ������ԣ���ֽ����ɫ,˵����Һ�ʼ��ԡ���OH-���ӷ�Ӧ�����Ӳ��ܹ��棬Fe3+��H+��Mg2����HCO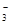 �ų���������ϡ�����ữ�������������˵������CO
�ų���������ϡ�����ữ�������������˵������CO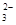 ������ԭ��Һ��һ�����ڵ�������Na+����Һ�����ٺ���һ�������ӣ�,CO32��,OH����һ�������ڵ�������Fe3+,H+,Mg2+,HCO3���������ܿ϶��Ƿ���ڵ�������Cl����ȡ����ԭ��Һ����������ϡ�����ữ���ٵμ�����AgNO3,���а�ɫ��������������Cl��,����û�С�
������ԭ��Һ��һ�����ڵ�������Na+����Һ�����ٺ���һ�������ӣ�,CO32��,OH����һ�������ڵ�������Fe3+,H+,Mg2+,HCO3���������ܿ϶��Ƿ���ڵ�������Cl����ȡ����ԭ��Һ����������ϡ�����ữ���ٵμ�����AgNO3,���а�ɫ��������������Cl��,����û�С�
�����Ѷȣ�һ��
2��ѡ���� ���������У��ȿ������ᷴӦ���ֿ�������������Һ��Ӧ���ǣ�������
A��NaHSO4
B��NaHCO3
C��Na2SO3
D��NH4NO3
�ο��𰸣�A��NaHSO4�������Ӧ��A����
B��NaHCO3�����ᷴӦ�ų�������̼���壬������������Һ��Ӧ����̼���ƣ�B��ȷ��
C��Na2SO3������������Һ����Ӧ��C����
D��NH4NO3�������Ӧ��D����
��ѡB��
���������
�����Ѷȣ���
3���ƶ��� ��7�֣�ij����Һ�п��ܺ���A13+��Fe3+��K+��NH4+��C1-�����ӣ���ͨ������ʵ������е������ӽ��м��飺
��1��ȡ��������Һ����ϸ�۲죬����ɫ��
��2������������Һ�еμ�NaOH��Һ���а�ɫ�������ɣ�NaOH��Һ�������������ȫ�ܽ�,�ټ��Ȼ��д̼�����ζ�������������������ʹʪ��ĺ�ɫʯ����ֽ������
�ݴ˿����жϸô���Һ��һ�����е���������?��һ��û�е���������?������һ��������û�м��飬�����������ӵ�ʵ�鷽���ǣ���дʵ�����ƣ�?��������?��
�ο��𰸣���7�֣�A13+? NH4+ (2��)? Fe3+?(2��)��?��ɫ��Ӧ (1��)
ͨ����ɫ�ܲ���������ɫ����ɫ? (2��)
���������ʵ�飨1��˵������Һ��û������ɫ�����ӣ���Fe3+�����ڣ�
�����Ӻ��������Ʒ�Ӧ���ɰ�ɫ�������������������������������Ʒ�Ӧ����ƫ�����ƣ����Կ��������������г����������ʧ�����������ӵ�������Ӧ��
笠������ڼ������������������Ʒ�Ӧ������ʹʪ��ĺ�ɫʯ����ֽ����ɫ�İ���������笠����ӵ�������Ӧ��
����ʵ�飨2�������ж�ԭ��Һ�к���A13+��NH4+��
ͨ������ʵ���������ж���Һ���Ƿ��м����ӣ�Ҫ������Ƿ��м����ӣ�����ͨ����ɫ��Ӧ����ɫ��Ӧ�ķ����ǣ�ͨ����ɫ�ܲ����۲���棬����������ɫ��˵���м����ӣ�����û�У�
�ʴ�Ϊ��A13+��NH4+��Fe3+����ɫ��Ӧ������ɫ�ܲ����������ɫ
���������⿼���˳������ӵļ��飬�������ʵļ����У����������ӵļ��顢���������ӵļ��顢��������ļ��飻Ҫע����ǣ���ɫ��Ӧ��Ԫ�ص����ʲ��ǵ��ʵ����ʣ�Ҫ�۲��Ԫ�ص���ɫ��Ӧʱ����������ɫ�ܲ�������ȥ��Ԫ�صĸ��ţ����ܹ۲쵽��Ԫ����ɫ��Ӧ����ɫ
�����Ѷȣ�һ��
4��ѡ���� 1 mol�����ڹ��յ���������ȫ��Cl2����ȡ����Ӧ�������ɵ����ʵ����������ȴ������ҪCl2�����ʵ���Ϊ
A.4 mol
B.3 mol
C.2.5 mol
D.0.5 mol
�ο��𰸣�C
���������
�����Ѷȣ���
5��ѡ���� ���������У�ֻ�����Ӽ�����
A.MgF2
B.Al2O3
C.NH4Cl
D.H2O
�ο��𰸣�AB
���������
�����Ѷȣ�����