��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ���������û�������������������ų��ķ�������Ҫ��ѧ�ɷ�ΪSiO2��Լ45%��Fe2O3��Լ40%��Al2O3��Լ10%��MgO��Լ5%��Ŀǰ�ҹ��Ѿ��ڼ�����ȡ��ͻ��--��������������
I��ijѧ��̽����ѧϰС���ͬѧ����˲�ͬ�ķ������û�ѧ����֪ʶ���н���Ԫ�ص���ȡʵ�飨��֪25��������þKsp=5.6��10-12����������Ksp=3.5��10-38��һˮ�ϰ����볣��K=1.8��10-5���䱥����Һ��c��OH-��ԼΪ1��10-3mol?L-1����
����һ��
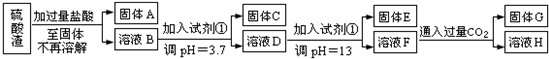
��ش�
��1��д������E�Ļ�ѧʽ��______��
��2���Լ�����______
A����������?B��������?C����ˮ?D��ˮ
��3����Ҫȷ�ⶨ��Һ��pH�Ƿ�ﵽ3.7��������Ʒ�пɹ�ʹ�õ���______
A��ʯ����Һ?B���㷺pH��ֽ?C������pH��ֽ?D��pH��
��4����ҺH�����ʵĻ�ѧʽ��______
��5��Ҫ������C������E����G��ת��Ϊ��Ӧ���ȶ������������е�ʵ�����Ϊ______��
��6������������Һ����ı仯���������ҺH��c��Mg2+��=______��
��������
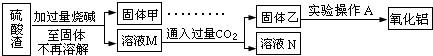
��ش�
��7���˷�������Ҫ�����У�______
��8��д������ҺM����������������У�����Ҫ��ѧ��Ӧ�����ӷ���ʽ��______
II��Ϊ�˷���ij����������Ԫ�صĺ������Ƚ�������Ԥ����������Ԫ�ػ�ԭ��Fe2+������KMnO4����Һ�����������½���������ԭ�ζ�����Ӧ�����ӷ���ʽ�ǣ�5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O��
��1���жϵ���ζ��յ��������______��
��2��ijͬѧ��ȡ2.000g��������Ԥ������������ƿ�����Ƴ�100mL��Һ����ȡ25.00mL��������Һ����1.000��10-2mol?L-1KMnO4����Һ�ζ����ﵽ�ζ��յ�ʱ�����ı���Һ10.00mL�������������Ԫ�ص�����������______��
�ο��𰸣�I�������������ijɷ�ΪSiO2��Fe2O3��Al2O3��MgO�������������мӹ�������ʱ����������������Ӧ�����Թ���A�Ƕ������裬��������������������þ�����ᷴӦ��������ҺB���������Ȼ�þ���Ȼ������Ȼ��������ᣨ������������ҺB�м��Լ��ٲ�������Һ��pHֵΪ3.7�����������ҺpH=3.7ʱFe3+�Ѿ�������ȫ֪���Լ������ܺ��Ȼ�����Ӧ���ɳ����������Һ������ӷ�Ӧû�г������ɣ������Լ���ֻ����ǿ����Һ������C����������������ҺD�м����Լ��ٲ�������Һ��pHֵΪ13����Һ��ǿ������Һ����Ԫ������Һ����ƫ��������Ӵ��ڣ�þ���Ӻ���������������������þ���������Թ���E��������þ����ҺF�����ʺ���ƫ�����ƺ��Ȼ��ƣ���F��Һ��ͨ�����������̼���壬ƫ�����ƺͶ�����̼��Ӧ����������������������G������������
��1������E��������þ���ʴ�Ϊ��Mg��OH��2��
��2���Լ�����ǿ����Һ����ѡ��A��?
��3����PHֵ��ȷ��С�����һλ����ʯ����Һ��õ�PHֵ��һ����Χ�ڣ��㷺pH��ֽ��õ�PHֵ��һ������������pH��ֽ��pH�ƾ���ȷ��С�����һλ����ѡ��CD��?
��4����ҺF�����ʺ���ƫ�����ƺ��Ȼ��ƣ���F��Һ��ͨ�����������̼���壬ƫ�����ƺͶ�����̼��Ӧ������������������̼�����ƣ��ʴ�Ϊ��NaCl��NaHCO3��
��5������C����������������E��������þ������G���������������Ⱦ��ɷֽ�õ���Ӧ��������ʴ�Ϊ�����գ�?
��6������Һ��PHֵΪ13��C��OH-��=10-1mol?L-1��Ksp=C��Mg2+����C2��OH-��=C��Mg2+����10-2=5.6��10-12������C��Mg2+��=5.6��10-10?mol?L-1���ʴ�Ϊ��5.6��10-10?mol?L-1��
��7���ٲ�Ʒ�������������д�����Ƕ������裻�ڲ�����Լ����������ʴ�Ϊ���ٲ�Ʒ�������������д�����Ƕ������裻�ڲ�����Լ�����������
��8����Һ��Ҫ���й����ƣ������ƺͶ�����̼��Ӧ���ɹ��������̼�����ƣ�����ʽΪ��Na2SiO3+2CO2+2H2O=H2SiO3��+2NaHCO3���ʴ�Ϊ��SiO32-+2CO2+2H2O=H2SiO3��+2HCO32-��
II����1����KMnO4����Һ��������һ��ָʾ�����ʴ�Ϊ����������һ��KMnO4����Һʱ����Һ��ɫ��Ϊ�Ϻ�ɫ�����ڰ�����ڲ���ɫ��
��2�����ù�ϵʽ�����㣺
? ? 5Fe2+��MnO4-
?2��10-5mol? 1.000��10-2mol?L-1��0.01L��4
��Ԫ�ص�����Ϊ��2��10-3mol��56g/mol=1.12��10-1g����Ԫ�ص���������Ϊ?1.12��10?-1g2.000g��100%=5.6%���ʴ�Ϊ��5.6%��
���������
�����Ѷȣ�һ��
2�������� ��֪Fe2O3�ڸ�¯�������з�Ӧ��Fe2O3��CO��2FeO��CO2����Ӧ�γɵĹ������Fe2O3��FeO���У�Ԫ������������������ mFe�UmO��ʾ
��1���������������У�mFe�UmO��������?��ѡ�� a��b��c��ѡ�۷֣�
��a��21�U9?��b��21�U7.5?��c�� 21�U6
��2����mFe�UmO��21�U8������Fe2O3��CO��ԭ�İٷ���
��3���� Fe2O3��CO��ԭ�İٷ���ΪA������A���ͻ������mFe�UmO�Ĺ�ϵʽΪ���ú�mFe��mO�Ĵ���ʽ��ʾ���� A����?
������ͼ�л���A%��mFe/mO��ϵ��ͼ��
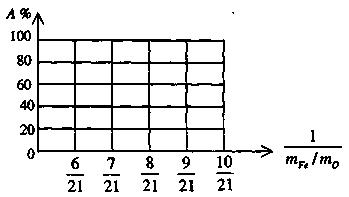
��4����� Fe2O3��CO�ķ�Ӧ���������У�
3Fe2O3��CO��2Fe3O4��CO2?��Fe3O4��CO��3FeO��CO2
�Է�����Ӧ�γɵĹ���������ܵ���ɼ���Ӧ��mFe�UmO����mFe�UmO��21�Ua��д��a��ȡֵ��Χ��������������±���
�������ɣ��û�ѧʽ��ʾ��
| a��ȡֵ��Χ
|
?
| ?
�ο��𰸣���1��a��c��
��2��33.3%
��3��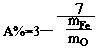

��4�����������Fe2O3��Fe3O4ʱ��8��a�� 9
���������Fe3 O4��FeOʱ6��a�� 8 O4��FeOʱ6��a�� 8
���������Fe 2O3��Fe3O4��FeOʱ6��a��9 �� 2O3��Fe3O4��FeOʱ6��a��9 ��
�����������
�����Ѷȣ���
3������� I������������ҩƬ��һ������ȱ����ƶѪ��ҩ����ij��ѧ����С��ⶨ������Ԫ�غ�����ʵ�鲽�����£�

��1���γ�ҩƬ���³Ƶ���Ʒag�����������Ѹ���ܽ⣬������Һ��������ͼ��ʾ�������Ƿ���ȷ��______���粻��ȷ��˵��ԭ����ȷ�ɲ���д��
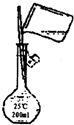
��2��ϴ�ӵ�Ŀ���dz�ȥ�����ڳ����ϵ�______����д���ӷ��ţ�
��3�������������գ���ȴ�����£��Ƶ�������Ϊb1g���ٴ����ղ���ȴ�����³Ƶ�������Ϊb2?g����b1-b2=0.3����������IJ���______����ͨ������ɵó������
��4����ͬѧ��Ϊ����������������������ˮ���������費�䣬�ԿɴﵽĿ�ģ�����������______
���û�ѧ����ʽ��ʾ��
II��ij��ѧ��ȤС������ʵ��ʱ����AgNO3��Һ��KI��Һ��ϣ������л�ɫ�������ɣ���Ѹ����ʧ����Ҿ��������Ϻ��֣����ܵ�ԭ���Ƿ��������з�Ӧ��AgI+I-

[AgI2]-
��1����ͬѧ�����������ʵ�鷽����������֤������Э�������ʵ�飮
ʵ��l����Ũ����Һ�еμ�AgNO3��Һ���۲쵽�������ɣ�
ʵ��2����AgNO3��Һ�еμӢ���Һ���л�ɫ�������ɣ���______��
��2����ͬѧ��ʵ�����õ���Һ�еμ�������Һ������ֳ����˳���������ͳ��ֳ�����ԭ��______��
��3����ͬѧ��ʵ�����õ���Һ�У��μ���ˮҲ���Կ�����������������ҺΪ��ɫ���ֲ����������ɫ�����ͨ���������ݣ�������Ϊ�����ij�����������AgCl�������ĵ�������______��
ͬѧ��ͨ����������֪����AgCl����������Ũ��ˮ����д����һ��Ӧ�����ӷ���ʽ______��
�ο��𰸣�I����1������ƿ��ר�����ƾ�ȷһ�����ʵ�����Ũ�ȵ���Һ����������ʵ������250.00mL��Һ����ȷ��0.01mL�����Ա�����250mL����ƿ��ͼ����200mL����ƿ����
�ʴ�Ϊ������ȷ������ƿӦ����250mL��
��2�����ݲⶨ������Ԫ�غ�����ʵ�鲽��֪������ϡ����������������ӣ�������ˮ���������ӣ����백ˮ���백�����Ӻ����������ӣ����պ���ɫ�Ĺ��壬Ŀ���ǵõ���������������������ǰ�Ĺ����л��������������ʣ����ȥ��Щ���ʣ�
�ʴ�Ϊ��NH4+��Cl-��SO42-��OH-����
��3�������������յ�Ŀ���ǵõ����ص��������������壬��������أ�˵�������к��нᾧˮӰ�����ĺ����IJⶨ�����Թ�������أ���ʵ���Ҳ�����õ���������ƽ��������ƽ�ľ�ȷ��Ϊ0.1�ˣ����Խ����������գ���ȴ�����£��Ƶ�������Ϊb1g���ٴ����ղ���ȴ�����³Ƶ�������Ϊb2?g����b1-b2=0.3����������IJ������ٴμ��ȣ������ڸ���������ȴ��������ֱ���������������0.1��Ϊֹ��
�ʴ�Ϊ���ٴμ��ȣ������ڸ���������ȴ��������ֱ���������������0.1��Ϊֹ��
��4��������������+2�۵������л�ԭ�ԣ������е��������л�ԭ�ԣ������������ڿ����кܿ챻��������������4Fe��OH��2+O2+2H2O=4Fe��OH��3��ֻ������������Ч���������ˮ�����յ�Ч����ͬ��
����4Fe��OH��2+O2+2H2O=4Fe��OH��3��
II����1����ͬѧ�����������ʵ�鷽����������֤��AgNO3��Һ��KI��Һ��ϣ������л�ɫ�������ɣ���Ѹ����ʧ��ʵ��������Ѿ��õ��˻�ɫ���������ݿ��ܷ����ķ�ӦAgI+I-?[AgI2]-��֪�ټ����μ�KI��Һ����ɫ�����ܽ⣬
�ʴ�Ϊ�������μ�KI��Һ����ɫ�����ܽ⣻
��2����ͬѧ��ʵ�����õ���Һ�еμ�������Һ���������ǿ�����ԣ��ܽ������������ɵ��ʵ⣬ʹ�����ӵ�Ũ�Ƚ��ͣ�����AgI+I-?[AgI2]-����Ӧ��Ũ�Ƚ��ͣ�ƽ�����淴Ӧ�����ƶ������Գ��ֵ⻯����ɫ������
�ʴ�Ϊ������������Һ�����Ὣ������������ʹ������Ũ�ȼ�С��ƽ��AgI+I-?[AgI2]-�����ƶ���
��3����ͬѧ��ʵ�����õ���Һ�У��μ���ˮҲ���Կ�����������������ҺΪ��ɫ���ֲ����������ɫ����ͨ���������ǵ��ܽ�ȱȽϴ�С���ܽ��С�����γɳ��������������ĵ�������AgI��AgCl���ܽ�ȣ�AgCl����������Ũ��ˮ���γ��������[Ag��NH3��2]+��
�ʴ�Ϊ��AgI��AgCl���ܽ�ȣ�AgCl+2NH3?H2O=[Ag��NH3��2]++Cl-+2H2O��
���������
�����Ѷȣ�һ��
4��ʵ���� ij�о���ѧϰС�����о���Fe2+�Ʊ�Fe(OH)2�� �����У����������ʵ�鷽���� �����У����������ʵ�鷽����
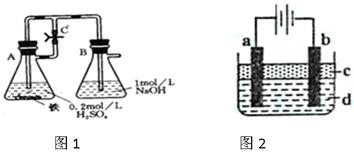
����һ������ͼ1����ʵ�飬����A�еķ�Ӧ��ʼʱ�����ɼ�C���ڴ�״̬��һ��ʱ��رյ��ɼ�C������A�еķ�Ӧ���ڽ��С�������_______�����й۲쵽��ɫ��������ʵ�����漰���Ļ�ѧ����ʽ�У�?
����������ͼ2����ʵ�飬���������������Һ�����ȹ۲쵽��ɫ������������ṩ���Լ���缫������ѡ����ȷ��������ں����ϣ�
�ٴ�ˮ?��NaCl��Һ?��NaOH��Һ?�����Ȼ�̼?��CuCl2��Һ?���Ҵ�?��Fe��?��ֲ����?��̼��
aΪ___________��bΪ___________��cΪ___________��dΪ___________��(�����)
�ο��𰸣����� һ��B��Fe+H2SO4=FeSO4+H2����FeSO4+2NaOH=Fe(OH)2��+Na2SO4�� һ��B��Fe+H2SO4=FeSO4+H2����FeSO4+2NaOH=Fe(OH)2��+Na2SO4��
H2SO4+2NaOH=Na2SO4��2H2O ���кͷ�Ӧ����ʽ��д���۷֣�
���������ߡ����ߡ��ࡢ��
�����������
�����Ѷȣ�һ��
5��ѡ���� ij����[Cr2O72��] ��ˮ����������泥�FeSO4����NH4��2 SO4��6H2O�ݴ�������Ӧ����Ԫ�غ�Ԫ����ȫת��Ϊ�������ó��������õ�n molFeO��FeyCrxO3�������Ǵ��������е�ʵ����ģ����������������?��?��
A��������������淋�������Ϊn��2-x��mol��
B��������ˮ��Cr2O72����������Ϊmol
C����Ӧ�з���ת�Ƶĵ�����Ϊ3nx mol��
D����FeO��FeyCrxO3��3x=y
�ο��𰸣�A
���������
�𰸣�A
��Ӧ����Ԫ�غ�Ԫ����ȫת��Ϊ����n mol FeO��FeyCrxO3���ɸ�ԭ���غ��Bѡ����ȷ��1 mol Cr2O72���ڷ�Ӧ�е�6 mol ���ӣ�1 mol Cr2O72����Ӧ��ת�Ƶĵ�����Ϊ6��1mol �� 3nx mol��Cѡ����ȷ��������FeO�Ļ��ϼ�û�б仯���ɵ�ʧ�����غ��3nx=ny�� 3x��y? Dѡ����ȷ��������Ԫ���غ�֪������������淋�������Ϊn��(1+y)mol �� n��(3x+1)mol�����ѡ��A�Ǵ���ġ�
�����Ѷȣ�����
|