��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� �������ӷ���ʽ��ȷ����
A����ˮ����������SO2���壺OH��+SO2=HSO3��
B��ϡ�����м���������ۣ� Fe + 4H��+ NO3��=Fe3��+ NO�� + 2H2O
C����NaOH��Һ���շ����е������NO+NO2+OH��=NO2��+H2O
D����������Һ��ͨ������CO2��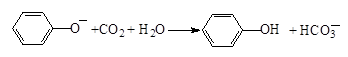
�ο��𰸣�D
�����������ˮ��������Һ�����������������ӱ�ʾ����NH3?H2O+SO2=NH4++HSO3������A�����������������ܷ�Ӧ�����������ӣ�������������������ӣ�ֻ���������ӣ���3Fe+8H��+2NO3��=3Fe2��+2NO�� + 4H2O����B��������������Һ���յ�����������������κ�ˮ����������Υ������غ�ԭ����ԭ�Ӹ����غ�ԭ��������NO+NO2+2OH��=2NO2��+H2O����C��ȷ���������ԣ�̼��>����>̼��������ӣ�������Һͨ�������Ķ�����̼���壬���ɱ��Ӻ�̼�����ƣ�����������̼���ƣ���D��ȷ��
�����Ѷȣ���
2��ѡ���� ����ȷ��ʾ���з�Ӧ���ӷ���ʽ����
[? ]
A��������ˮ��Ӧ��2F2+2H2O �� 4H++4F-+O2��
B��������KAl(SO4)2��Һ����μ���Ba(OH)2��Һ��SO42-ǡ�ó�����ȫ��
2Al3+��3SO42-��3Ba2+��6OH-�� 2Al(OH)3����3BaSO4��
C����Na2S2O3��Һ��ͨ������������S2O32-��2Cl2��3H2O �� 2SO32-��4Cl-��6H+
D��FeSO4������Һ��¶�ڿ����У�4Fe2+��O2��4H+�� 4Fe3+��2H2O
�ο��𰸣�D
���������
�����Ѷȣ�һ��
3��ѡ���� �������ӷ���ʽ����д�У���ȷ���ǣ�������
A����NaOH��Һȥ�������������Ĥ��Al2O3+2OH-+3H2O�T2[Al��OH��4]-+H2��
B��������Һ������������Һ��ϣ�H++SO42-+Ba2++OH-�TBaSO4��+H2O
C����������ˮ��Ӧ��Na+H2O�TNa++H2��
D��ʯӢ���ռ���Һ��Ӧ��SiO2+2OH-�TSiO32-+H2O
�ο��𰸣�A����NaOH��Һȥ�������������Ĥ�����ӷ�ӦΪAl2O3+2OH-+3H2O�T2[Al��OH��4]-����A����
B��������Һ������������Һ��ϵ����ӷ�ӦΪ2H++SO42-+Ba2++2OH-�TBaSO4��+2H2O����B����
C����������ˮ��Ӧ�����ӷ�ӦΪ2Na+2H2O�T2Na++2OH-+H2������C����
D��ʯӢ���ռ���Һ��Ӧ�����ӷ�ӦΪSiO2+2OH-�TSiO32-+H2O����D��ȷ��
��ѡD��
���������
�����Ѷȣ�һ��
4��ѡ���� �������ӷ���ʽ��ȷ����?��?��
A��������������Һ�м�������С�մ�Ca2����OH����HCO3��
B������Ȼ�þ��Һ���ܷ�Ӧ����ʽ��2Cl����2H2O
C��Na2S����ˮ��S2����2H2O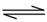 H2S��2OH��
H2S��2OH��
D��ͭƬ����ϡ���Cu��NO3����4H��
�ο��𰸣�A
�����������
�����Ѷȣ���
5��ѡ���� �������ӷ���ʽ��ȷ����
A����Ư��Һ��Һ��ͨ������SO2��3ClO-��SO2��H2O=SO42-��Cl-��2HClO
B��2-�������������������Һ��ˮ�⣺CH3CHBrCOOH��OH- CH3CH(OH)COOH��Br-
CH3CH(OH)COOH��Br-
C����һ������������Һ����μ���Ba(OH)2��Һ�������������ʱ��2Al3+��3SO42-��3Ba2+��6OH-=2Al(OH)3����3BaSO4��
D��������ϡ��Һ�м�������ϡ����6I-��2NO3-��8 H+=3I2��2NO����4H2O
�ο��𰸣�A
���������A.HClO��ǿ�������ԣ���SO2�л�ԭ�ԣ����ᷢ��������ԭ��Ӧ����Ӧԭ����ȷ����д�������ӷ���ʽ��ԭ����ȷ��B��2-�������������������Һ��ˮ�⡣����ˮ�ⷴӦ������Ӧ����кͷ�Ӧ�����Է�Ӧ����ʽΪ�� ��C����һ������������Һ����μ���Ba(OH)2��Һ��Al3+������ȫʱ����Ӧ�����ӷ���ʽΪ��2Al3+��3SO42-��3Ba2+��6OH-=2Al(OH)3����3BaSO4�����������μ�Ba(OH)2��Һ���ᷢ����Ӧ��2Al(OH)3��SO42-+ Ba2+��2OH-==BaSO4��+2AlO2-��4H2O��������������������ӣ�������һ������������Һ����μ���Ba(OH)2��Һ�������������ʱ�ܷ���ʽΪ��Al3+��2SO42-��2Ba2+��4OH-=AlO2-��2H2O ��2BaSO4��.����D��������ϡ��Һ�м�������ϡ����ᣬFe3+��HNO3���������ԣ�����HI����������ԭ��Ӧ���������ӷ���ʽΪ��Fe3++4I-��2NO3-��4 H+=2I2��2NO����2H2O+Fe2+������
��C����һ������������Һ����μ���Ba(OH)2��Һ��Al3+������ȫʱ����Ӧ�����ӷ���ʽΪ��2Al3+��3SO42-��3Ba2+��6OH-=2Al(OH)3����3BaSO4�����������μ�Ba(OH)2��Һ���ᷢ����Ӧ��2Al(OH)3��SO42-+ Ba2+��2OH-==BaSO4��+2AlO2-��4H2O��������������������ӣ�������һ������������Һ����μ���Ba(OH)2��Һ�������������ʱ�ܷ���ʽΪ��Al3+��2SO42-��2Ba2+��4OH-=AlO2-��2H2O ��2BaSO4��.����D��������ϡ��Һ�м�������ϡ����ᣬFe3+��HNO3���������ԣ�����HI����������ԭ��Ӧ���������ӷ���ʽΪ��Fe3++4I-��2NO3-��4 H+=2I2��2NO����2H2O+Fe2+������
�����Ѷȣ�һ��