��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ��ͼ����ʢ��ϡ H2SO4���ձ��з����õ������ӵĵ缫X��Y�����·�е���������ͼ��ʾ�����ڸ�װ�õ�����˵����ȷ����
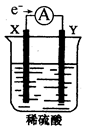
A��Y ���ϲ�����ɫ��ζ����
B�������缫�ֱ�Ϊ Fe ��̼������ X Ϊ̼���� Y Ϊ Fe
C��X ���Ϸ������ǻ�ԭ��Ӧ�� Y ���Ϸ�������������Ӧ
D�������缫���ǽ����������ǵĻ��˳��Ϊ X > Y
�ο��𰸣�AD
�����������ԭ����нϻ��õĽ�����������ʧȥ���ӣ�����������Ӧ�����Ӿ����ߴ��ݵ������ϣ�������Һ�е��������������ƶ������������ƶ��������õ����ӣ�������ԭ��Ӧ�����ݵ��ӵ�������жϣ�X�Ǹ�����Y����������Һ�е��������������õ����ӣ���������������ѡ��AD��ȷ��BC�Ǵ���ģ���ѡAD��
�����Ѷȣ�һ��
2��ѡ���� ��֪Na2S2O3+H2SO4�TNa2SO4+SO2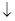 +SO2
+SO2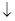 +H2O���и���ʵ������Һ���ȱ���ǵ���?
+H2O���и���ʵ������Һ���ȱ���ǵ���?
���
| ?
| �μӷ�Ӧ������
|
��Ӧ�¶�(��)
| 
| 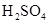
| 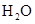
|
V(mL)
| C(mol/L)
| V(mL)
| C(mol/L)
| V(mL)
|
A
| 10
| 5
| 0��1
| 5
| 0��1
| 5
|
B
| 10
| 5
| 0��1
| 5
| 0��1
| 10
|
C
| 30
| 5
| 0��2
| 5
| 0��2
| 5
|
D
| 30
| 5
| 0��2
| 5
| 0��2
| 10
�ο��𰸣�C
���������Ӱ�췴Ӧ���ʵ������У�Ӱ���ɴ�СΪ�������¶ȡ�Ũ�Ⱥ�ѹǿ�����ų�AB��Ũ��Ϊ��Ϻ��Ũ�ȣ�C��������£�Ũ�ȴ�C�������
�����Ѷȣ���
3������� ��������������Ӧ����A��NaOH+HCl=NaCl+H2O? ��B��2FeCl3+Cu=2FeCl2+CuCl2
��1����������Ӧ���ʣ��ж��ܷ���Ƴ�ԭ���______
��2��������ܣ�˵����ԭ��______
��3��������ԣ���д���������������ƺ͵缫��Ӧʽ��
______��������������Ӧʽ��______
______�Ǹ�����������Ӧʽ��______��
�ο��𰸣���1��ԭ����ǽ���ѧ��ת��Ϊ���ܵ�װ�ã�ֻ��������ԭ��Ӧ���е��ӵ�ת�ƣ�����A��Ϊ��������ԭ��Ӧ��������Ƴ�ԭ��أ���B��Ϊ������ԭ��Ӧ��������Ƴ�ԭ��أ�
�ʴ�Ϊ����A�����У�B�����ԣ�
��2��ԭ����ǽ���ѧ��ת��Ϊ���ܵ�װ�ã�����������ԭ��Ӧ����������������Ӧ��A��Ϊ��������ԭ��Ӧ��û�з������ӵ�ת�ƣ��ʲ�����Ƴ�ԭ��أ�
�ʴ�Ϊ����A������������ԭ��Ӧ��û�з������ӵ�ת�ƣ�
��3����2FeCl3+Cu=2FeCl2+CuCl2��Ӧ�У�FeCl3����ԭ��Ϊ������Ӧ������̼�����������缫��ӦΪ2Fe3++2e-=2Fe2+��
Cu��������Ϊԭ��ظ�����Ӧ���缫��ӦΪCu-2e-=Cu2+��
�ʴ�Ϊ��̼����2Fe3++2e-=2Fe2+��ͭƬ��Cu-2e-=Cu2+��
���������
�����Ѷȣ�һ��
4��ѡ���� ����������ʵ���ж����ӵ�������˳��Ϊ��A+B2+=A2++B��D+2H2O=D��OH��2+H2������B��EΪ�缫��E������Һ���ԭ��أ��缫��ӦΪ��E2++2e-=E��B-2e-=B2+��������
A��E2+��B2+��A2+��D2+
B��D2+��E2+��A2+��B2+
C��D2+��A2+��B2+��E2+
D��A2+��B2+��D2+��E2+
��Դ:91������ 91eXAm.org
�ο��𰸣���A+B2+=A2++B�У�������B2+��A2+��
��D+2H2O=D��OH��2+H2����������H+��D2+��
����B��EΪ�缫��E������Һ���ԭ��أ��缫��ӦΪ��E2++2e-=E��B-2e-=B2+��������E2+��B2+��
�����⼸�����ӵ������Դ�С˳��Ϊ��E2+��B2+��A2+��D2+��
��ѡA��
���������
�����Ѷȣ���
5��ѡ���� �й�����ͼ��ʾԭ���(������װ�к�������KCl������Һ)������������ȷ����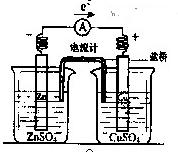
A��ͭƬ���к�ɫ���ʸ���
B��ȡ�����ź�������Ȼ����ƫת
C����Ӧ�У������е�K+������CuSO4��Һ
D��пƬ�Ϸ���������Ӧ
�ο��𰸣�B
���������ԭ����У���Һ�е��������������õ��ӣ�����ԭ��A��ȷ�������е�K+������CuSO4��Һ�����������ӡ�C��ȷ��пƬ�Ǹ�������������D��ȷ��Bȡ�����ź��������Ͽ���������ԭ��ء�
�����Ѷȣ�һ��
|