| �߿�ʡ������ | |
|
|
| �߿�ʡ������ | |
|
|
|
���л�ѧ�ر�֪ʶ�㡶ˮ�ĵ���ƽ�⡷��Ƶ����Ԥ�⣨2017�����°棩(ʮ)
�ο��𰸣�B �����������Һ������ʵ����c��H+����c��OH-����A��pH<7����һ�������ԣ���ˮ��100��ʱ��PH=6�����ԣ�����B����Һ�д��ڵ���غ�c��Na+��+c��H+��=c��OH-��+c��HA-��+2c��A 2-����c��Na+��=c��A2-������ c��H+����c��OH-������ȷ��C����Һ�п��ܲ�����HA-��H2A ��H2A������ǿ�ᣬ��NaHSO4��Һ�в�����H2SO4������D����Һ�������������ʵ���Ũ�ȵ�NaOH��Һǡ�÷�Ӧ��˵��������Ϊ��ʽ�Σ�������˵����Һ�������Ӻ�����������Ũ����Դ�С�����Բ���˵��ԭ��Һ�����ԣ����� �����Ѷȣ�һ�� 2��ѡ���� ������Һ���������ʵ���Ũ�ȹ�ϵһ����ȷ���ǡ������������������������������������� |
�ο��𰸣�B
���������A����Ϻ���ˮ��ƽ��NH4��+ OH�� NH3�� H2O ����Һ��c(Cl��)=0.05mol/L��c(Na��)=0.025mol/L������NH4��ֻ�������������룬����c(NH4��)��С��0.05mol/L��c(OH��)��С��0.025mol/L��������Һ�Լ��ԣ���c(OH��)��c(H��)������c(Cl��) ��c(NH4��)��c(Na��) ��c(OH��)��c(H��)��A����ȷ��
NH3�� H2O ����Һ��c(Cl��)=0.05mol/L��c(Na��)=0.025mol/L������NH4��ֻ�������������룬����c(NH4��)��С��0.05mol/L��c(OH��)��С��0.025mol/L��������Һ�Լ��ԣ���c(OH��)��c(H��)������c(Cl��) ��c(NH4��)��c(Na��) ��c(OH��)��c(H��)��A����ȷ��
B�����������غ��֪�����ʵ�����NaClO��NaHCO3�����Һ�У�c(HClO)��c(ClO��)��c(HCO3��)��c(H2CO3)��c(CO32��)��B��ȷ��
C��ֻ�е�HAΪǿ�ᣬMOHΪǿ��ʱ��c(M��)��c(A��)��c(OH��)��c(H��)���ܳ�����C����ȷ��
D�����ݵ���غ㣬ij��Ԫ�������ʽ��NaHA��Һ��c(Na��)+ c(H��)��c(OH��)��c(HA��)��2c(A2��)��D����ȷ����ѡB��
���㣺������ʵĵ��룻�����ˮ��
���������⿼��������ʵĵ��뼰�����ˮ���֪ʶ����һ�����Ѷȣ����ڴ�����Ŀ������Ӧ��Ϥ���������غ㡢�����غ�͵���غ㡣
�����Ѷȣ���
3��ѡ���� ���е��뷽��ʽ��д��ȷ���ǣ� ? ��
A��H2SO4�TH22++SO42-
B��NaHCO3�TNa++H++CO32-
C��NaOH�TNa++O2-+H+
D��Na3PO4�T3Na++PO43-
�ο��𰸣�D
���������
�����Ѷȣ�һ��
4������� ҹĻ���٣��������˻����᳡�����ڵƻ�Իͣ���ɪ�������貵��̻��ڿ�����ɰ����廷��ͼ�����볡�ڱ������Ӧ����ҹ�����������������ɣ��������������Դ�ͳ�Ļ�Ԫ�ء��й��족Ϊ��ɫ����ش���������
��1�����������˲��ֽ�����Ԫ��������___________��Ӧ���÷�Ӧ����__________�����������ѧ�����仯��
��2����ͼ��ʾ����Ԫ������A��B��C��D��E���ֻ����ԲȦ���沿��ָ���ֻ����ﺬ��һ����ͬԪ�أ����ֻ����������ֶ�����Ԫ���γɣ�ÿ�ֻ������������Ԫ�أ�A����������Ҫ�ɷ֣�B��E������������������Ϊ18��B���ȶ������н�ǿ�������ԣ���ϡ��Һ��ҽ���Ϲ㷺ʹ�õ���������E�ķ��ӽṹģ��Ϊ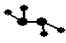 ��C��D��Ϊԭ�Ӿ��壬C����Ϊ���ά����Ҫ���ϣ�D����������Ԫ�ص�ԭ�Ӹ�����Ϊ3:4����������֮��Ϊ3:2������������Ϣ�ش��������⣺
��C��D��Ϊԭ�Ӿ��壬C����Ϊ���ά����Ҫ���ϣ�D����������Ԫ�ص�ԭ�Ӹ�����Ϊ3:4����������֮��Ϊ3:2������������Ϣ�ش��������⣺ 
��B��ˮ��Һ�������ԣ�����Ҫ�ĵ��뷽��ʽ�ɱ�ʾΪ___________________��D�Ļ�ѧʽ��_________��
��A��B��E�о����е�һ��Ԫ��Ϊ____________ (��Ԫ������) ��
��E����ʽΪ____________________��
��Һ̬B��Һ̬E��Ӧ������һ����̬���ʺ�һ�ֳ���Һ�壬1molB�μӷ�Ӧ�ų�����QkJ���䷴Ӧ���Ȼ�ѧ����ʽΪ _____________________��
��NH3�����е�Nԭ����һ�Թ¶Ե��ӣ��ܷ�����Ӧ��NH3+HCl=NH4Cl����д��E����������ʱ��������Ӧ�Ļ�ѧ����ʽ_____________________��
��3����ʵ�����ҹ�������ԱӦ�õ��Ӽ����ģ������и��ܵ�����N60�����Ľṹ��C60ʮ�����ơ���֪N60������ÿ��Nԭ�Ӿ��Ե����������������ԭ�ӣ���N60�ṹ��ÿ����ԭ�Ӿ��γ�8�����ӵ��ȶ��ṹ�����Ʋ�1��N60���ӵĽṹ�к���_________��N-N��
�ο��𰸣���1����ɫ��Ӧ������
��2����H2O2 HO2-+H+��Si3N4�����⣻��
HO2-+H+��Si3N4�����⣻�� ��
��
��N2H4(l)+2H2O2(l)=N2(g)+4H2O(l) ��H=-2QkJ/mol����N2H4+2HCl=N2H6Cl2
��3��90
���������
�����Ѷȣ�һ��
5������� ��7�֣��������ʵ�����Ũ��Ϊa mol/L�ı�����ȥ�ⶨV mL NaOH��Һ�����ʵ���Ũ�ȣ�����д���пհף�
��1����ʽ�ζ���������ˮϴ����װ���Һǰ��Ӧ�ý��еIJ����� ��
��2����ͼ����ʽ�ζ�����Һ���ڵζ�ǰ��Ķ�����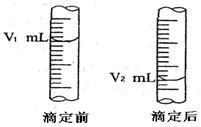
��c (NaOH) = ������ʽ����
��3�����ڵζ�ǰ�ζ��ܼ��첿���������ݣ��ζ���ζ��ܼ��첿��������ʧ����ⶨ��NaOH���ʵ���Ũ�Ȼ� �����ƫ����ƫС����Ӱ�죩
�ο��𰸣���1����ϴ��2�֣���2��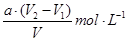 ��3�֣���3��ƫ��2�֣�
��3�֣���3��ƫ��2�֣�
�����������1����װҺ��ǰ����Ҫ��ϴ�������������ⲣ�����ϲ�����ˮӰ����Һ��Ũ�ȡ���2���������ʵ�����ʽ���м��㡣��3��������ʧ���������Ƶ��������ֵ��ʵ��ֵ����Ũ�ȼ��㹫ʽ��Ũ�ȼ���ֵƫ��
���㣺���ζ�
����������ʵ�鿼���ѶȲ������ڼ��⡣
�����Ѷȣ�һ��
| ���� �� С������ӡ�� �������� ���ر��� �����ض����� | |
| ��һƪ�����л�ѧ֪ʶ�㽲�⡶ԭ���ԭ��.. | |
| �����Ŀ |