微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 能促进水的电离,并使溶液中c(H+)>c(OH-)的操作是
①将水加热煮沸? ②向水中投入一小块金属钠?
③向水中通CO2? ④向水中通NH3? ⑤向水中加入明矾晶体?
⑥向水中加入NaHCO3固体? ⑦向水中加NaHSO4固体
A.①③⑥⑦
B.①③⑤⑥
C.⑤⑦
D.⑤
参考答案:D
本题解析:大量吸热,所以升高温度,促进电离,但纯水仍然显中性。钠溶于水生成氢氧化钠,增大OH-的浓度,抑制水的电离。同样③④⑦的水溶液均电离出氢离子或OH-,抑制水的电离。⑤⑥属于盐类的水解,促进电离,其中⑤水解显酸性,⑥水解显碱性,所以答案选D。
本题难度:简单
2、填空题 在a mL醋酸溶液中滴加0.01 mol・L-1的氢氧化钠溶液,滴定曲线如图所示。
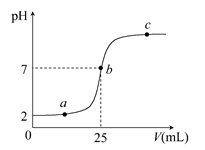
(1)醋酸溶液浓度________(填“大于”“小于”或“等于”)0.01 mol・L-1,理由是________;
(2)b点,c(Na+)________c(CH3COO-)(填“>”“<”或“=”)
(3)当醋酸与氢氧化钠溶液恰好完全中和时,曲线上对应的点Q应在____;
A.2与a之间 B.a与b之间
C.b与c之间 D.a与c之间
(4)下列关系式一定正确的是________。
A.a点,c(H+)>c(OH-)>c(CH3COO-)>c(Na+)
B.a点,c(Na+)>c(CH3COO-)>c(H+)>c(OH-)
C.c点,c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
D.c点,c(Na+)+c(H+)=c(CH3COO-)+c(OH-)
参考答案:(1)大于;CH3COOH是弱电解质,只部分电离
(2)= (3)C (4)D
本题解析:(1)开始时,醋酸溶液的pH=2,c(H+)=0.01 mol・L-1,由于醋酸是弱电解质,醋酸溶液中存在未电离的CH3COOH,故c(CH3COOH)>0.01 mol・L-1。(2)b点,pH=7表示c(H+)=c(OH-),由电荷守恒式c(Na+)+c(H+)=c(OH-)+c(CH3COO-)得出:c(Na+)=c(CH3COO-)。(3)CH3COOH+NaOH=CH3COONa+H2O,当醋酸与氢氧化钠恰好完全中和时,溶液呈碱性,pH>7,曲线上对应的Q点应在b与c之间。(4)a点,溶液的溶质是醋酸和醋酸钠,溶液显酸性,醋酸是弱酸,离子浓度大小关系为:c(CH3COO-)>c(H+)>c(OH-);无论溶液呈酸性、中性或碱性,其中都只存在Na+、H+、CH3COO-、OH-,所以一定有电荷守恒式,D选项正确。
本题难度:困难
3、选择题 水中加入下列溶液对水的电离平衡不产生影响的是
[? ]
A.NaHSO4溶液?
B.KF溶液?
C.KAl(SO4)2溶液?
D.NaI溶液
参考答案:D
本题解析:
本题难度:一般
4、实验题 (8分)某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:
①将碱式滴定管用蒸馏水洗净后,用待测溶液润洗后,再注入待测溶液,调节滴定管的尖嘴部分充满溶液,并使液面处于"0"刻度以下的位置,记下读数;将锥形瓶用蒸馏水洗净后,用待测溶液润洗锥形瓶2~3次;从碱式滴定管中放入25.00mL待测溶液到锥形瓶中。
②将酸式滴定管用蒸馏水洗净后,立即向其中注入0.1000mol/L标准盐酸,调节滴定管的尖嘴部分充满溶液,并使液面处于"0"刻度以下的位置,记下读数。
③向锥形瓶中滴入酚酞作指示剂,进行滴定。滴定至指示剂刚好变色,且并不马上变色为止,测得所耗盐酸的体积为V1mL。
④重复以上过程,但在滴定过程中向锥形瓶加入5mL的蒸馏水,测得所耗盐酸的体积为V2mL。试回答下列问题:
(1)锥形瓶中的溶液从 色变为 色时,停止滴定。
(2)滴定时边滴边摇动锥形瓶,眼睛应观察
A、滴定管内液面的变化
B、锥形瓶内溶液颜色的变化
(3)该小组在步骤①中的错误是 由此造成的测定结果 (偏高、偏低或无影响)
(4)步骤②缺少的操作是
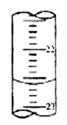
(5)下图,是某次滴定时的滴定管中的液面,其读数为 mL
(6)根据下列数据:
滴定次数
| 待测液体积(mL)
| 标准盐酸体积(mL)
|
滴定前读数(mL)
| 滴定后读数(mL)
|
第一次
| 25.00
| 0.50
| 20.40
|
第二次
| 25.00
| 4.00
| 24.10
|
请计算待测烧碱溶液的浓度(保留四位小数) mol/L
参考答案:(1)红色、无色 (2)B (3)待测液润洗锥形瓶 偏高
(4)酸式滴定管用蒸馏水洗净后,应用标准盐酸润洗2-3次
(5)22.60 (6)0.0800
本题解析::(1)标准酸滴定NaOH溶液,以酚酞作指示剂,滴定终点时,溶液的颜色由红色变为无色;
(2)滴定时边滴边摇动锥形瓶,眼睛应观察锥形瓶锥形瓶内溶液颜色的变化。
(3)装液前不能润洗;若锥形瓶用待测液润洗,待测液的物质的量偏多,造成V(酸)增大,根据c(碱)=c(酸)×V(酸)/V(碱)可知,c(碱)偏高;
(4)酸式滴定管用蒸馏水洗净后,应用标准盐酸润洗2-3次;
(5)滴定管中的液面的读数为22.60mL,故答案为:22.60;
(4)两次消耗的盐酸标准液的体积为24.90mL,25.10mL,均有效,盐酸溶液的平均体积为(24.90mL+25.10mL)/2=25.00mL,
HCl~NaOH
1 1
0.1000mol?L-1×25.00 c(烧碱)×20.00
解得c(盐酸)=0.1250mol/L,
考点:中和滴定。
本题难度:一般
5、实验题 为测定未知浓度的硫酸溶液,实验如下:用1.00mL待测硫酸配制100 mL稀H2SO4溶液;以0.14mol
/L的NaOH溶液滴定上述稀H2SO425.00mL,滴定终止时消耗NaOH溶液15.00mL。
(1)该学生用标准0.14 mol/L NaOH溶液滴定硫酸的实验操作如下:
A.用酸式滴定管取稀H2SO4 25.00 mL,注入锥形瓶中,加入指示剂。
B.用待测定的溶液润洗酸式滴定管。
C.用蒸馏水洗干净滴定管。
D.取下碱式滴定管用标准的NaOH溶液润洗后,将标准液注入碱式滴定管刻度“0”以上2~3 cm处,再