��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ��13�֣�A��B��C��D��E��F���ֻ��������A��B��C��D��E���ɶ�����Ԫ����ɣ���ɫ��Ӧ��Ϊ��ɫ��B��C��E��������Ԫ����ɡ�B��C�����Ԫ����ͬ����C��Ħ��������B��80g/mol ���ش�
��1�����廯����AΪdz��ɫ��ĩ���û������к��еĻ�ѧ��Ϊ?
A�����Ӽ�? B�����Թ��ۼ�? C���Ǽ��Թ��ۼ�? D�����
����?�±�ΪB��Fʵ��IJ�������
���ں�B����Һ�м���ϡ ������dz��ɫ���Ǻ�ʹ����ʯ��ˮ����ǵ���ɫ�д̼�����ζ������ ������dz��ɫ���Ǻ�ʹ����ʯ��ˮ����ǵ���ɫ�д̼�����ζ������
|
��20mL��ˮ�еμ�F�ı�����Һ1~2mL����Һ��ʺ��ɫ
|
�۽�ʵ��ڵõ��ĺ��ɫҺ��������������գ����յõ�����ɫ����
|
д��B��ϡ ��Ӧ�����ӷ���ʽ?
��Ӧ�����ӷ���ʽ?
д�����з�Ӧ�Ļ�ѧ����ʽ?
��3������6������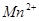 ��
�� ��
�� ��
�� ��
�� ��C�к��е������ӣ���
��C�к��е������ӣ��� ���һ�����ӷ���ʽ����֪
���һ�����ӷ���ʽ����֪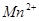 Ϊ��ԭ�����õ�1mol
Ϊ��ԭ�����õ�1mol �������������ʵ���Ϊ?mol
�������������ʵ���Ϊ?mol
��4��������D��E�ת��D E������D��E ��
E������D��E �� H2O�Ļ����13.04g�����ȵ���ȫ��Ӧ���������ͨ��ŨH2SO4����3.42g��ʣ������ͨ����ʯ������2.20g����������D������Ϊ?g��E ��
H2O�Ļ����13.04g�����ȵ���ȫ��Ӧ���������ͨ��ŨH2SO4����3.42g��ʣ������ͨ����ʯ������2.20g����������D������Ϊ?g��E ��
 �Ļ�ѧʽΪ?
�Ļ�ѧʽΪ?
�ο��𰸣���1��AC(2��)��2��S2O32- + 2H+ =" S��" + SO2 + H2O(2��)
Fe3+ + 3H2O  ?Fe(OH)3(����)+3H+(2��)
?Fe(OH)3(����)+3H+(2��)
��3��2.5(2��) ��4��8.4? (2��)? Na2CO3��7H2O(3��)
�����������1��������ɫ��֪A�ǹ������ƣ����еĻ�ѧ�������Ӽ��ͷǼ��Լ���
��2������B��ϡ���ᷴӦ�������֪��B��Na2S2O3����ӦʽΪS2O32- + 2H+ =" S��" + SO2 + H2O�����ݷ�Ӧ�ڢۿ�֪F���Ȼ�������ӦʽΪFe3+ + 3H2O  ?Fe(OH)3(����)+3H+��
?Fe(OH)3(����)+3H+��
��3�� ΪS2O82������ԭ������SO42����S�Ļ��ϼ�����1����λ��1mol��ԭ��ʧȥ5mol���ӣ����Ը��ݵ�ʧ�����غ��֪����Ҫ�����������ʵ�����2.5mol��
ΪS2O82������ԭ������SO42����S�Ļ��ϼ�����1����λ��1mol��ԭ��ʧȥ5mol���ӣ����Ը��ݵ�ʧ�����غ��֪����Ҫ�����������ʵ�����2.5mol��
��4��D��̼�����ƣ��ֽ�����CO2��H2O�Լ�̼���ơ��������ͨ��ŨH2SO4����3.42g����������ˮ��3.420g��ʣ������ͨ����ʯ������2.20g����CO2��2.20g�����ʵ�����0.05mol����̼��������0.1mol��������8.4g���ֽ����ɵ�ˮ��0.05mol��������0.9g��E �� H2O��ˮ��������2.52g�����ʵ�����0.14mol��Na2CO3��XH2O��������13.04g��8.4g��4.64g������̼���Ƶ�������4.64g��2.52g��2.12g�����ʵ�����0.02mol��������֮����1�U7�����Ի�ѧʽΪNa2CO3��7H2O��
H2O��ˮ��������2.52g�����ʵ�����0.14mol��Na2CO3��XH2O��������13.04g��8.4g��4.64g������̼���Ƶ�������4.64g��2.52g��2.12g�����ʵ�����0.02mol��������֮����1�U7�����Ի�ѧʽΪNa2CO3��7H2O��
�����Ѷȣ�һ��
2������� ��15�֣���֪A��B��C��D��E�������ڱ���ǰ�����ڵ�Ԫ�أ����ǵĺ˵�����������ӡ������Ϣ���±���ʾ�������ƶϻش��������⣺������ʱA��B��C��D��E������Ӧ��Ԫ�ط��ű�ʾ��
A
| A������������Ӧ��ˮ���ﻯѧʽΪH2AO3
|
B
| BԪ�صĵ�һ�����ܱ�ͬ������������Ԫ�ض���
|
C
| Cԭ����ͬ����ԭ���а뾶���ϡ��������⣩���䵥����ɫΪ��ɫ
|
D
| Z�Ļ�̬ԭ�����������Ų�ʽΪ3s23p2
|
E
| E��Cλ�ڲ�ͬ���ڣ�Eԭ�Ӻ���������������C��ͬ�����������Ӿ�����
|
��1��C�����ڱ���λ�ڵ����������ڵ������壬E��̬ԭ�Ӻ�������Ų�ʽ����������������
��2��A��B��D����Ԫ�ص縺���ɴ�С����˳��Ϊ��������������������A������Ȼ��ﹹ�ɾ��������������Ϊ������������������������������
��3��A��B������⻯���н��ȶ����������������ѧʽ����B������⻯���E�ĺ�ɫ����������ڼ���ʱ�ɷ�Ӧ��д���䷴Ӧ����ʽ������������������������������������
��4)E�ĵ��ʺ���������ϡ�����пɷ�Ӧ�����˽������Ӧ��Ƴ�ԭ��أ���д��������Ӧ����ʽ��������������������������������������������
��5��úȼ�ղ�������������B����������������صĻ������⣬��ˣ�����AH4����ԭ��������Ⱦ����֪��?
�� AH4(g)+2 BO2��g)�� B2(g)+AO2(g)+2H2O (g)? ��H1����867kJ��mol
�� 2BO2(g) ?B2O4(g)? ��H2=��56.9 kJ��mol
д��AH4��B2O4��Ӧ���Ȼ�ѧ����ʽ������������������������������������������������
�ο��𰸣���1������A��[Ar]3d104s1����2��N>C>Si�����Ӽ������������»�������
��3��NH3? 2NH3+3CuO 3Cu+N2+3H2O����4��H2O2+2e-+2H+=2H2O��
3Cu+N2+3H2O����4��H2O2+2e-+2H+=2H2O��
��5��CH4(g)+N2O4(g)=N2(g)+CO2(g)+2H2O(g)?��H=��810.1KJ/mol
�����������������ɵã�A��C��B��N��C��Na��D��Si��E��Cu����1��Na�����ڱ���λ�ڵ������ڵڢ�A�壻29��Ԫ��Cu��̬ԭ�Ӻ�������Ų�ʽ��1s22s22p63s23p63d104s1��[Ar]3d104s1����2��C��N��Si����Ԫ�صķǽ�����N>C>Si��Ԫ�صķǽ�����Խǿ��Ԫ�صĵ縺�Ծ�Խ�����Ԫ�صĵ縺���ɴ�С����˳��ΪN>C>Si������CԪ�ص�����Ȼ���CCl4���ɾ���ķ��Ӿ��壬���Ӽ���������Ƿ��Ӽ�������Ҳ�з��»�������3��Ԫ�صķǽ�����Խǿ�����⻯����ȶ��Ծ�Խǿ��Ԫ�صķǽ�����N>C������CH4��NH3�н��ȶ�����NH3�����ݵ����غ㼰�����غ㶨�ɿɵ�NH3��CuO�����ڼ���ʱ��Ӧ�ķ���ʽ��2NH3+3CuO 3Cu+N2+3H2O����4)Cu���ʺ���������ϡ�����пɷ�Ӧ���ɽ������Ӧ��Ƴ�ԭ��أ�������Ӧ����ʽH2O2+2e-+2H+=2H2O�������ĵ缫��ӦʽΪCu-2e-=Cu2+����5�� �٣��������ɵã�CH4(g)+N2O4(g)=N2(g)+CO2(g)+2H2O(g)?��H=��810.1KJ/mol��
3Cu+N2+3H2O����4)Cu���ʺ���������ϡ�����пɷ�Ӧ���ɽ������Ӧ��Ƴ�ԭ��أ�������Ӧ����ʽH2O2+2e-+2H+=2H2O�������ĵ缫��ӦʽΪCu-2e-=Cu2+����5�� �٣��������ɵã�CH4(g)+N2O4(g)=N2(g)+CO2(g)+2H2O(g)?��H=��810.1KJ/mol��
�����Ѷȣ�һ��
3��ѡ���� ����A��B����Ԫ�ص�ԭ�����������п������AB2�����ӻ��������
A��6��8? B��19��16? C��12��17? D��10��8
�ο��𰸣�C
���������A��Ԫ�ص�ԭ������Ϊ6��8�ķֱ��ǣ�CԪ�غ� OԪ�أ��γ�AB2�Ļ�����ΪCO2Ϊ���ۻ��������
B��Ԫ�ص�ԭ������Ϊ19��16�ķֱ��ǣ�KԪ�غ� SԪ�أ��γ�A2B�Ļ�����,����
C��Ԫ�ص�ԭ������Ϊ12��17�ķֱ��ǣ�MgԪ�غ� ClԪ�أ��γ�AB2�Ļ�����ΪMgCl2Ϊ���ӻ������ȷ��
D��Ԫ�ص�ԭ������Ϊ10��8�ķֱ��ǣ�NeԪ�غ� OԪ�أ������γɻ��������
�����Ѷȣ���
4��ѡ���� ijԪ��B�ĺ˵����ΪZ����֪Bn-��Am+�ĺ��������ͬ�ĵ��Ӳ�ṹ����AԪ�ص�ԭ��������Z��n��m����ʾ��ӦΪ��?��
A��Z+n-m
B��Z-n+m
C��Z-n-m
D��Z+m+n
�ο��𰸣�D
���������Ԫ��B�ĺ˵����ΪZ����Bn-���еĺ����������Z��n������ΪBn-��Am+�ĺ��������ͬ�ĵ��Ӳ�ṹ����˵�����߾�����ͬ�ĺ��������������AԪ�ص�ԭ��������Z+m+n����ѡD��
�����������ǻ���������Ŀ��飬��Ҫ�ǿ���ѧ�����������ͺ����������ϵ���˽����������ּ�ڹ���ѧ���Ļ���֪ʶ�����ѧ��������û���֪ʶ���ʵ�������������
�����Ѷȣ�һ��
5��ѡ���� ���š�3p��û�и�������Ϣ��
A���ܼ�
B�����Ӳ�
C�������Dz�
D���������ڿռ����չ����
�ο��𰸣�D
���������3p��ʾԭ�Ӻ����3�ܲ㣨���Ӳ㣩p�ܼ��������Dz㣩���������p���Ӧ��3����ͬ��չ����Ĺ�����ɷֱ��ʾΪpx��py��pz������û�и�������ѡD��
�����Ѷȣ���