微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (1)18g重水2H2O中含氢原子______个,含电子数为______个.
(2)在无土栽培中,配制只含0.5mol/LNH4+、0.6mol/L?Cl-、0.5mol/L?K+、______mol/L?SO42-的某营养液,若用KCl、(NH4)2?SO4、______配制1L该营养液,则需这三种固体的物质的量分别为?0.5mol、0.2mol、______mol.
2、计算题 计算题:
(Ⅰ).(6分)标准状况下,22.4LHCl气体溶于50ml水后再配成250m1溶液。
(1) 计算HCI的物质的量?
(2)计算所得盐酸的物质的量浓度?
(Ⅱ)(6分)某种待测浓度的H2SO4溶液5mL,加入10mL0.5mol/LBaCl2溶液,恰好完全反应。问得到BaSO4沉淀多少克?
3、实验题 有下列化学仪器:
①托盘天平;②玻璃棒;③药匙;④烧杯; ⑤量筒;⑥容量瓶;⑦胶头滴管;⑧细口试剂瓶;⑨标签纸。
(1)现需要配制500 mL、1 mol・L-1硫酸溶液,需用质量分数为98%、密度为1.84 g・cm-3的浓硫酸____mL。
(2)从上述仪器中,按实验使用的先后顺序,其编号排列是____ 。
(3)容量瓶使用前检验漏水的方法是____。
(4)若实验遇到下列情况,对硫酸溶液的物质的量浓度有何影响(填“偏高”“偏低”或“无影响”)。
①用以稀释浓硫酸的烧杯未洗涤____。
②未经冷却时趁热将溶液注入容量瓶中____。
③摇匀后发现液面低于刻度线再加水____。
④容量瓶中原有少量蒸馏水____。
⑤定容时俯视刻度线____。
4、选择题 在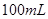
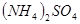 和
和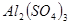 的混合溶液中,加入足量的
的混合溶液中,加入足量的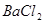 的溶液,生成
的溶液,生成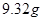 沉淀,再加入足量
沉淀,再加入足量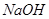 溶液并加热,生成
溶液并加热,生成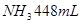 (标准状况),则原溶液中
(标准状况),则原溶液中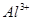 的浓度为
的浓度为
A.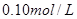
B.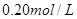
C.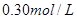
D.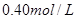
5、选择题 将0.1mol Cu与40ml 10mol/LHNO3充分反应,测得反应后的溶液里含有a molH+
由此可知?
A.生成的气体一定是NO2,在标准状况下的体积4.48 L
B.生成的气体一定是NO,在标准状况下的体积约1.49L
C.被还原的硝酸的物质的量为(0.2-a)mol
D.反应后的溶液里含有0.2mol NO3-