��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ij�о�С��ͨ��ʵ��̽��Cu���仯��������ʣ����в�����ȷ���ܴﵽĿ�ĵ���
A����ͭ˿����Ũ�����м��ȣ���Ӧ���ˮ���뷴Ӧ���У��۲�����ͭ��Һ����ɫ
B�������½�ͭ˿����ʢ�������ļ���ƿ�У��۲�CuCl2������
C����CuCl2��Һ���������м������ɣ��õ���ˮCuCl2����
D����������ͭ��[Cu2(OH)2CO3]��ͭ�����������н��ݣ���ȥͭ��
�ο��𰸣�D
���������A����ȷ�IJ���Ӧ�ý�ͭ˿����Ũ�����м��ȣ���Ӧ��ȡһ�����ķ�ӦҺ����ʢ��ˮ���ձ��У�B��Ӧ���ú��ȵ�ͭ˿��Cu2��ˮ�⣬����CuCl2��Һ���ܵõ�CuCl2���壬C����ͭ�����������ͭ���������ᣬ�ʿ��������ȥͭ�������ͭ�̣�D��ȷ��
�����Ѷȣ�һ��
2�������
(1)д��Cu��ȡCuSO4(ϡH2SO4������)�ķ���ʽ________________��
(2)Cu��ŨH2SO4����Ҳ����ȡCuSO4���䷴Ӧ����ʽΪ��________________������������ȡ����________________�ߺ�(�ǰ����)��ԭ����________________��
�ο��𰸣�(1)2H2SO4��O2��2Cu 2CuSO4��2H2O
2CuSO4��2H2O
(2)2H2SO4(Ũ)��Cu CuSO4��SO2����2H2O?ǰ?��ʡ��������������Ⱦ���ŷ�
CuSO4��SO2����2H2O?ǰ?��ʡ��������������Ⱦ���ŷ�
����������ڼ��������£�Cu��O2����ת��ΪCuO��CuO������ϡH2SO4����CuSO4��H2O��
�����Ѷȣ���
3��ѡ���� ���������۷���FeCl3��Һ�У���ȫ��Ӧ����Һ�е�Fe2+��Fe3+�ܶ���ȣ����ѷ�Ӧ��Fe3+��δ��Ӧ��Fe3+�����ʵ���֮����
A��2 ��3
B��3 ��2
C��1 ��2
D��1 ��1
�ο��𰸣�A
����������ѷ�Ӧ��Fe3+��δ��Ӧ��Fe3+�����ʵ����ֱ���x��y������ݷ���ʽ��֪
2Fe3����Fe��3Fe2��
2mol? 1mol 3mol
x? 1.5x
����y��1.5x
���x�Uy��2 ��3
��ѡA
�����������ǻ���������Ŀ��飬�ѶȲ�����Ҫ�ǿ���ѧ��������û���֪ʶ�������������������dz����Լ�����Ŀ��飬ֱ�Ӹ��ݷ���ʽ��ʽ���㼴�ɡ�
�����Ѷȣ�һ��
4��ʵ���� ��6�֣��ڿ�չ�о���ѧϰ��У�ij�о�С���ͬѧ���������3��ʵ��װ�ã������ռ�����֤���ڸ�������ˮ������Ӧ��������
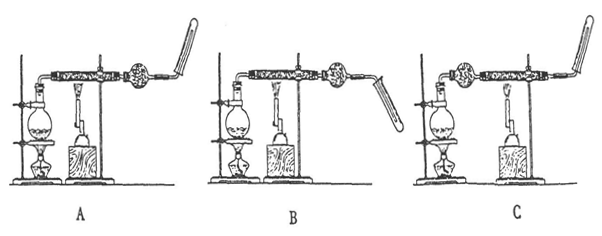 ��1����ָ������ȷ�ó�ʵ����۵�װ��(��"A"��"B"��"C")?��
��1����ָ������ȷ�ó�ʵ����۵�װ��(��"A"��"B"��"C")?��
��2��д�����ڸ�������ˮ������Ӧ�Ļ�ѧ����ʽ?��
��3�������ü��������ռ��������壬������������ķ���������?��
�ο��𰸣�A? 3Fe +4H2O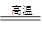 Fe3O4+4H2?�����ſ������ռ���ȼ�б�����
Fe3O4+4H2?�����ſ������ռ���ȼ�б�����
�����������1��ˮ���������۸������ڲ������з�Ӧ�����ų�C������ܽ�ˮ���գ����������ܶȽ�С���ų�B���ռ�����Ӧ�������ſ�����������A
��2��3Fe +4H2O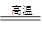 Fe3O4+4H2
Fe3O4+4H2
��3���ɲ�����������������ˮ���������ռ����������ǰ�߽ϼ�
�����ļ���һ��ɽ����ȼ��������ˮ����ͭ����ˮ�����ɣ�������ɽ����ȼ���������������ɣ�
�����Ѷȣ�һ��
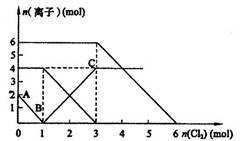
5�������� ��7�֣���FeI2��FeBr2�Ļ����Һ��ͨ��������������Һ��ijЩ���ӵ����ʵ����仯��ͼ��ʾ��
��֪��2Fe2++Br2 2Fe3++2Br��?2Fe3++2I��
2Fe3++2Br��?2Fe3++2I�� 2Fe2++I2
2Fe2++I2
��1��Fe2+��I����Br���Ļ�ԭ����ǿ��������˳��Ϊ������������������
��2����ͨ��2mol Cl2ʱ����Һ���ѷ��������ӷ�Ӧ�ɱ�ʾΪ������������������������
��3��ԭ�����Һ��FeBr2�����ʵ���Ϊ������������������
��4��ԭ��Һ�У�n(Fe2+):n(I��):n(Br��)������������������
�ο��𰸣���7�֣���1��I����Fe2+��Br����2��2Fe2++2I��+2Cl2 2Fe3++I2+4Cl��
2Fe3++I2+4Cl��
��3��3mol?��4��2:1:3
�����������1�����ݻ�ԭ���Ļ�ԭ��ǿ�ڻ�ԭ����Ļ�ԭ�ԣ��ɷ���ʽ2Fe2++Br2 2Fe3++2Br��?2Fe3++2I��
2Fe3++2Br��?2Fe3++2I�� 2Fe2++I2��֪��Fe2+��I����Br���Ļ�ԭ����ǿ��������˳��ΪI����Fe2+��Br��
2Fe2++I2��֪��Fe2+��I����Br���Ļ�ԭ����ǿ��������˳��ΪI����Fe2+��Br��
��2����ͼ���֪����ͨ���0mol<n��Cl2��<1molʱ��������Ӧ��2Fe3++2I�� 2Fe2++I2��I�������ʵ�����2mol����0mol����Һ��I��Ϊ2mol��FeI2Ϊ1mol��
2Fe2++I2��I�������ʵ�����2mol����0mol����Һ��I��Ϊ2mol��FeI2Ϊ1mol��
��ͨ���1mol<n��Cl2��<3molʱ��������Ӧ��2Fe2++Cl2 2Fe3++2Cl����Fe2+�����ʵ�����4mol����0mol����Һ��FeBr2Ϊ4��1=3mol��Br��Ϊ6mol��
2Fe3++2Cl����Fe2+�����ʵ�����4mol����0mol����Һ��FeBr2Ϊ4��1=3mol��Br��Ϊ6mol��
������֪����ͨ���3mol<n��Cl2��<6molʱ��������Ӧ��2Br��+Cl2 Br2+2Cl��
Br2+2Cl��
��ͨ��2mol Cl2ʱ���ɵ��ӵĵ�ʧ�غ��֪���μӷ�Ӧ��I��Ϊ2mol��Fe2+Ϊ2mol�����ӷ�ӦʽΪ��2Fe2++2I��+2Cl2 2Fe3++I2+4Cl��
2Fe3++I2+4Cl��
��3��ԭ�����Һ��FeBr2�����ʵ���Ϊ3mol
��4��ԭ��Һ�У�n(Fe2+):n(I��):n(Br��)��4��2��6=2:1:3
�����Ѷȣ�һ��