微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列实验方案设计中,可行的是
A.加稀盐酸后过滤,除去混在铜粉中的少量镁粉和铝粉
B.用萃取的方法分离汽油和煤油
C.用溶解、过滤的方法分离KNO3和NaCl固体的混合物
D.将O2和H2的混合气体通过灼热的氧化铜,以除去其中的H2
参考答案:A
本题解析:A 正确,盐酸和镁粉和铝粉反应,和铜粉不反应,所以,加稀盐酸后过滤可除去铜粉中的镁、铁杂质。
B 错误,用蒸馏的方法分离汽油和煤油
C 错误,用冷却热饱和溶液的方法,过滤的硝酸钾固体,在蒸发滤液得到氯化钠固体,进而分离KNO3和NaCl固体的混合物
D 错误,将O2和H2的混合气体通过灼热的氧化铜,会发生爆炸。
本题难度:简单
2、实验题 学习卤代烃性质时,我们知道溴乙烷在不同溶剂中与氢氧化钠发生不同类型的反应,生成不同的反应产物。我们可以通过实验的方法去验证反应的产物:
(1)在溴乙烷与氢氧化钠的乙醇溶液的__________(反应类型)中可以观察到有气体生成。某同学用如下图所示装置对该气体进行验证,他所观察到的现象是_________________________;
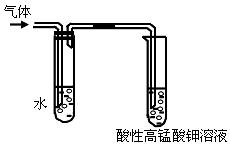
(2)盛水试管的作用是______________________;
(3)除了用酸性高锰酸钾溶液外,还可以用_________试剂检验该气体,其反应原理是_________________________(用化学方程式表示)。
(4)另一位同学取少量溴乙烷与氢氧化钠水溶液反应后的混合溶液,向其中滴加硝酸银溶液,加热,产生少量沉淀。该同学由此得出溴乙烷与氢氧化钠水溶液反应,生成了溴化钠。老师和同学都认为这样不合理。若请你用实验验证该反应中生成了溴化钠,你与该同学实验方案不同的实验方法是___________________________________。
参考答案:(1)消去反应;高锰酸钾褪色
(2)除去气体中少量的乙醇
(3)溴水;CH2=CH2+ Br2→BrCH2CH2Br
(4)将混合溶液先用稀硝酸酸化,再向溴乙烷中加硝酸银溶液
本题解析:
本题难度:一般
3、实验题 资料显示:“氨气可在纯氧中安静燃烧……”。某校化学小组学生设计如下装置(图中铁夹等夹持装置已略去)进行氨气与氧气在不同条件下反应的实验。
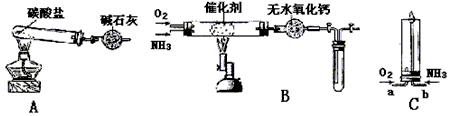
(1)用装置A制取纯净、干燥的氨气,大试管内碳酸盐的化学式是 ________;碱石灰的作用是 _____________。
(2)将产生的氨气与过量的氧气通到装置B(催化剂为铂石棉)中,用酒精喷灯加热:
①氨催化氧化的化学方程式是______________ ;试管内气体变为红棕色,该反应的化学方程式是________________ ;
②停止反应后,立即关闭B中两个活塞。一段时间后,将试管浸入冰水中,试管内气体颜色变浅,请结合化学方程式说明原因 ___________________。
(3)将过量的氧气与A产生的氨气分别从a、b两管进气口通入到装置C中,并在b管上端点燃氨气:
①两气体通入的先后顺序是 ________________。 其理由是__________________。
②氨气燃烧的化学方程式是_______________________ 。
参考答案:
(1)①(NH4)2CO3[或NH4HCO3];
②吸收水和二氧化碳
(2)①4NH3+5O2 4NO+6H2O? ;2NO+O2====2NO2? ;、
4NO+6H2O? ;2NO+O2====2NO2? ;、
②2NO2(气)  N2O4(气)+热量,降低温度使平衡正向移动,部分红棕色NO2转化为无色N2O4。
N2O4(气)+热量,降低温度使平衡正向移动,部分红棕色NO2转化为无色N2O4。
(3)①先通入O2,后通入NH3;若先通氨气,氨在空气中不能点燃,逸出造成污染;
②4NH3+3O2  2N2+6H2O
2N2+6H2O
本题解析:
本题难度:一般
4、实验题 (8分)为了测定Na2CO3与Na2SO3混合物中各组分的含量,取样品23.2g以下图所示装置(铁架台、铁夹等仪器未在图中画出)进行实验:
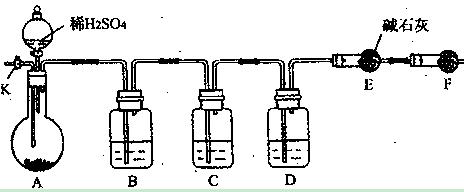
(1)将仪器连接好以后,必须进行的第一步操作是?;
(2)装置B的作用是? ;
;
(3)已知装置C中装有品红溶液, 其作用是?;
其作用是?;
(4)实验室中备有以下常用试剂:a.浓硫酸? b. 品红溶液? c. 酸性高锰酸钾溶液
d. 饱和碳酸氢钠溶液? e. 氢氧化钠溶液? f. 无水硫酸铜? g. 碱石灰
请将下列装置中应盛放的试剂的序号填在横线上:
B中应盛放?,D中应盛放?,F中应盛放?;
(5)若装置E在实验完成时增重4.4g,则Na2CO3与Na2SO3的物质的量之比为?。
参考答案:(第五小问2分,其余每空1分,共8分)
(1)检验装置的气密性
(2)除去二氧化碳中的二氧化硫气体
(3)检验二氧化硫是否已除尽
(4)B中:e? D中:a? F中g
(5)1:1
本题解析:略
本题难度:简单
5、实验题 (13分)硫代硫酸钠是一种重要的化工产品。某兴趣小组拟制备硫代硫酸钠晶体(Na2S2O3・5H2O)。
I.[查阅资料]
(1)Na2S2O3・5H2O是无色透明晶体,易溶于水。其稀溶液与BaCl2溶液混合无沉淀生成。
(2)向Na2CO3和Na2S混合液中通入SO2可制得Na2S2O3,所得产品中常含有少量Na2SO3和Na2SO4。
(3)Na2SO3易被氧化;BaSO3难溶于水,可溶于稀HCl。
Ⅱ.[制备产品]
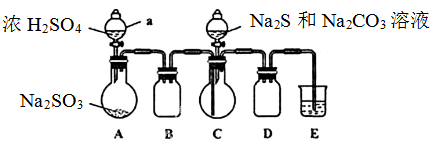
实验装置如图所示(省略夹持装置)
实验步骤:
(1)检查装置气密性,按图示加入试剂。仪器a的名称是____;E中的试剂是___(选填下列字母编号)。
A.稀H2SO4? B.NaOH溶液? C.饱和NaHSO3溶液
(2)先向C中烧瓶加入Na2S和Na2CO3混合溶液,再向A中烧瓶滴加浓H2SO4。
(3)待Na2S和Na2CO3完全消耗后,结束反应。过滤C中混合液,滤液经____(填写操作名称)、结晶、过滤、洗涤、干燥、得到产品。
Ⅲ.[探究与反思]
(1)为验证产品中含有Na2SO3和Na2SO4,该小组设计了以下实验方案,请将方案补充完整。(所需试剂从稀HNO3、稀H2SO4、稀HCl、蒸馏水中选择)
取适量产品配成稀溶液,滴加足量BaCl2溶液,有白色沉淀生成,_____,若沉淀未完全溶解,并有刺激性气味的气体产生,则可确定产品中含有Na2SO3和Na2SO4。
(2)为减少装置C中生成的Na2SO4的量,在不改变原有装置的基础上对原有实验步骤(2)进行了改进,改进后的操作是_______。
(3)Na2S2O3・5H2O的溶解度随温度升高显著来源:91考试网 91ExaM.org增大,所得产品通过_____方法提纯。
参考答案:Ⅱ.(1)分液漏斗;B?(3)蒸发
Ⅲ. (1)过滤,用蒸馏水洗涤沉淀,向沉淀中加入足量稀HCl。
(2)先向A中烧瓶滴加浓硫酸,产生的气体将装置中空气排尽后,再向C中烧瓶加入Na2S和Na2CO3混合溶液。(3)重结晶
本题解析:Ⅱ.[制备产品]
(1)根据仪器的构造特点可知,仪器a的名称是分液漏斗。根据装置可知,A装置是制备SO2的,C装置是制备得Na2S2O3,BD装置是防倒吸的,由于SO2有毒,需要尾气处理,因此E装置是吸收SO2的。由于SO2是酸性氧化物,可以用氢氧化钠溶液吸收,即E中的试剂是氢氧化钠溶液,答案选B。
(3)由于Na2S2O3・5H2O是无色透明晶体,易溶于水,因此要从溶液中得到硫代硫酸钠晶体,责问需要经过蒸发浓缩、冷却结晶、过滤、洗涤、干燥、得到产品。
Ⅲ.[探究与反思]
(1)Na2S2O3・5H2O的稀溶液与BaCl2溶液混合无沉淀生成,而实验过程中有白色沉淀生成,因此要进一步验证,则可以向白色沉淀中滴加稀盐酸,若沉淀未完全溶解,并有刺激性气味的气体产生,则可确定产品中含有Na2SO3和Na2SO4。
(2)由于亚硫酸盐易被氧化生成硫酸盐,而装置中含有空气,空气能氧化亚硫酸盐,所以为减少装置C中生成的Na2SO4的量,改进后的措施是先向A中烧瓶滴加浓硫酸,产生的气体将装置中空气排尽后,再向C中烧瓶加入Na2S和Na2CO3混合溶液。
(3)由于Na2S2O3・5H2O的溶解度随温度升高显著增大,因此所得产品通过重结晶方法提纯。
本题难度:一般