|
���л�ѧ֪ʶ�㽲�⡶�����йص����ӷ���ʽ����д����Ƶ����̣�2017�����°棩(��)
2017-08-01 01:18:08
��Դ:91������
����:www.91exam.org �� �� �� ��
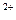 +2OH +2OH +SO +SO +2H +2H  BaSO BaSO ��+2H ��+2H O O
�ο��𰸣�D
���������Aѡ��̼����dz������û�ѧʽ��ʾ��Bѡ����Ͽ���ʵ��Cѡ��HCO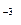 ���ܲ�д��Dѡ���� Ba��OH�� ���ܲ�д��Dѡ���� Ba��OH�� ��H ��H SO SO ���ǿ�����ˮ��ǿ����ʣ�BaSO ���ǿ�����ˮ��ǿ����ʣ�BaSO ���ܣ�H ���ܣ�H O�ѵ��롣 O�ѵ��롣
�����Ѷȣ�һ��
2������� ��1���û�ѧ����ʽ��ʾSO2�γ�����������ķ�Ӧ��______��
��2��Ϊ��֤���������к�����Ԫ�أ����в�������ȷ˳����______������ţ���
�ٵμ�AgNO3��Һ?�ڳ��������?��ȡ�ϲ�ˮ��Һ?�ܼ���5%��NaOH��Һ�ݵμӹ���ϡHNO3���μ�AgNO3��Һʱ������Ӧ�����ӷ���ʽ��______��
��3�����������Ҫ�ɷ�ΪFeCO3����FeSO4��Һ���Թ�����NH4HCO3��Һ��ϣ��õ���FeCO3����Һ��д����һ�仯���̵����ӷ���ʽ______��
�ο��𰸣���1��������������γ��з���SO2+H2O

H2SO3��2H2SO3+O2�T2H2SO4��
�ʴ�Ϊ��SO2+H2O

H2SO3��2H2SO3+O2�T2H2SO4��
��2��֤���������к�����Ԫ�أ�Ӧ�ȷ���ˮ����������ӣ����������кͣ����������ữ��������������ȷ��˳���Ǣܢڢۢݢ٣�
�μ�AgNO3��Һ���������ӷ���ʽΪAg++Br-=AgBr�����ʴ�Ϊ���ܢڢۢݢ٣�Ag++Br-=AgBr����
��3��FeSO4��Һ���Թ�����NH4HCO3��Һ��ϣ��õ���FeCO3����Һ����Ӧ��ΪFeSO4��NH4HCO3��
������ΪFeCO3��CO2��H2O���÷�Ӧ�����ӷ���ʽΪFe2++2HCO3-=FeCO3+CO2��+H2O��
�ʴ�Ϊ��Fe2++2HCO3-=FeCO3+CO2��+H2O��
���������
�����Ѷȣ�һ��
3��ѡ���� �������ʷ�����Ӧʱ�����ӷ���ʽ����ȷ����
A���������Ȼ�����Һ��Ӧ��Fe+2Fe3+��3Fe2+[
B������������ͨ���廯������Һ�У�2Fe2++4Br-+3Cl2��2Fe3++2Br2+6Cl-
C��Fe(OH)3�����ᷴӦ��Fe(OH)3+3H+��Fe3++3H2O
D��FeS��ϡ���ᷴӦ��FeS+2H+��Fe2++H2S��
�ο��𰸣�D
�����������
�����Ѷȣ���
4��ѡ���� ���з�Ӧ�����ӷ���ʽ��ȷ����
A����0.1mol��L-1��NH4Al(SO4)2��Һ��0.2mol��L-1��Ba(OH)2��Һ�������ϣ�
Al3����2SO42����2Ba2����4OH����AlO2������2BaSO4��+2H2O
B��Ca(HCO3)2��Һ��������NaOH��Һ��Ӧ��
Ca2�� �� 2HCO3�� ��2OH�� = CaCO3���� CO32�� �� 2H2O
C����NaClO��Һ��ͨ�����������̼�����ӷ���ʽ:
2ClO��+CO2+ H2O
D��������ˮ��Ӧ��Cl2+H2O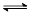 H++Cl��+HclO H++Cl��+HclO
�ο��𰸣�D
���������
A��NH4Al(SO4)2��Һ��Ba(OH)2��Һ1��2��Ӧ��©����NH4+��OH���ķ�Ӧ��
NH4++Al3����2SO42����2Ba2����4OH����Al��OH)3����2BaSO4��+NH3.H2O
B�� Ca(HCO3)2��Һ��������NaOH��Һ��Ӧ��˭�ٶ�˭Ϊ1��
Ca2�� �� HCO3�� ��OH�� = CaCO3���� 2H2O
C����NaClO��Һ��ͨ�����������̼����HCO3-��
ClO��+CO2+ H2O =? HClO+HCO3��
�����Ѷȣ���
5��ѡ���� ���з�Ӧ�У��������ӷ���ʽH++OH-===H2O��ʾ����
[? ]
A��NH4Cl+NaOH  NaCl+NH3��+H2O NaCl+NH3��+H2O
B��Mg(OH)2+2HCl===MgCl2+2H2O
C��NaOH+NaHCO3===Na2CO3+H2O
D��NaOH+HNO3===NaNO3+H2O
�ο��𰸣�D
���������
�����Ѷȣ���
| 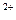 +2OH
+2OH +SO
+SO +2H
+2H
 BaSO
BaSO ��+2H
��+2H O
O NaCl+NH3��+H2O
NaCl+NH3��+H2O