��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� �� I��ij��ɫϡ��ҺX�У����ܺ����±����������е�ij���֣�
| ������ | CO32-��SiO32-��AlO2-��Cl-
������
Al3+��Cu2+��Mg2+��NH4+��Na+
|
��ȡ����Һ�����������м���ij�Լ�Y���������������ʵ�����n��������Լ�Y�����V���Ĺ�ϵ��ͼ��ʾ��
��1����Y�����ᣬ����Һ�к��еĽ�����������______��ab�η�����Ӧ�������ӷ���ʽΪ______��Oa���ϱ��вμӷ�Ӧ�����ӵ����ʵ���֮��Ϊ��______[Ҫ�������ӷ��ţ���n��Na+��]��
��2����Y��NaOH��Һ����bc�η�Ӧ�����ӷ���ʽΪ______�������������ӵ�ˮ�����أ�����H+��OH-Ӱ�죬����Һ��ֻ�����������ӣ������ǵ����Ӹ�����Ϊ______[����������ǰ���������ں���ǰ���ͼ��ں��˳������]��
�� II����Ϊ��IVA��Ԫ�أ����ĵ��ʺͻ�������ijЩ���ʵĻ�ѧ����������������֮������֪��Ԫ�ؾ����������ʣ���Sn4++Sn�T2Sn2+����2Sn2++O2+4H+�T2Sn4++2H2O����2H++SnO22-?Sn��OH��2?Sn2++2OH-���Իش�
��1�����������ᣬ����Ӧ�����Һ��ͨ���������йط�Ӧ������������Ӧ�仯����д���йط�Ӧ�Ļ�ѧ����ʽ��______��______��
��2������1������Һ���ɺ�����������ù��壬�仯����������FeCl3��Һ��Ӧ�ı仯�������õ��Ĺ��������ǣ�����ʽ��______��
��3��������SnCl2��Һ������ļ���Һ��Ӧ�ķ�����Sn��OH��2���ü���______��

2������� A��Z��R��D��E��F��G������ԭ���������������Ҳ�����20��Ԫ�أ����������ַǽ���Ԫ��λ��ͬһ���壮��֪A��Z��D������R�γ�ԭ�ӣ������ӣ�������ͬ�Ķ��ֳ����������ش������й����⣮
��1����X��Y��D��F�γɵ�����������Ӧ��ˮ���Ũ�Ⱦ�Ϊ0.1mol/L��X��Y��Һ��pH֮��Ϊ14����X��Y�ľ����۵���Ըߵ�Ϊ��д��ѧʽ��______���������ֲ�����ڵ�ԭ����______����ͬ�¶��£�������ʵ���Ũ�ȵ�X��Y���Ե���Һ�У���ˮ�������c��H+������Դ�С��ϵΪ______��
��2��A��Z��E�����γ��������幹�͵���̬����Q��P����֪P��ȼ����Ϊ1430kJ/mol������ȼ�յ��Ȼ�ѧ����ʽ______��
��3��R��D��F�䣻R��F��G������γɶ��ֻ����������������Ŀǰ�㷺ʹ�õľ�������ɱ�������Ļ��������ͬ���ʵ���Ũ�ȵ����������ʵ���Һ������ɱ��������ǿ�����ʵĻ�ѧʽΪ______����һ�����ʵ���Һ�У�������Ũ���ɴ�С��˳��Ϊ______��
��4����������Ԫ�ؼ����γɶ��ֳ�����Ԫ���������Z��G�γɵ�һ�ֻ�����������ѧ������������HC1��Һ�Ļ�ѧ��Ӧ����ʽΪ______��ZR2�ĵ���ʽ��______���÷��ӵĿռ乹��Ϊ______������ZRF2�ĽṹʽΪ______
��5��R���γɶ��ֵ��ʣ���R2��R3���о��������½��Ƶõ�һ�����ΪR4�ķ����У�ÿ��Rԭ�Ӿ�����������Rԭ�Ӹ��γ�һ��������1molR4�й��õ��Ӷ���Ϊ______NA�����й�R4��˵������ȷ����______
��R4��R3��R2��Ϊͬλ��
��R4������A��Z��D�ĵ��ʷ�Ӧ
��R4�и�ԭ��������Ϊ8���ӽṹ
��R4��1�����ͻ����
3������� ��֪��������A�������������������Ľ�����D��������ˮ�İ�ɫ���壮FΪ���ɫ���壮��ɫ�������������������ɺ���ɫ�������ң�ͼ�в��ֲ���ͷ�Ӧ�������ԣ���
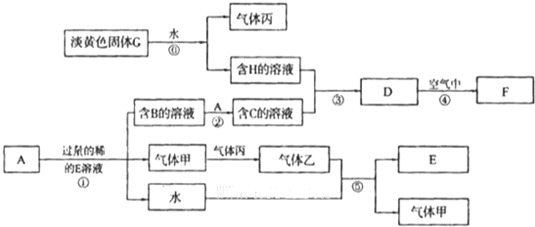
�����������Ϣ�ش��������⣺
��1��д���������ʵĻ�ѧʽC______G______��
��2��д����Ӧ�ٵĻ�ѧ����ʽ______����Ӧ�ڵ����ӷ���ʽ______��
��3����Ӧ���������̹۲쵽������Ϊ______��
��4����Ӧ���У��������������ҵ��Թܵ�����ˮ���У���ַ�Ӧ���Թ���Һ��ռ�Թ������______��
��5��ij��ƶѪ֢����Ӧ����C���ʵ������ӣ��������ӵ�ҩƬ�������һ����������£�������µ����þ��DZ��������Ӳ��������е�����������Ϊ���鳤�ڷ��õ�ҩƬ�Ѿ�ʧЧ����ҩƬȥ�����º����飬ȡ���������ҩƬ�����ձ��У�������������ˮ��Ȼ��μ�����______��Һ����Һ��______ɫ��������ҩƬ��ʧЧ��
4���ƶ��� ��10�֣�A��J����ѧ��ѧ���������ʣ�����֮���ת����ϵ����ͼ��ʾ�����ֲ�������ȥ������֪A��һ�ָ��۵����ʣ�D��һ�ֺ���ɫ���塣
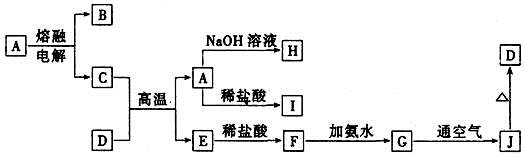
��ش��������⣺�����ƶ����ҵ�ͻ�Ƶ��ǹؼ���A��һ�ָ��۵����ʣ���֪AΪAl2O3��D��һ�ֺ���ɫ���壬��֪DΪFe2O3��BΪO2��CΪAl,EΪFe,FΪFeCl2,GΪFe(OH)2,JΪFe(OH)3��HΪNaAlO2��IΪAlCl3��
��1�����A���ʵ������缫��ӦʽΪ___________��C��D�ڸ����·�Ӧ�������÷�Ӧ��Ҫ�����һ���Լ���____________________(д��ѧʽ)
��2��д��G��J��Ӧ��ʵ�������뻯ѧ����ʽ____________________________________��__________________________________
��3��H ��I��Ӧ�����ӷ���ʽΪ___________________________________________
��4�������ӷ���ʽ��ʾI���������ھ�ˮ��ԭ��___________________________________
5��ѡ���� �ɶ�����Ԫ����ɵ���ѧ��������A��B��C��D��E��X������ ��ͼת����ϵ������������ͷ�Ӧ������ȥ���������ƶϲ���ȷ����
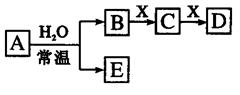
A.��X��Na2CO3��CΪCO2����Aһ������������D��E����Ӧ
B.��A�ǵ��ʣ�B��D�ķ�Ӧ��OH-+HCO3- =H2O+ CO32-����Eһ���ܻ�ԭFe2O3
C.��DΪCO��C�ܺ�E��Ӧ����Aһ��ΪNa2O2
D.��DΪ��ɫ��������AĦ��������ȣ���Xһ��������