微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 在给定的四种溶液中,加入以下各种离子,各离子能在原溶液中大量共存的是
A.滴加酚酞试液显红色的溶液Fe3+、NH4+、Cl-、SCN-
B.水电离出来的c(H+)=10-13mol/L的溶液K+、HCO3-、Br-、Ba2+
C.所含溶质为Na2SO4的溶液K+、CO32-、NO3-、Ca2+
D.pH=1的溶液Cu2+、Na+、Mg2+、NO3-
参考答案:D
本题解析:分析:A.滴加酚酞试液显红色的溶液呈碱性,溶液中存在大量的OH-离子;
B.水电离出来的c(H+)=10-13mol/L的溶液可能呈酸性,也可能呈碱性;
C.所含溶质为Na2SO4的溶液中,与SO42-反应生成沉淀的离子不能存在,
D.pH=1的溶液呈酸性,溶液中存在大量的H+离子.
解答:A.滴加酚酞试液显红色的溶液呈碱性,溶液中存在大量的OH-离子,Fe3+与OH-或SCN-都不能大量共存,故A错误;
B.水电离出来的c(H+)=10-13mol/L的溶液可能呈酸性,也可能呈碱性,无论溶液呈酸性还是碱性,HCO3-都不能存在,故B错误;
C.所含溶质为Na2SO4的溶液中,与SO42-反应生成沉淀的Ca2+离子不能存在,故C错误;
D.pH=1的溶液呈酸性,溶液中存在大量的H+离子,在酸性条件下,四种离子不发生任何反应,能大量共存,故D正确.
故选D.
点评:本题考查离子共存,题目信息量较大,难度中等,解答本题时要注意把握各项前提条件,熟练掌握离子的性质.
本题难度:一般
2、选择题 向酚酞试液中加入过量Na2O2粉末,振荡,下列叙述正确的是
A.溶液最后变成红色
B.溶液最后褪色
C.无气体生成
D.无明显现象
参考答案:B
本题解析:分析:根据Na2O2粉末能与水反应产生氢氧化钠和氧气,碱能使酚酞变红,过氧化钠具强氧化性,有漂白作用,能将变红的酚酞褪色.
解答:Na2O2和水反应生成NaOH和氧气,使酚酞变红,但Na2O2有强氧化性,将变红的酚酞氧化变为无色,所以溶液先变红后褪色,有气体生成.
故选B.
点评:本题考查了过氧化钠性质的运用,培养了学生分析问题和解决问题的能力.
本题难度:一般
3、选择题 氧化铝是铝土矿的主要成分.氧化铝属于
A.碱性氧化物
B.酸性氧化物
C.两性氧化物
D.混合物
参考答案:C
本题解析:分析:根据碱性氧化物酸性氧化物以及两性氧化物的概念结合氧化铝的性质来回答分析.
解答:A、碱性氧化物是能和酸反应生成盐和水的氧化物,氧化铝不但可以和碱反应还可以和酸反应均生成盐和水,故A错误;
B、酸性氧化物是能和碱反应生成盐和水的氧化物,氧化铝不但可以和酸反应还可以和碱反应均生成盐和水,故B错误;
C、氧化铝不但可以和酸反应还可以和碱反应均生成盐和水,属于两性氧化物,故C正确;
D、氧化铝是含有氧元素和氯元素的纯净物,故D错误.
故选C.
点评:本题考查学生常见物质的概念,注意氧化铝是两性氧化物这一结论,要求平时注意知识的灵活应用,难度不大.
本题难度:一般
4、选择题 将足量的铜与一定体积?10mol?L-1的浓硝酸充分反应,得到Cu(NO3)2溶液和NO2、NO混合气体,将集满混合气体的容器倒扣在水中,通入2.24L?O2(标准状况)后,所有气体完全被水吸收生成硝酸.发生反应为:4NO2+O2+2H2O=4HNO3;4NO+3O2+2H2O=4HNO3.若向所得Cu(NO3)2溶液中加入5mol?L-1NaOH溶液使Cu2+恰好完全沉淀,则消耗NaOH溶液的体积是
A.40?mL
B.60?mL
C.80?mL
D.100?mL
参考答案:C
本题解析:分析:整个过程中HNO3 反应前后没有变化,即Cu失去的电子都被O2得到了,根据电子得失守恒,求出参加反应的铜,然后求出 Cu(NO3)2,再根据 Cu(NO3)2与NaOH 反应的关系,求出NaOH的物质的量,进而计算NaOH溶液的体积.
解答:完全生成HNO3,则整个过程中HNO3 反应前后没有变化,即Cu失去的电子都被O2得到了,
根据得失电子守恒:n(Cu)×2=n(O2)×4,即n(Cu)×2=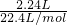 mol×4,
mol×4,
解得n(Cu)=0.2mol,所以Cu(NO3)2 =0.2mol,则:
?Cu2+~2OH-
? ?1? ?2
?0.2mol? n(OH-)
所以n(OH-)=0.2mol×2=0.4mol
需要NaOH溶液的体积为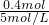 =0.08L=80mL,
=0.08L=80mL,
故选C.
点评:本题考查混合物计算、氧化还原反应计算等,难度较大,利用常规方无法解答,是守恒思想在混合计算典型利用,判断金属失去的电子等于氧气获得的电子是关键.
本题难度:简单
5、选择题 常温下,能被浓硝酸钝化的金属是
A.Mg
B.Fe
C.Cu
D.Al
参考答案:BD
本题解析:试题分析:常温下,能被浓硝酸钝化的金属是铁和铝,答案选BD。
考点:考查钝化的有关判断
点评:该题是基础性试题的考查,难度不大,有助于调动学生的学习兴趣和学习积极性,记住即可。
本题难度:一般