��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ij��ɫ��Һ��Na+��Ag+��Ba2+��Al3+��Fe3+��AlO2-��MnO4-��CO2-3��SO42-�е���������ɣ�ȡ����Һ��������ʵ�飺
��A��ȡ��Һ�������������ϡ���ᣬ���������ɣ��õ���Һ�ף�
��B������Һ�����ټ������̼�������Һ�����������ɣ�������ɫ�����ң��õ���Һ����
��C������Һ���м������Ba��OH��2��Һ�����������ɣ�������ɫ��������
��������ʵ��ش��������⣺
��1����Һ��һ�������ڵ�������______��
��2��һ�����ڵ�������______��
��3�����ɳ����ҵ����ӷ�Ӧ����ʽ��______��
�ο��𰸣���1��ȡ��Һ�������������ϡ���ᣬ���������ɣ�����Һ�к�������CO32-����һ������Ag+��Ba2+��Al3+��
Fe3+����Щ������CO32-���ӷ�Ӧ���ɳ��������ܴ������棬������Һ�ĵ����ԣ���Һ��һ������Na+���ӣ�
��Һ��ɫ����MnO4-���ʴ�Ϊ��Ag+��Ba2+��Al3+��Fe3+��MnO4-��
��2�����ݣ�1���ķ����ͽ����Һ�к���CO32-��Na+���ӣ���Һ�׳����ԣ��ټ������̼�������Һ�����������ɣ�������ɫ������Ӧ�Ƿ�����Al3++3HCO3-=Al��OH��3��+3CO2��������Ӧ����Al3+���ӣ���ԭ��Һ��Ӧ����AlO2-���ӣ��ʴ�Ϊ��Na+��AlO2-��CO32-��
��3��Al3+����ˮ������ԣ�HCO3-����ˮ��ʼ��ԣ����߷�����ٽ���ˮ������Al��OH��3������CO2���壬��Ӧ�ķ���ʽΪAl3++3HCO3-=Al��OH��3��+3CO2�����ʴ�Ϊ��Al3++3HCO3-=Al��OH��3��+3CO2����
���������
�����Ѷȣ�һ��
2������� ij����ZAX���Ȼ���XCl21.10g�����Һ������1mol?L-1����������Һ20mL���ܰ���������ȫ�����������Լ��㣺
��1��X����������
��2����X�ĺ���������Ϊ20����37g?X1735Cl2���������ӵ����ʵ�����
�ο��𰸣���1�������������ʵ���Ϊ0.02L��1mol?L-1=0.02mol���������ӵ����ʵ���Ϊ0.02mol��
��Cl-+Ag+�TAgCl����֪����������Һ20mL�ܰ���������ȫ����������
��Cl-�����ʵ���Ϊ0.02mol��
XCl2�����ʵ���Ϊ0.01mol��
��XCl2��Ħ������Ϊ1.10g0.01mol=110g/mol��
����Է�������Ϊ110����X��������Ϊ110-35��2=40��
��X��������Ϊ40��?
��2��X��������Ϊ40-20=20��Cl��������Ϊ17��
37g?X1735Cl2���������ӵ����ʵ���Ϊ37g110g/mol����20+17��2��=18mol��
��37g?X1735Cl2���������ӵ����ʵ���Ϊ18mol��
���������
�����Ѷȣ�һ��
3��ѡ���� ����������ȷ���ǣ�������
A�����ǵ���ʣ������ӷ���ʽ�ж�Ҫ��������ʽ��ʾ
B�����ֽⷴӦ����������Һ�з�Ӧ������Ũ�ȼ�С�ķ������
C������кͷ�Ӧ�����ӷ���ʽ��������H++OH-=H2O��ʾ
D�����ֽⷴӦ����߱����ӷ�Ӧ�����������������ܽ���
�ο��𰸣�A�������Ե����һ�������ӷ�Ӧ�б�����ѧʽ����̼��ơ��Ȼ����ȣ������Ե������������ʽ��ʾ����NaCl��NaOH�ȣ���A����
B������֮��������ˮ�����塢����ʱ�����ֽⷴӦ�ܹ�����������Ũ�ȼ�С�����Ը��ֽⷴӦ����������Һ�з�Ӧ������Ũ�ȼ�С�ķ�����У���B��ȷ��
C�����ᡢ����������������ӷ�Ӧ��Ӧ������ѧʽ��������백ˮ�ķ�Ӧ������H++OH-=H2O��ʾ����C����
D�����ֽⷴӦ�ķ�����߱����ӷ�Ӧ������֮һ���ɣ���������NaOH��Ӧ����D����
��ѡB��
���������
�����Ѷȣ�һ��
4��ѡ���� ����ȷ��ʾ���л�ѧ��Ӧ�����ӷ���ʽ���ǣ�������
A������ͨ��ˮ�У�Cl2+H2O=Cl-+ClO-+2H+
B��FeCl2��Һ��ͨ��Cl2��Fe2++Cl2=Fe3++2Cl-
C������ͨ��ϡHNO3�У�NH3+H+=NH4+
D��̼�����Һ������ķ�Ӧ��CO32-+2H+=H2O+CO2��
�ο��𰸣�A��HClOΪ������ʣ�Ӧд�ɻ�ѧʽ����ȷ��д��Ϊ��Cl2+H2O=Cl-+HClO-+H+����A����
B����ɲ��غ㣬��ȷ��д��Ϊ��2Fe2++Cl2=2Fe3++2Cl-����B����
C������Ϊ�������壬����������Һ��Ӧ��NH3+H+=NH4+����C��ȷ��
D��̼���������ˮ��Ӧд�ɻ�ѧʽ����D����
��ѡC��
���������
�����Ѷȣ�һ��
5������� ���ֶ�����Ԫ��A��B��C��D�����ʻ�ṹ��Ϣ���£�
��Ϣ��ԭ�Ӱ뾶��С��A��B��C��D
��Ϣ������Ԫ��֮���γɵ�ij���ַ��ӵı���ģ�ͼ��������ʣ�

�����������Ϣ�ش��������⣮
��1����CԪ�������ڱ��е�λ��______����д��BC2���ӵĵ���ʽ______��
��AԪ�صĵ��������ʼ�����Ӧ�����ӷ���ʽ______��
����PtΪ�缫��KOHΪ�������Һ�������ֱ�ͨ���Һ�C�ĵ��ʿ����ȼ�ϵ�أ�д����صĵ缫��Ӧʽ������______������______
��2��A���������У�EԪ�صĵ��ʻ�ԭ����ǿ��A��E���ʷ�Ӧ�õ��Ļ�����M��һ����Ҫ�Ļ���ԭ�ϣ���ͼ�ǵ��100ml����M��Һ��װ�ã�X��Y���Ƕ��Ե缫��ʵ�鿪ʼʱ��ͬʱ�����߸����뼸�η�̪��Һ����
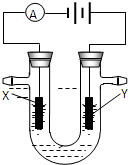
�ٵ�����Y���ϵĵ缫��Ӧʽ______������Y�缫��Ӧ����ķ�����______��
�ڵ��һ��ʱ����������ռ���112ml��״���µ����壬��ʱ���Һ��PHΪ______��������Һ��������ֲ��䣬�����£�
�ο��𰸣����ǵ��������������֮һ���ǰ��������������������������Ҫ��Դ��Ҳ������������Ҫ����ɲ��֣�Ӧ��H2O�����ݽṹ����;��֪������CH4������ǿ���������ᣬ������������ɱ����Ӧ��HClO����������Ԫ�طֱ�ΪH��C��O��Cl������ԭ�Ӱ뾶��С˳���֪A��Cl��B��C��C��O��D��H��
��1����C��OԪ�أ�������2�����Ӳ㣬����������Ϊ6��Ӧλ�ڵڶ����ڢ�A�壬B��C�γɵĻ�����ΪCO2��Ϊ���ۻ��������ʽΪ
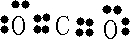
��
�ʴ�Ϊ���ڶ����ڢ�A�壻?
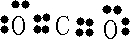
��
��Cl2��ˮ��Ӧ����HCl��HClO������HClΪǿ�ᣬ��ȫ���룬HClOΪ���ᣬ
��Ӧ�����ӷ���ʽΪCl2+H2O?

H++Cl-+HClO��
�ʴ�Ϊ��Cl2+H2O?

H++Cl-+HClO��
��CH4���л�ԭ�ԣ��ڷ�Ӧ���ױ�������ʧȥ���ӣ���ԭ��صĸ������缫��ӦʽΪCH4-8e-+10OH-=CO32-+7H2O��O2���������ԣ���ԭ��ص�������������ԭ��Ӧ��
�缫��ӦʽΪ2O2+8e-+4H2O=8OH-��
�ʴ�Ϊ��CH4-8e-+10OH-=CO32-+7H2O��2O2+8e-+4H2O=8OH-��
��2����A���������У�EԪ�صĵ��ʻ�ԭ����ǿ����EΪNaԪ�أ��õ������ҺΪNaCl��Һ�����ʱ������ӦΪ2Cl-2e-=Cl2����Cl2����ǿ�����ԣ�����ʪ��ĵ⻯�ص�����ֽ����Y�缫�������飬��������ֽ����ɫ��
�ʴ�Ϊ��2Cl-2e-=Cl2����?��ʪ��ĵ⻯�ص�����ֽ����Y�缫��������ֽ����ɫ��
�ڵ��ʱ��������ӦΪ��2H2O+2e-=2OH-+H2�����������������ʵ���Ϊ0.112L22.4L/mol=0.005mol��
��n��OH-��=2��H2��=2��0.005mol=0.01mol��c��OH-��=0.01mol0.1L=0.1mol/L��
����c��OH-��?c��H+��=1��10-14����c��H+��=1��10-13mol/L��
PH=-lg��10-13��=13��
�ʴ�Ϊ��13
���������
�����Ѷȣ�һ��