��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ���и��������˳���У���ȷ���ǣ�������
A��ԭ�Ӱ뾶Na��Mg��Al
B������H2SiO3��H2CO3��H2SO4
C���ȶ���HF��HCl��HBr
D������NaOH��Mg��OH��2��Al��OH��3
�ο��𰸣�A��Na��Mg��Al�������ڱ�ͬһ���ڣ�������ԭ�Ӱ뾶��С������Na��Mg��Al����A����
B��ͬ���ڴ����ң�Ԫ�صķǽ���������ǿ��ͬ������ϵ��£�Ԫ�صķǽ��������������зǽ�����Si��C��S��Ԫ�صķǽ�����Խǿ�����Ӧ������������ˮ���������Խǿ������������H2SiO3��H2CO3��H2SO4����B��ȷ��
C��F��Cl��Brλ��ͬһ���壬ͬ����Ԫ�ش��ϵ���Ԫ�صķǽ��������������Ӧ���⻯����ȶ��������������ȶ���HF��HCl��HBr����C����
D��Na��Mg��Al�������ڱ�ͬһ���ڣ�������Ԫ�صĽ��������������Ӧ������������ˮ����ļ������������Լ���NaOH��Mg��OH��2��Al��OH��3����D����
��ѡB��
���������
�����Ѷȣ�һ��
2��ѡ���� ��Ԫ�����ڱ��н����ͷǽ���Ԫ�صķֽ��ߵĸ��������ҵ���������
A����������ũҩ��Ԫ��
B������뵼����ϵ�Ԫ��
C����������IJ���
D���������µĺϽ����
�ο��𰸣�A������ũҩԪ�ؿ��Դ����ڱ������Ͻ��еķǽ���Ԫ�����ҵ�����A����
B��λ��Ԫ�����ڱ��н����ͷǽ���Ԫ�صķֽ��ߵĸ�����Ԫ�ؼ��н��������зǽ����ԣ����ư뵼��IJ����ڽ����ͷǽ����ķֽ��߸����ң���B��ȷ��
C����������IJ����ڹ���Ԫ�����ң������ȣ���C����
D�������ºϽ�Ԫ����Ԫ�����ڱ��Ĺ��ɽ��������ҵ�����D����
��ѡB��
���������
�����Ѷȣ���
3��ѡ���� ���ǵ������ڢ�A��Ԫ�أ������������ڱ��е�λ�����У��鲻���ܾ��е�������
A.��ĵ�����ͨ��������ǹ���
B.As2O5��ˮ������һ��ǿ��
C.AsH3��PH3�ȶ�
D.��ij������ϼ���-3��+3��+5
�ο��𰸣�B
������������ݵ���Ԫ�ؼ��仯��������ʼ�ͬ����Ԫ�ص����ʵݱ������������𣮵���Ԫ�ش��ϵ��£��䵥�����������̬�仯�����ʳʹ�̬������ĵ�����ͨ�������ҲӦ�ǹ��壻����Ԫ�ش��ϵ��£�����������ˮ���������������HNO3Ϊǿ�H3PO4Ϊ��ǿ�ᣬ��H3AsO��ӦΪ�������Ԫ�ش��ϵ��£���̬�⻯����ȶ�����������PH3��AsH3�ȶ�����Ԫ�صij������ϼ�Ϊ-3��+3��+5������ij������ϼ�ҲӦΪ-3��+3��+5
�����Ѷȣ�����
4��ѡ���� M��N���Ƕ�����Ԫ�أ�ԭ�Ӱ뾶N>M�����ǿ��γɻ�����MN2���ɴ˿ɵó�����ȷ�ж���
[? ]
A��M��N������ͬһ����
B��M��N����һ����
C��M�϶��ǽ���Ԫ��
D��N�����ڵ������ڵĢ�A���A��
�ο��𰸣�C
���������
�����Ѷȣ�һ��
5��ѡ���� ���б��﷽ʽ������ǣ�������
A��H�sCl
B��
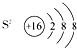
C��818O
D��O=C=O
�ο��𰸣�A���Ȼ�����ӵĵ���ʽΪ
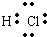
����A����
B�������ӵĽṹʾ��ͼ�ǣ�
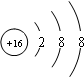
����B��ȷ��
C��������Ϊ10��ԭ�ӵķ���Ϊ818O����C��ȷ��
D��CO2���ӵĽṹʽ��O=C=O����D��ȷ��
��ѡA��
���������
�����Ѷȣ���