��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ������������ȷ���ǣ�������
A���ò��缫���NaOH��Һ��һ��ʱ�����Һ�����ʵ�������������
B���õ�ⷨ������ͭʱ����ͭ������
C���ö��Ե缫���100mL����ʳ��ˮ������112mL�����������ʱ������������Ũ��ԼΪ0.05mol/L���ٶ���Һ�����Ϊ100mL��
D��ͭпԭ��ع���ʱ�����������·�õ�����
�ο��𰸣�A���ò��缫���NaOH��Һʱ������������������ʧ�������������������������ӵõ�������������������Һ���������Ƶ������䣬ˮ���������٣�����һ��ʱ�����Һ�����ʵ�������������A����
B���õ�ⷨ������ͭʱ����ͭ����������ͭ����������B����
C���ö��Ե缫���100mL����ʳ��ˮ������112mL�����������ʱ������������112mL���������ݵ�ط�Ӧ����ʽ�������ɵ��������Ƶ����ʵ�����
�������������Ƶ����ʵ���Ϊx��
2NaCl+2H2O?���?.?Cl2��+H2��+2NaOH
? 22.4L? 2mol
? 0.112L? x
x=0.01mol������������Ũ��C=nV=0.01mol0.1L=0.1mol/L����C����
D��ͭпԭ��ع���ʱ��������пʧ���ӷ���������Ӧ�������ϵõ��ӷ�����ԭ��Ӧ�����ӴӸ��������·�����������������������·�õ����ӣ���D��ȷ��
��ѡD��
���������
�����Ѷȣ���
2������� ��14�֣�����V�����仯����㷺Ӧ���ڹ�ҵ�����²��Ϻ�����Դ������
��1��V2O5�ǽӴ���������Ĵ�����
��һ�������£� �������ӳt min��
�������ӳt min�� ��
��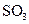 ���ʵ���Ũ�ȷֱ�Ϊa mol/L��b mol/L, ��
���ʵ���Ũ�ȷֱ�Ϊa mol/L��b mol/L, �� ��ʼ���ʵ���Ũ��Ϊ mol/L ������
��ʼ���ʵ���Ũ��Ϊ mol/L ������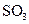 �Ļ�ѧ��Ӧ����Ϊ mol/(L��min) ��
�Ļ�ѧ��Ӧ����Ϊ mol/(L��min) ��
�ڹ�ҵ�����ᣬβ�� ��_______���գ�
��_______���գ�
��2��ȫ��Һ�����ܵ�������ò�ͬ��̬���ӶԵ�������ԭ��Ӧ��ʵ�ֻ�ѧ�ܺ͵����ת����װ�ã���ԭ������29ͼ��ʾ��
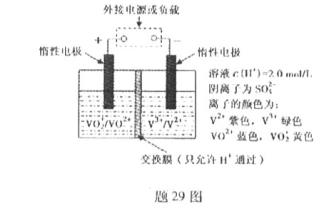
�ٵ������Һ���ɻƱ�������缫��ӦʽΪ ��
�ڳ������У��Ҳ���Һ��ɫ���� ɫ��Ϊ ɫ��
�۷ŵ�����������ӵ������� �� �����ʱ��ת�Ƶĵ�����Ϊ3.01 1023���������Һ��n(H+)�ı仯��Ϊ ��
1023���������Һ��n(H+)�ı仯��Ϊ ��
�ο��𰸣�
��1����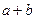 ��
��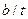
�ڰ�ˮ
��2����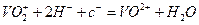
���� ��
�۲���������Ӧ��ͨ������Ĥ�����ƶ�ʹ����ͨ����Һ��0.5mol
�����������
�����Ѷȣ���
3��ѡ���� ij������ȼ�ϵ����CaHSO4����Ϊ����ʴ���H����������ṹ����ͼ������ܷ�Ӧ�ɱ�ʾΪ��2H2��O2��2H2O�������й�˵����ȷ����
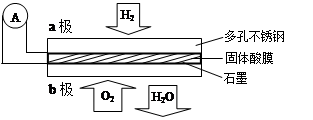
A������ͨ�����·��b������a��
B��b���ϵĵ缫��ӦʽΪ��O2��2H2O��4e����4OH��
C��ÿת��0��1 mol���ӣ�����1��12 L��H2
D��H����a��ͨ�����������ʴ��ݵ�b��
�ο��𰸣�D
������������ݵ���ܷ�Ӧ��2H2+O2=2H2O��֪��ͨ��������һ��Ϊ��صĸ���������������Ӧ����ӦΪH2-2e-�T2H+��ͨ��������һ��Ϊ��ص�������������ԭ��Ӧ����ӦΪO2+4e-+4H+=2H2O����ع���ʱ������ͨ�����·�Ӹ�����������������a������b�����������Һ���������������ƶ�����H+��a��ͨ�����������ʴ��ݵ�b����ÿת��0��1mol���ӣ�����0��05mol��H2����״���µ����Ϊ1��12L��A������Ԫ�صĻ��ϼ����ߣ���aΪ��������������Ӧ����ͨ�����·��a������b����A����B���õ��Ϊ���Ե�أ���ӦΪO2+4e-+4H+=2H2O����B����C����û��˵���Ƿ�Ϊ��״����������������һ��Ϊ1��12L����C����D��ԭ����У��������������ƶ�������H+��a��ͨ�����������ʴ��ݵ�b������D��ȷ����ѡD��
�����Ѷȣ�һ��
4��ѡ���� п��ͭ��ϡ������ɵ�ԭ��أ������й�˵����ȷ���ǣ� ��
��п�������ݲ��� �ڵ�����Zn�����·����Cu
�۸�����Zn +2e-=Zn2+ ��Cu2+����Һ����Cu����Zn��Ǩ��
A���٢ڢ�
B���ڢ�
C����
D���ڢ�