微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 用来表示可逆反应:2A(g)+B(g) 2C(g)ΔH<0的正确图象是下图中的(?)
2C(g)ΔH<0的正确图象是下图中的(?)

A? B? C? D
参考答案:AC
本题解析:略
本题难度:简单
2、填空题 (8分)现有反应aA(g)+bB(g)  pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数也减小,则:
pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数也减小,则:
(1)该反应的正反应是________热反应,且a+b________p(填“>”“<”或“=”)。
(2)减压时,A的质量分数________(填“增大”“减小”或“不变”,下同),正反应速率________。
(3)若加入B(体积不变),则A的转化率________,B的转化率________。
(4)若升高温度,则平衡时,B、C的浓度之比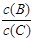 将________。
将________。
(5)若加入催化剂,平衡时气体混合物的总物质的量________。
参考答案:(1)吸 > (2)增大 减小 (3)增大 减小 (4)减小 (5)不变
本题解析:(1)升高温度时,B的转化率变大,说明升高温度,平衡向正反应方向移动,即正反应是吸热反应。减小压强时,混合体系中C的质量分数减小,说明降低压强,平衡向逆反应方向移动,则正反应是体积减小的,即a+>p。
(2)降低压强,平衡向逆反应方向移动,所以A的质量分数增大。反应速率都是减小的。
(3)增加B的浓度,平衡向正反应方向移动,所以A的转化率增大,但B的转化率降低。
(4)升高温度,平衡向正反应方向移动,则C的浓度增大,B的浓度减小,因此 减小。
减小。
(5)催化剂不能改变平衡状态,所以平衡时气体混合物的总物质的量不变。
本题难度:一般
3、选择题 不久前,科学家发现了一种新能源――“可燃冰”晶体.它的主要成分是甲烷与水分子(CH4・xH2O).据测定1 m3这种晶体可释放出140 m3甲烷气体(设气体体积已折算成标准状况,可燃冰的密度近似为1 g・cm-3).试推算该“可燃冰”中,CH4与H2O分子个数比为
A.1∶6
B.1∶7
C.1∶8
D.1∶9
参考答案:C
本题解析:根据甲烷的体积求其物质的量及甲烷的质量,进而求H2O的质量和物质的量.
本题难度:一般
4、计算题 (9分)某温度时,在2? L密闭容器中气态物质X和Y反应生成气态物质Z,它们的物质的量随时间的变化如下表所示。
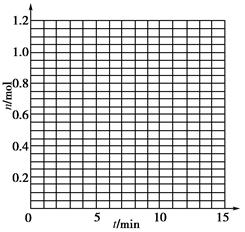
(1)根据下表中数据,在下图中画出X、Y、Z的物质的量(n)随时间(t)变化的曲线:
t/min
| X/mol
| Y/mol
| Z/mol
|
0
| 1.00
| 1.00
| 0.00
|
1
| 0.90
| 0.80
| 0.20
|
3
| 0.75
| 0.50
| 0.50
|
5
| 0.65
| 0.30
| 0.70
|
9
| 0.55
| 0.10
| 0.90
|
10
| 0.55
| 0.10
| 0.90
|
14
| 0.55
| 0.10
| 0.90
|
(2)体系中发生反应的化学方程式是___________________________________________;
(3)列式计算该反应在0~3 min时间内产物Z的平均反应速率:___________________;
(4)该反应达到平衡时反应物X的转化率α等于??;
(5)如果该反应是放热反应。改变实验条件(温度、压强、催化剂)得到Z随时间变化的曲线1、2、3(如下图所示)则曲线1、2、3所对应的实验条件改变分别是:1______________,2______________,3______________。
参考答案:
 (1)
(1) ? (2)X+2Y
? (2)X+2Y 2Z
2Z
(3)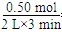 =0.083 mol・L-1・min-1? (4)45%? (5)升高温度加入催化剂增大压强
=0.083 mol・L-1・min-1? (4)45%? (5)升高温度加入催化剂增大压强
本题解析:
 本题考查化学反应速率和化学平衡的综合运用,图像识别和有关计算。
本题考查化学反应速率和化学平衡的综合运用,图像识别和有关计算。
 (1)根据题目中表格给出的数据,在坐标系中找出相应的点,然后用光滑的曲线描点即可。
(1)根据题目中表格给出的数据,在坐标系中找出相应的点,然后用光滑的曲线描点即可。
 (2)考查可逆反应的有关计算,一般采用三段式计算,即
(2)考查可逆反应的有关计算,一般采用三段式计算,即
 ? aX? +? bY
? aX? +? bY cZ
cZ
 起始量(mol)? 1.00? 1.00? 0
起始量(mol)? 1.00? 1.00? 0
 转化量(mol)? 0.45? 0.9? 0.9
转化量(mol)? 0.45? 0.9? 0.9
 平衡量(mol)? 0.55? 0.1? 0.9
平衡量(mol)? 0.55? 0.1? 0.9
 根据各物质的物质的量的变化量之比是相应的化学计量数之比可知,体系中发生反应的化学方程式是: X+2Y
根据各物质的物质的量的变化量之比是相应的化学计量数之比可知,体系中发生反应的化学方程式是: X+2Y 2Z。
2Z。
 (3)根据图像可知在3min时,生成物Z的物质的量为0.5mol,其平均速率为
(3)根据图像可知在3min时,生成物Z的物质的量为0.5mol,其平均速率为
0.083mol/L・min。
 (4)平衡时X的物质的量是0.55mol,消耗X是0.45mol,所以X的转化率等于0.45mol÷1.00mol×100%=45%。
(4)平衡时X的物质的量是0.55mol,消耗X是0.45mol,所以X的转化率等于0.45mol÷1.00mol×100%=45%。
 (5)由题目所给图象可知,在1中,平衡时Z的物质的量小于原平衡的物质的量,说明平衡逆向移动,条件为升高温度;在2中,平衡时Z的物质的量与原平衡相同,且速率加快,条件为加入催化剂;在3中,平衡正向移动,且速率加快,条件为加压。
(5)由题目所给图象可知,在1中,平衡时Z的物质的量小于原平衡的物质的量,说明平衡逆向移动,条件为升高温度;在2中,平衡时Z的物质的量与原平衡相同,且速率加快,条件为加入催化剂;在3中,平衡正向移动,且速率加快,条件为加压。
本题难度:一般
5、填空题 (10分)已知A(g)+B(g) C(g)+D(g)反应的平衡常数和温度的关系如下:
C(g)+D(g)反应的平衡常数和温度的关系如下:
|温度/ ℃
| 700
| 900
| 830
| 1000
| 1200
|
平衡常数
| 1.7
| 1.1
| 1.0
| 0.6
| 0.4
|
回答下列问题:
(1).该反应的平衡常数表达式K=?。
(2).830℃时,向一个5 L的密闭容器中充入0.20mol的A和0.80mol的B,如反应初始6s内A的平均反应速率v(A)=0.003 mol・L-1・s-1。,则6s时c(A)=??mol・L-1,若反应经一段时间后,达到平衡时A的转化率为?,如果这时向该密闭容器中再充入1 mol氩气,平衡时A的转化率为?;
(3).1200℃时反应C(g)+D(g)  A(g)+B(g)的平衡常数的值为?。
A(g)+B(g)的平衡常数的值为?。
参考答案:(1) (2)0.022 80% 80%? (3)2.5
(2)0.022 80% 80%? (3)2.5
本题解析:试题分析:(1)该反应平衡常数表达式为 。
。
(2)v(A)=△c(A)/t,A浓度变化为0.003×6=0.018mol/L,所以6s时A的物质的量浓度为(0.04-0.018)mol/L=0.022mol/L;设达到平衡时转化的A的物质的量浓度为xmol/L。
A(g)? +? B(g) C(g)+D(g)
C(g)+D(g)
始(mol/L)0.04? 0.16
平(mol/L)0.04-x? 0.16-x? x? x
830℃时K=1得(0.04-x)(0.16-x) =x・x解得x=0.032。
所以A的转化率为0.032/0.04×100%=80%。若向溶液中再充入氩气,各组分浓度不变,平衡不移动。A的转化率仍为80%。
(3)C(g)+D(g)  A(g)+B(g)与A(g)+B(g)
A(g)+B(g)与A(g)+B(g) C(g)+D(g)平衡常数互为倒数,1200℃时反应C(g)+D(g)
C(g)+D(g)平衡常数互为倒数,1200℃时反应C(g)+D(g)  A(g)+B(g)的平衡常数K=1/0.4=2.5。
A(g)+B(g)的平衡常数K=1/0.4=2.5。
点评:反应物、生成物互为颠倒,平衡常数互为倒数。
本题难度:一般