��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ��16�֣�±�����Ҫ�ɷ���MgCl2�������Fe2+��Fe3+��Mn2+���������ӡ���±��Ϊԭ�ϰ���ͼ��ʾ���̽������������Ƶ���������þ��
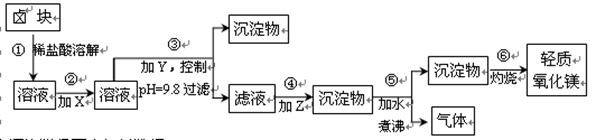
�������ϵ��±�������ݣ�
��1�� �����������������pH
| ��2�� ԭ�ϼ۸��
|
����
| ��ʼ����
| ������ȫ
| ����
| �۸�Ԫ/�֣�
|
Fe(OH)3
| 2.7
| 3.7
| a��ƯҺ����25.2%NaClO��
| 450
|
Fe(OH)2
| 7.6
| ? 9.6�~
| b��˫��ˮ����30%H2O2��
| 2400
|
Mn(OH)2
| 8.3
| 9.8
| c���ռ��98%NaOH��
| 2100
|
Mg(OH)2
| 9.6
| 11.1
| d�������99.5%Na2CO3��
| 600
|
�~Fe2+�����������״�����״���Һ�г�ȥ�����뽫����������Fe(OH)3������ʽ���ܳ�����
��Ҫ���Ʒ�������������������ɱ��ϵͣ�������ϱ��ṩ�����ϻش�
��1�������м�����Լ�X��Y��Z���ѡ�������DZ�2�е�??��ѡ���Լ���ţ���
��2������ڷ�����Ӧ�����ӷ���ʽΪ?��������з�����Ӧ�Ļ�ѧ����Ϊ???��
��3������ۿ���pH=9.8��Ŀ����???��
��4�� ����ʵ���ҽ��в��������ʵ�飬�����õ��������������š��ƾ���ơ�?��
�����ǡ�
��5����̽��Mg(OH)2�ܽ��Ե�ʵ���У�������װ������Mg(OH)2��Һ���Թ��м�������
NH4Cl���壬�������Һ�����壬���û�ѧƽ���ԭ��������Һ������ԭ
��?��
�ο��𰸣���16�֣�
��1��a��c��d����1�֣�
��2��2Fe2+ + ClO�� + 2H+ = Cl�� +2Fe3++ H2O��MgCO3 + H2O��Mg(OH)2+ CO2������3�֣�
��3��ʹMg2+��������ʾ����ܳ���ת��Ϊ������ȥ��2�֣�
��4������?��2�֣�
��5��Mg(OH)2(s) 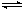 Mg2+ (aq)+ 2OH��(aq)�� NH4Cl �������NH4+��OH����ϳ��������NH3��H2O��������c(OH��)��Mg(OH)2�ܽ�ƽ�������ƶ���3�֣���
Mg2+ (aq)+ 2OH��(aq)�� NH4Cl �������NH4+��OH����ϳ��������NH3��H2O��������c(OH��)��Mg(OH)2�ܽ�ƽ�������ƶ���3�֣���
�����������1������ͼ�м���X��Ŀ���ǽ�������������Ϊ�����ӣ������������ļ۸�Ӧ��ѡ��Ư�ۣ�����Y��Ŀ���ǵ�����Һ��pH��ʹ�����ӡ������ӳ�����̼������Һ�Լ��ԣ������Բ�ǿ������ѡ�����������ƣ�����Z��Ŀ����ʹþ���ӳ���������ѡ��̼���ƣ��Ҽ�ˮ��У�ʹ���ɵ�̼��þ����ת��Ϊ������þ�������ɱ��ϵͣ�����Լ�X��Y��Z���ѡ�������DZ�2�е�a��c��d��
��2������NaClO��Ŀ���ǽ�������������Ϊ�����ӣ����ӷ���ʽΪ2Fe2+ + ClO�� + 2H+ = Cl�� +2Fe3++ H2O��������ǰ�̼��þ����ת��Ϊ������þ����ѧ����ʽΪMgCO3 + H2O��Mg(OH)2+ CO2����
��3�����ݱ�1�е����ݿ�֪��pH=9.8ʱ�����ӡ���������ȫ��������þ���ӿ�ʼ�����������̵�Ҫ���Dz�Ʒ�����������ʣ����Բ���ۿ���pH=9.8��Ŀ����ʹMg2+��������ʾ����ܳ���ת��Ϊ������ȥ��
��4������ʱ�õ��������������š��ƾ���ơ������������ǡ�
��5��NH4Cl��Һ�е�笠��������ܽ�ƽ����Mg(OH)2(s) 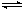 Mg2+ (aq)+ 2OH��(aq)�����������ӽ�������������NH3��H2O��������c(OH��)��Mg(OH)2�ܽ�ƽ�������ƶ�������������þ���ܽ⡣
Mg2+ (aq)+ 2OH��(aq)�����������ӽ�������������NH3��H2O��������c(OH��)��Mg(OH)2�ܽ�ƽ�������ƶ�������������þ���ܽ⡣
�����Ѷȣ�һ��
2��ѡ���� 25��ʱ��ij���ʵ�ˮ��Һ����ˮ�������c��H+��=1��10-12mol/L������Һ��һ�����ܴ������ڵ�������
A.NH4+
B.HCO3-
C.SO32-
D.NO3-
�ο��𰸣�B
���������������25��ʱ��ij���ʵ�ˮ��Һ����ˮ�������c��H+��=1��10-12mol/L��Ϊ������Һ����������֮�䲻�ܽ������ˮ�����塢�����ȣ����ܴ������棬�Դ������
���25��ʱ��ij���ʵ�ˮ��Һ����ˮ�������c��H+��=1��10-12mol/L��Ϊ������Һ��
A������Һ����������笠����Ӳ���Ӧ���ܹ��棬��A��ѡ��
B��HCO3-�������ᷴӦ������Ӧ��һ�����ܹ��棬��Bѡ��
C������Һ������֮�䲻��Ӧ���ܹ��棬��C��ѡ��
D������������Һ������֮�䲻��Ӧ���ܹ��棬��D��ѡ��
��ѡB��
���������⿼�����ӵĹ��棬��ȷϰ���е���Ϣ�ǽ����Ĺؼ�����Ϥ���ֽⷴӦ�������������ɽ����Ŀ�ѶȲ���
�����Ѷȣ�����
3������� ����A��B��C��D��E��F���ֳ����������֪���ǰ�������������K����Ag����Na����
Ba2����Fe2����Al3������������Cl����OH����AlO2-��NO3-��SO42-��CO32-�������Ƿֱ����0.1 mol/L����Һ��������ʵ�飺
�ٲ����ҺA��C��E���ʼ��ԣ��Ҽ���A��E��C��E����ɫ��dz��ɫ������ɫ�ܲ����۲죩������B��Һ�еμ�ϡ��ˮ�������������ɳ����������ȫ���ܽ⣻����F��Һ�еμ�ϡ���ᣬ��Һ����ػ�ɫ��������ɫ�������ɣ�����D��Һ�еμ�Ba��NO3��2��Һ����������
��1��д��A��D��E��F�Ļ�ѧʽ��
A________��D________��E________��F________��
��2�������ӷ���ʽ����C��Һ�ʼ��Ե�ԭ��__________________________________��
��3��д��ʵ����з�Ӧ�����ӷ���ʽ��________________________________��
�ο��𰸣���1��Ba��OH��2 AlCl3 KAlO2 FeSO4
��2��CO32-��H2O HCO3-��OH��
HCO3-��OH��
��3��3Fe2����NO3-��4H��=3Fe3����NO����2H2O
���������ʹ��Һ�ʼ��Ե���������OH����AlO2-��CO32-������ʵ��ڿ���ȷ��BΪAgNO3������ʵ��ۿ���ȷ��F����ΪFeCl2����FeSO4������ʵ��ܿ���ȷ��D�����ܺ���SO42-������FΪFeSO4��DΪAlCl3��������������������С��̼������ģ�����ƫ�����εļ���ǿ��̼���εģ���ϼ���A��E��C������ȷ��AΪBa��OH��2��EΪKAlO2��CΪNa2CO3��C��Һ�ʼ��Ե�ԭ��CO32-��H2O HCO3-��OH����ʵ����з�Ӧ�����ӷ���ʽΪ3Fe2����NO3-��4H��=3Fe3����NO����2H2O��
HCO3-��OH����ʵ����з�Ӧ�����ӷ���ʽΪ3Fe2����NO3-��4H��=3Fe3����NO����2H2O��
�����Ѷȣ�һ��
4��ѡ���� ���л������У����ܷ�����ȥ��Ӧ����
A.CH3CH2OH
B.CH3CH2Cl
C.(CH3)2CHBr
D.(CH3)3C��CH2Br
�ο��𰸣�D
�����������ȥ��Ӧ��ָ��һ�������£��л����������ȥһ����С�������ɷ����к���˫���Ļ������Ȳ������л���ķ�Ӧ����ȥ��Ӧ��Ϊ���֣�һ���Ǻ����ǻ������ʣ��ǻ�������̼ԭ���ϵ��⣬��Ũ�������170��������£���ȥһ��ˮ����һ��˫����ˮ���ӡ�һ����±���������������ƴ���Һ���������£�±��ԭ�Ӻ�����̼ԭ���ϵ�����ȥ������±�����˫������ȥ��Ӧ�߱�������Ϊ����������������̼�������ڵ�C��һ��Ҫ���⣺
�����Ѷȣ�����
5��ѡ���� ���и������ӣ����������NaOH��Һ���ܴ����������
A.Al3+��K+��AlO2-��Cl-
B.Ba2+��Na+��Cl-��SO42-
C.Na+��Cl-��SO42-��I-
D.Na+��K+��Ag+��NO3-
�ο��𰸣�C
���������
�����Ѷȣ�����