微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 在温度为373K时,将0.100mol无色的N2O4气体放入1L抽空的密闭容器中,立刻出现红棕色,直至建立N2O4?

?2NO2的平衡.下图是隔一定时间测定到的N2O4的浓度(纵坐标为N2O4的浓度,横坐标为时间)
(1)计算在20至40秒时间内,NO2的平均生成速率为______mol?L-1?S-1.
(2)该反应的化学平衡常数表达式为K=______.
(3)下表是不同温度下测定得到的该反应的化学平衡常数.
据此可推测该反应(生成NO2)是______反应(选填“吸热”或“放热”).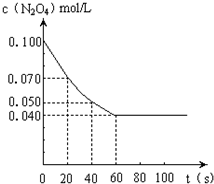
参考答案:(1)在20至40秒时间内,c(N2O4)=0.07mol/L-0.05mol/L20s=0.001mol/(L?s),
由方程式可知:c(NO2)=2×c(N2O4)=2×0.001mol/(L?s)=0.002mol/(L?s),故答案为:0.002;
(2)平衡常数为生成物的浓度幂之积除以反应物的浓度幂之积,在N2O4?

?2NO2中,k=C2(NO2)C(N2O4),
故答案为:C2(NO2)C(N2O4);
(3)由表中数据可知,温度升高,平衡常数增大,则说明升高温度,平衡向正反应方向移动,则正反应为吸热反应,
故答案为:吸热.
本题解析:
本题难度:简单
2、简答题 373K时,某1L密闭容器中加入1molPCl5发生如下可逆反应:
PCl5?(g)

PCl3(g)+Cl2?(g).其中物质PCl3的物质的量变化如右图所示.
(1)前20s内PCl5(g)的平均反应速率为______
(2)373K时该反应的平衡常数的值为______
(3)若在此平衡体系中再加入1mol的PCl5,与原平衡比较,新平衡时PCl5的转化率______(填“增大”或“减小”,下同).PCl5的平衡浓度______
(4)将原平衡升温至473K,重新达平衡时(其他条件不变),PCl3的平衡浓度为PCl5的3倍,该反应的正反应为______(填“放热反应”或“吸热反应”),为增大平衡体系中Cl2的物质的量,下列措施正确的是(其它条件相同)______
a.升高温度?b.扩大容器的体积
c.加入合适的催化剂?d.再充入PCl3.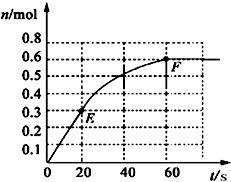
参考答案:(1)由图象可知20s时,生成的PCl3的物质的量为0.3mol,所以前20s内,PCl3(g)的平均反应速率为
v(PCl3)=△n(PCl3)V△t=0.3mol1L20s=0.015mol?L-1?s-1,反应速率之比等于化学计量数之比,所以v(PCl5)=v(PCl3)=0.015mol?L-1?s-1.
故答案为:0.015mol?L-1?s-1;
(2)由图象可知60s时,反应达平衡,平衡时生成的PCl3的物质的量为0.6mol,
利用三段式解题法,求出平衡时混合物各组分的物质的量
?PCl5?(g)

PCl3(g)+Cl2?(g),
开始(mol):1? 0? 0
变化(mol):0.6? 0.6? 0.6
平衡(mol):0.4? 0.6? 0.6
所以k=c(PCl3)c(Cl2)c(PCl5)=0.6×0.60.4=0.9mol?L-1,
故答案为:0.9mol?L-1;
(3)平衡体系中再加入1mol的PCl5,重新到达平衡状态,可以等效为开始加入2mol的PCl5,体积增大为原来的2倍,达平衡(该平衡与原平衡等效)后再将体积压缩到原来大小,与原平衡相比,积压缩压强增大平衡状态,平衡向体积减小的方向移动,即向逆反应方向移动,转化率减小,移动结果降低浓度增大趋势,平衡时浓度仍然高于原平衡,故新平衡时PCl5的转化率减小,浓度增大.
故答案为:减小;增大;
(4)由(2)可知,373K时该反应达平衡时,PCl3的平衡浓度为PCl5的1.5倍,而升温至473K重新达平衡时(其他条件不变),PCl3的平衡浓度为PCl5的3倍,倍数增加,说明平衡向正反应移动,升高温度平衡向吸热反应移动,故该反应正反应为吸热反应.
增大平衡体系中Cl2的物质的量,平衡应向正反应移动.
a、正反应为吸热反应,升高温度,平衡向正反应移动,Cl2的物质的量增大,故a正确;
b、扩大容器的体积、压强降低,平衡向体积增大方向移动,即向正反应移动,Cl2的物质的量增大,故b正确;
c、加入合适的催化剂,缩短达到平衡的时间,平衡不移动,Cl2的物质的量不变,故c错误;
d、再充入PCl3,平衡向逆反应移动,Cl2的物质的量减小,故d错误;
则ab措施正确,故答案为:吸热反应;ab.
本题解析:
本题难度:一般
3、选择题 下列对化学反应限度的叙述中错误的是
[? ]
A.任何可逆反应在给定条件下都有一定的限度
B.化学反应达到限度时,正、逆反应速率相等
C.化学反应的限度与时间的长短无关
D.化学反应的限度不随外界条件的改变而改变
参考答案:D
本题解析:
本题难度:简单
4、填空题 钨是属于有色金属,也是重要的战略金属,钨矿在古代被称为“重石”.1783年被西班牙人德普尔亚发现黑钨矿也从中提取出钨酸,同年,用碳还原三氧化钨第一次得到了钨粉,并命名该元素.钨是的用途十分广,涉及矿山、冶金、机械、建筑、交通、电子、化工、轻工、纺织、军工、航天、科技、各个工业领域.现在高温下,在密闭容器中用H2还原WO3可得到金属钨,其总反应为:WO3(s)+3H2(g)
W(s)+3H2O(g)
请回答下列问题:
(1)上述反应的化学平衡常数表达式为______.
(2)某温度下反应达平衡时,H2与水蒸气的体积比为2:3,则H2的平衡转化率为______;随温度的升高,H2与水蒸气的体积比减小,则该反应正反应为______反应(填“吸热”或“放热”).
(3)上述总反应过程大致分为三个阶段,各阶段主要成分与温度的关系如下表所示:
| 温度 | 25℃~550℃~600℃~700℃
主要成份
WO3W2O5WO2W
|
第一阶段反应的化学方程式为______;580℃时,固体物质的主要成分为______;假设WO3完全转化为W,则三个阶段消耗H2物质的量之比为______
(4)钨丝灯管中的W在使用过程中缓慢挥发,使灯丝变细,加入I2可延长灯管的使用寿命,其工作原理为:W(s)+2I2(g)WI4(g).下列说法正确的有______.
A.灯管内的I2可循环使用
B.WI4在灯丝上分解,产生的W又沉积在灯丝上
C.WI4在灯管壁上分解,使灯管的寿命延长
D.温度升高时,WI4的分解速率加快,W和I2的化合速率减慢.
参考答案:(1)WO3(s)+3H2(g)高温.W(s)+3H2O(g)的平衡常数k=c3(H2O)c3(H2),故答案为:c3(H2O)c3(H2);
(2)由反应方程式知,消耗的H2与生成的水的物质的量相等,故H2的平衡转化率为3mol2mol+3mol×100%=60%,
升高温度,H2与水蒸气的体积比减小,说明升温时平衡向右移动,故正反应为吸热反应,
故答案为:60%,吸热;
(3)由表中主要成分与温度关系可知,第一阶段反应为WO3与H2反应是W2O5,同时还生成H2O,反应方程式为:
2WO3+H2高温.W2O5+H2O,580℃时,温度介于550℃~600℃,固体为W2O5、WO2的混合物;
假定有2molWO3,由2WO3+H2高温.W2O5+H2O、W2O5+H2?高温.2WO2+H2O、WO2+2H2?高温.W+2H2O可知,三个阶段消耗的氢气的物质的量之比为1mol:1mol:2mol×2=1:1:4,
故答案为:2WO3+H2高温.W2O5+H2O,W2O5、WO2,1:1:4;
(4)由所给化学方程式知,挥发的W与I2结合形成气态WI4,由于气体运动的结果,WI4会与还没有挥发的W接触,在高温下WI4分解生成的W及I2,生成W附着在还没有挥发的W上,灯管内的I2可循环使用,故A、B对;灯管壁温度较低,WI4不会分解,故C错;升高温度,也能加快W与I2的反应速率,故D错,
故答案为:A、B.
本题解析:
本题难度:一般
5、填空题 在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g)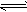 CO(g)+H2O(g)其化学平衡常数K与温度t的关系如下表:
CO(g)+H2O(g)其化学平衡常数K与温度t的关系如下表:

回答下列问题:
(1)该反应的化学平衡常数表达式为K=_______________。
(2)该反应为_____________反应(填“吸热”“放热”)。
参考答案:(1)K=[c(CO)・c(H2O)]/[c(CO2)・c(H2)]
(2)吸热
本题解析:
本题难度:一般