微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 NaNO2有像食盐一样的外观和咸味,它可将正常的血红蛋白变为高铁血红蛋白,使血红蛋白中的铁元素由二价变为三价,失去携氧能力,美蓝是亚硝酸盐中毒的有效解毒剂。
(1)下列说法正确的是_________(填序号)。
A.解毒剂美蓝应该具有氧化性? B.中毒时亚硝酸盐发生氧化反应
C.解毒时高铁血红蛋白被还原? D.中毒过程中血红蛋白显氧化性
(2)已知NaNO2能发生如下反应:2NaNO2+4HI=2NO+I2+2NaI+2H2O从上述反应推知________(填序号)。
A.氧化性:I2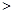 NaNO2?B.氧化性:NaNO2
NaNO2?B.氧化性:NaNO2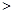 I2
I2
C.还原性:HI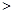 NO? D.还原性:I2
NO? D.还原性:I2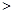 HI
HI
(3)根据上述反应,可用试纸和生活中常见的物质进行实验来鉴别NaNO2和NaCl。现供选用的物质有:①白酒?②碘化钾淀粉试纸?③淀粉?④白糖?⑤食醋,进行本实验时,可以选用的物质至少有__________(填序号)。
(4)某工厂的废液中含有2%~5%的NaNO2,直接排放会造成污染。下列试剂中:①NaCl②NH4Cl?③HNO3?④浓H2SO4,能使NaNO2转化为N2的是_______(填序号)。
参考答案:(1)C(2分)
(2)BC(2分,选对一个得1分,错选一个倒扣一分)
(3)②⑤(全对得2分)
(4)②(2分)
本题解析:(1)NaNO2使人中毒的原因是:NaNO2把Fe2+氧化为Fe3+,NaNO2发生了还原反应,血红蛋白显示了还原性,故B、D项错误;美蓝解毒时把Fe3+还原为Fe2+,美蓝具有还原性,所以A项错,C项正确。
(2)在同一氧化还原反应中,氧化性强弱顺序为:氧化剂>氧化产物;还原性强弱顺序为:还原剂>还原产物,所以BC项正确。
(3)根据(2)中化学反应,NaNO2在酸性条件下可将I?氧化为I2,所以②⑤即可鉴别NaNO2与NaCl。
(4)NaNO2转化为N2,NaNO2作氧化剂,需要加入还原剂,故选②NH4Cl。,,,
本题难度:一般
2、选择题 下列叙述中,可以说明金属甲的活动性比金属乙的活动性强的是
A.在氧化-还原反应中,甲原子失去的电子比乙原子失去的电子多
B.同价态的阳离子,甲比乙的氧化性强
C.甲能跟稀盐酸反应放出氢气而乙不能
D.甲原子的最外层电子数比乙原子的最外层电子数少
参考答案:C
本题解析:考查金属性强弱比较。比较金属性强弱时,可以利用元素周期律、金属和酸或水反应生成氢气的难易程度、最高价氧化物的水化物的碱性强弱或金属单质之间的相互置换能力等。失电子的多少和金属性强弱无关,只与失去电子的难易程度有关系,越容易失去电子的,金属性越强。因此选项AD均不一定。金属性越强,相应阳离子的氧化性就越弱,B不正确。答案选C。
本题难度:简单
3、选择题 下列反应中氯元素被氧化的是
[? ]
A.5Cl2+I2+6H2O===10HCl+2HIO3
B.2Cl2+2Ca(OH)2===CaCl2+Ca(ClO)2+2H2O
C.MnO2+4HCl===MnCl2+2H2O+Cl2↑
D.2NaCl+2H2O2 NaOH+Cl2↑+H2↑
NaOH+Cl2↑+H2↑
参考答案:D
本题解析:
本题难度:一般
4、选择题 单晶硅是制作电子集成电路的基础材料。科学家预计,到2011年一个电脑芯片上将会集成10亿个晶体管,其功能远比我们想象的要大的多,这对硅的纯度要求很高。用化学方法可制得高纯度硅,其化学方程式为 : ①SiO2+2C Si+2CO ②Si+2Cl2
Si+2CO ②Si+2Cl2 SiCl4 ③SiCl4+2H2
SiCl4 ③SiCl4+2H2 Si+4HCl,其中反应①和③属于
Si+4HCl,其中反应①和③属于
[? ]
A.化合反应
B.分解反应
C.置换反应
D.复分解反应
参考答案:C
本题解析:
试题分析:
解:化合反应是两种或两种以上物质反应后生成一种物质的反应,其特点可总结为“多变一”;分解反应是一种物质反应后生成两种或两种以上的物质,其特点可总结为“一变多”.置换反应是一种单质和一种化合物反应生成另一种单质和另一种化合物;复分解反应是指两种化合物相互交换成分生成两种化合物的反应。
由化学方程式可知,①③反应中的反应物和生成物都是一种单质和一种化合物,属于置换反应;②中的反应物是两种,生成物是一种,属于化合反应。
故选C.
本题难度:简单
5、填空题 (1)在反应MnO2 + 4HCl = MnCl2 + 2H2O +Cl2↑中,
①用双线桥法标出电子转移的方向和数目:__________________________
②还原剂是_______________;
③HCl中,被氧化的Cl原子与未被氧化的Cl原子个数比是__________________。
④若要产生112 mL氯气,则转移的电子数目是____________________。
(2) 已知金属钠投入水中能发生下列反应2Na+2H2O==2NaOH+H2↑。现将2.3g钠投入水中,充分反应后。则n(NaOH )=___________;V(H2)=_____________(标准状况下);假设反应后得到的溶液中Na+与水分子的个数比为1:100,则反应所需的m(H2O)=________
参考答案:(1)① 电子转移的方向和数目“略”;②HCl;③1∶1;④6.02×1021
(2)①0.1mol;②1.12L;③181.8g
本题解析:
本题难度:一般