微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 某铁的氧化物,用7mol/L的盐酸100mL在一定条件下恰好完全溶解,所得溶液再通入0.56L氯气时,刚好使溶液中Fe2+完全转化为Fe3+。则该氧化物的化学式是(?)
A.FeO
B.Fe3O4
C.Fe4O5
D.Fe5O7
参考答案:D
本题解析:从2Fe2+ +Cl2=2Fe3+ +2Cl-可知Fe2+为0.05mol
设该氧化物为(FeO)x(Fe2O3)y?它与盐酸反应的方程式即为
FeO+2HCl==FeCl2+H2O? Fe2O3+6Hcl==2FeCl3+3H2O
故可知FeO为0.05mol?它反应的盐酸为0.1mol
故Fe2O3反应了0.6mol盐酸?故有0.1molFe2O3
FeO:Fe2O3的物质的量之比为1:2
即:(FeO)1(Fe2O3)2,也就是 Fe5O7,答案为D
本题难度:简单
2、填空题 铁盐、亚铁盐是实验室常用的药品。根据题意完成下列填空:
(1)若向硫酸亚铁溶液中滴加稀硝酸,可以看到溶液逐渐变黄。为检验最后溶液中是否还有亚铁离子剩余,可以_____________________________________________;向已酸化的FeCl3溶液中逐滴加入Na2S溶液,有浅黄色沉淀生成,溶液逐渐变为浅绿色。写出该反应的离子方程式?。
(2)向FeSO4溶液中加几滴硫氰化钾溶液,无现象,再滴加H2O2,溶液变红,继续滴加H2O2,红色逐渐褪去,且有气泡产生。呈红色的物质是?(写化学式)。
已知:11H2O2+2SCN―→2SO42―+2CO2↑+ N2↑+10H2O +2H+若生成1mol N2,H2O2和SCN―的反应中转移电子物质的量是?mol。
(3)由以上实验,推断Fe2+、S2―和SCN―的还原性强弱?(按从强到弱顺序排列)。
(4)向FeCl3溶液中加入KOH溶液至过量,微热,再通入Cl2,可观察到溶液呈紫色(高铁酸钾:K2FeO4)。写出此过程的离子方程式、配平并标出电子转移的数目和方向?。
参考答案:(1)取样,在样品中滴加酸性高锰酸钾溶液,若紫色褪去,则说明亚铁离子有剩余;(2分);2Fe3++S2―→2Fe2+ +S↓;
(2)Fe(SCN)3 (合理即可);22
(3)S2―>Fe2+>SCN―
(4) (方程式1分,方向和数目1分)
(方程式1分,方向和数目1分)
本题解析:(1)Fe2+ 有还原性,Fe3+ 有较强还原性,所以要检验Fe2+ 可以加入有颜色变化的氧化剂,所以可以往样品中加入酸性高锰酸钾溶液,若紫色褪去,则说明Fe2+ 有剩余;而因为Fe3+ 的氧化性,所以加入还原性的Na2S,S2― 被氧化为S单质析出淡黄色沉淀,离子方程式为2Fe3++S2―=2Fe2+ +S↓。
(2)Fe2+?被加入的氧化剂H2O2 氧化为Fe3+ ,所以生成铁离子与加入的SCN-发生络合反应,生成红色的Fe(SCN)3;由于加入的H2O2和SCN―发生氧化还原反应,H2O2 中的O化合价从-1价→-2价,S化合价-2→+6、N化合价-3→0价,所以从化合价升降可以判断H2O2 为氧化剂,当生成1mol N2 ,消耗H2O2 11mol,转移22mol电子。
(3)根据氧化还原规律,由上述几个反应可知Fe3+ 可以氧化S2― ,而不能氧化SCN― ,还原性S2―>SCN―同样Fe2+ 不能氧化SCN― ,所以可知三者还原性S2―>Fe2+>SCN― 。
(4)向FeCl3溶液通入强氧化性的氯气,生成了紫色的高铁酸钾,铁的化合价升高,铁元素被氧化,在碱性溶液中发生氧化还原反应,根据电子的是守恒配平得方程式为: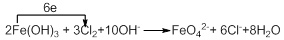 。
。
本题难度:困难
3、选择题 下列工业生产过程中,不涉及氧化还原反应的是
A.用S制备H2SO4
B.炼铁时用CaO除去原料中的SiO2
C.将海水中的MgSO4转变为金属Mg
D.用NO2生产HNO3
参考答案:B
本题解析:氧化还原反应的特征是化合价的升降,即凡是有元素化合价升降的反应都是氧化还原反应。氧化钙和二氧化硅反应属于化合反应,化合价没有变化,是非氧化还原反应。答案选B。
本题难度:简单
4、选择题 As2S3和As2O3物质相似,均具有还原性;Na2S2和Na2O2性质相似,均具有氧化性,当As2S3与Na2S2相互反应时,生成的盐可能是:
[? ]
A、NaAsS3?
B、Na2AsS4?
C、Na3AsS3?
D、Na3AsS4?
参考答案:AD
本题解析:
本题难度:一般
5、选择题 已知M2O7x一+3S 2一+14H+ ====2M3++3S↓+7H2O,则M2O7x一中的M的化合价为
A.+2
B.+3
C.+4
D.+6
参考答案:D
本题解析:该反应是离子反应型的氧化还原反应,可以根据电荷守恒计算,可以得到式子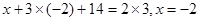 ,x=-2,则M2O72-,假设M的化合价为y,则有
,x=-2,则M2O72-,假设M的化合价为y,则有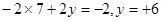 ,所以答案选D。
,所以答案选D。
本题难度:简单