��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� (14��)
A��H�Ǵ��������Һ�е����ʣ�����A���ճ������г��õĽ������ʣ�����֮�������¹�ϵ��(���ֲ���ͷ�Ӧ������)
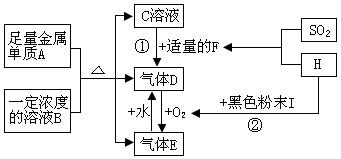
����������Ϣ���ش��������⣺
��1��д���������ʵĻ�ѧʽB?��E?��
��2��H�� SO2����ǿ��F���˷�Ӧ����������?.
��3��д���ٵ����ӷ���ʽ��?.
��4��д���ڵĻ�ѧ����ʽ��?.
��5��C��Һ�е���NaOH��Һ�к�����?.
�ο��𰸣�
(1) HNO3��NO2������2�֣�
(2) H2O2��2�֣�
(3) 3 Fe2++4H++NO3-="3" Fe3++NO��+2H2O����3�֣�
(4) 2H2O2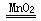 2H2O+O2����3�֣�
2H2O+O2����3�֣�
(5) �Ȳ�����ɫ������Ȼ��Ѹ�ٱ�Ϊ����ɫ������Ϊ���ɫ��������2�֣�
�����������
�����Ѷȣ���
2������� A��B��C��D�����ɶ�����Ԫ����ɵij������ʣ�����A��B��C����ͬһ��Ԫ�أ���һ���������ת������ͼ��ʾ�����ֲ�������ȥ����
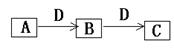
�밴Ҫ��ش��������⣺
��1����B��C Ϊ�����C�ܹ���ˮ��Ӧ����һ��ǿ��E��
�ٵ�BΪ��ɫ������ˮ�Ĵ̼�������ʱ��д��Bת��ΪC�Ļ�ѧ����ʽ��?��
�ڵ�BΪ��ɫ������ˮ������ʱ�� F��A��E�������ɡ���С�ļ���Fʱ���ɵõ�һ����ɫ��ζ������G(G��CO2������ͬ��ԭ����Ŀ�͵�����Ŀ)��һ����ɫ��ζ��Һ��H��д��F�ֽ�����G��H�Ļ�ѧ����ʽ?��
��2����DΪ�����A��B��C����ǿ����ʣ�C������ʳƷ���͡���ĭ���д��A��D��Ӧ�����ӷ���ʽ��?��
��3����DΪǿ���ǿ����Һʱ���ܷ���ͼʾת����ϵ����A��C����Һ�з�Ӧ���ɰ�ɫ����B��
��DΪǿ��ʱ��A��B��Ӧ�����ӷ���ʽ��?��
��DΪǿ��ʱ��B��C��Ӧ�����ӷ���ʽ��?��
�ο��𰸣�(1)��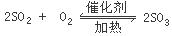 �� NH4NO3
�� NH4NO3 N2O��+2H2O? (2)2OH-+CO2=CO32-+H20
N2O��+2H2O? (2)2OH-+CO2=CO32-+H20
(3)AlO2-+H++H2O=Al(OH)3����[Al(OH)4] -+H+=Al(OH)3��+H2O
Al(OH)3+OH-=AlO2-+2H2O ��Al(OH)3+OH-=[Al(OH)4] -����
�����������1��������ͼ�������ʼ�Ĺ�ϵ�����B��C Ϊ�����C�ܹ���ˮ��Ӧ����һ��ǿ��E��˵��A��B��C�����е�Ԫ���Ƿǽ���Ԫ�ء�����Ҫ��Ŀ������Ϊ��S��SO2��SO3;��N2��NO��NO2.��NH3-- NO��NO2. ��H2S��SO2��SO3.�ٵ�BΪ��ɫ������ˮ�Ĵ̼�������ʱ��ֻ�Тٷ���Ҫ�� Bת��ΪC�Ļ�ѧ����ʽ��2SO2+O2 2SO3���ڵ�BΪ��ɫ������ˮ������ʱ�� F��A��E�������ɡ���С�ļ���Fʱ���ɵõ�һ����ɫ��ζ������G(G��CO2������ͬ��ԭ����Ŀ�͵�����Ŀ)��һ����ɫ��ζ��Һ��H��˵���ǵ������NH3-- NO��NO2.A��NH3��EΪHNO3��FΪNH4NO3��ɫ��ζ������G��N2O����ɫ��ζ��Һ��H��ˮ��F�ֽ�����G��H�Ļ�ѧ����ʽ��NH4NO3 = N2O��+2H2O����2�� ��ΪDΪ�����A��B��C����ǿ����ʣ�C������ʳƷ���͡���ĭ��𡣿�֪CΪС�մ�̼�����ƣ�BΪ�մ�̼���ơ�AΪ�������ƣ�DΪ������̼��д��A��D��Ӧ�����ӷ���ʽΪ��2OH-+CO2=CO32-+H20��(3)��DΪǿ�ᣬ����Ӧ�ĸ��������������ֱ���ƫ�����Ρ��������������Σ�A��B��Ӧ�����ӷ���ʽ��AlO2-+H++H2O=Al(OH)3����DΪǿ����Һʱ������Ӧ�ĸ��������������ֱ������Ρ�����������ƫ�����Ρ�B��C��Ӧ�����ӷ���ʽ��Al(OH)3+OH-=AlO2-+2H2O��
2SO3���ڵ�BΪ��ɫ������ˮ������ʱ�� F��A��E�������ɡ���С�ļ���Fʱ���ɵõ�һ����ɫ��ζ������G(G��CO2������ͬ��ԭ����Ŀ�͵�����Ŀ)��һ����ɫ��ζ��Һ��H��˵���ǵ������NH3-- NO��NO2.A��NH3��EΪHNO3��FΪNH4NO3��ɫ��ζ������G��N2O����ɫ��ζ��Һ��H��ˮ��F�ֽ�����G��H�Ļ�ѧ����ʽ��NH4NO3 = N2O��+2H2O����2�� ��ΪDΪ�����A��B��C����ǿ����ʣ�C������ʳƷ���͡���ĭ��𡣿�֪CΪС�մ�̼�����ƣ�BΪ�մ�̼���ơ�AΪ�������ƣ�DΪ������̼��д��A��D��Ӧ�����ӷ���ʽΪ��2OH-+CO2=CO32-+H20��(3)��DΪǿ�ᣬ����Ӧ�ĸ��������������ֱ���ƫ�����Ρ��������������Σ�A��B��Ӧ�����ӷ���ʽ��AlO2-+H++H2O=Al(OH)3����DΪǿ����Һʱ������Ӧ�ĸ��������������ֱ������Ρ�����������ƫ�����Ρ�B��C��Ӧ�����ӷ���ʽ��Al(OH)3+OH-=AlO2-+2H2O��
�����Ѷȣ�һ��
3������� ͼ��A��Z��һ�������µ�ת����ϵ�����ַ�Ӧ������δ�г��������У�A�������й㷺ʹ�õĽ������ʣ�������C��һ�ֳ���Һ�廯���E��F��X��Ϊ���壮����Y��Na2AO4����ǿ�����ԣ�������ɱ��������Z��һ�ֺ��ɫ���壮
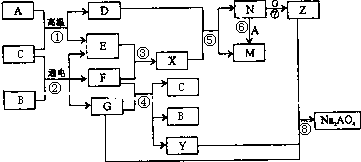
��ش��������⣺
��1��Y�ĵ���ʽΪ______��
��2���ڢ١���������������ԭ��Ӧ�����ֲ��ǻ��Ϸ�Ӧ����______������ţ���
��3����Ӧ�ݵ����ӷ���ʽ��______��
��4�����ڷ�Ӧ����ת�Ƶ�����Ϊ2NA�������ĵ�F�ڱ�״���µ������______L��
��5����Ӧ��Ļ�ѧ����ʽ��______��
�ο��𰸣�A�������й㷺ʹ�õĽ������ʣ�������C��һ�ֳ���Һ�廯���E��F��X��Ϊ���壮���ת����ϵ�ͷ�Ӧ�����������ƶϣ�A+C=D+E�ķ�Ӧ������ˮ���������ķ�Ӧ��B+Cͨ����õ�EFG��EFΪ���壬�ж��ǵ��ʳ��ˮ�ķ�Ӧ��CΪH2O��BΪNaCl��AΪFe��EΪH2��FΪCl2��GΪNaOH��DΪFe3O4��XΪHCl��NΪFeCl3��MΪFeCl2��ZΪFe��OH��3��
ת����ϵ�еķ�Ӧ��F��Cl2��+G��NaOH��=C��H2O��+B��NaCl��+Y��NaClO�����ж�YΪNaClO��
��1��YΪNaClO����ʽΪ��
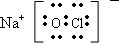
���ʴ�Ϊ��
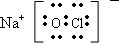
��
��2���ڢ١���������������ԭ��Ӧ�����ֲ��ǻ��Ϸ�Ӧ���ǣ���������ˮ�����������û���Ӧ����������ԭ��Ӧ���ڵ���Ȼ�����������ԭ��Ӧ�����ǻ��Ϸ�Ӧ����������������Ӧ�����Ȼ��⣬��������ԭ��Ӧ�����ڻ��Ϸ�Ӧ�������������������Ʒ�Ӧ��������ԭ��Ӧ�����ǻ��Ϸ�Ӧ���������������������ᷴӦ������������ԭ��Ӧ���ǻ��Ϸ�Ӧ�������Ȼ���������Ӧ�����Ȼ���������������ԭ��Ӧ���ǻ��Ϸ�Ӧ�����Ȼ������������Ʒ�Ӧ�Ǹ��ֽⷴӦ������������ԭ��Ӧ�����ǻ��Ϸ�Ӧ�����������ڢܢ���ϣ�
�ʴ�Ϊ���٢ڢܢࣻ
��3����Ӧ�������������������ᷴӦ����Ӧ�����ӷ���ʽ��Fe3O4+8H+=2Fe3++Fe2++4H2O���ʴ�Ϊ��Fe3O4+8H+=2Fe3++Fe2++4H2O��
��4����Ӧ����Cl2+2NaOH=NaCl+NaClO+H2O��1molCl2��Ӧ������ת��1mol����Ӧ��ת�Ƶ�����Ϊ2NA����Ӧ������Ϊ2mol�������ĵ�F��Cl2���ڱ�״���µ����Ϊ44.8L��
�ʴ�Ϊ��44.8��
��5����Ӧ�����������ơ����������ʹ������Ʒ����ķ�Ӧ����Na2FeO4����Ԫ�ػ��ϼ����ߣ�������������ԭ������������������������ԭΪ�����ӣ�����ԭ���غ���ƽд��
�Ļ�ѧ����ʽ�ǣ�2Fe��OH��3+4NaOH+3NaClO=Na2FeO4+3NaCl+5H2O���ʴ�Ϊ��2Fe��OH��3+4NaOH+3NaClO=Na2FeO4+3NaCl+5H2O��
���������
�����Ѷȣ�һ��
4������� ����X��Y��Z����Ԫ�أ���֪�����������
��X��Y��Z�ĵ����ڳ����¾�Ϊ���壮
��X�ĵ�����Z�ĵ�����ȼ�գ�����XZ��ȼ��ʱ����ʲ�ɫ��
��XZ��������ˮ����ˮ��Һ�е����X+��Z-��XZ��ˮ��Һ��ʹʯ����Һ��죮
��������X�ĵ��ʿ���һ����Y�ĵ��ʻ�������������X2Y��X2Y������ΪҺ�壮
��Z�ĵ�������X2Y�У�������Һ����Ư�����ã�
������������⣺
��1��д��XZ��X2Y�Ļ�ѧʽ��XZ______��?X2Y______
��2��д��X�ĵ�����Z�ĵ�����ȼ�յĻ�ѧ����ʽ______��
��3��Z�ĵ����ܷ�������������Һ������Ӧ��______����ܡ��������ܣ���д����Ӧ�Ļ�ѧ����ʽ��______���������ܷ�Ӧ����˿ղ�����д����
�ο��𰸣�X�ĵ�����Z�ĵ�����ȼ�գ�����XZ��ȼ��ʱ����ʲ�ɫ������XZ��������ˮ����ˮ��Һ�е����X+��Z-��XZ��ˮ��Һ��ʹʯ����Һ��죬˵��XΪH2��ZΪCl2��XZΪHCl��
������X�ĵ��ʿ���һ����Y�ĵ��ʻ�������������X2Y��X2Y������ΪҺ�壬˵��YΪO2��X2YΪH2O��Cl2����H2O�У���Ӧ����HCl��HClO��HClO����Ư�����ã�
��1�������Ϸ�����֪��XZΪHCl��X2YΪH2O���ʴ�Ϊ��HCl��?H2O��
��2��H2��Cl2��ȼ������HCl����Ӧ����ʽΪH2+Cl2?��ȼ?.?2HCl���ʴ�Ϊ��H2+Cl2?��ȼ?.?2HCl��
��3��Cl2��NaOH��Һ�з���������ԭ��Ӧ����NaCl��NaClO��H2O����Ӧ�Ļ�ѧ����ʽΪCl2+2NaOH�TNaCl+NaClO+H2O��
�ʴ�Ϊ���ܣ�Cl2+2NaOH�TNaCl+NaClO+H2O��
���������
�����Ѷȣ�һ��
5���ƶ��� ��ͼ��һЩ�������ʡ�������֮���ת����ϵͼ����Щ��Ӧ�еIJ������ʼ���Ӧ��������ȥ��A��B���Ԫ����ͬ���ڳ����¶�����ɫҺ�塣D��E�����Ԫ����ͬ��I��K�����Ԫ����ͬ��I�ڳ���������ɫ�ж����壬J�Ǻ�ɫ��ĩ��G��һ�ֺ�ɫ�������ʡ�

��1��A�Ļ�ѧʽ��?�� ��2��B�ĵ���ʽ��?��
��3��I��J��Ӧ�Ļ�ѧ����ʽΪ?��
��4����D����ɫ���壬�ҳ�������������Ϊ����ɫ���壬��G��F��Ӧ�����ӷ���ʽΪ
?��
�ο��𰸣���8�֣���1�� H2O2?��2��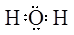 ��3��CuO? +? CO
��3��CuO? +? CO Cu? +? CO2?
Cu? +? CO2?
��4��3 Cu ?+ 8H+ +2NO3-�� 3 Cu2+ +2NO�� + 4 H2O?����2�֣�
���������A��B���Ԫ����ͬ���ڳ����¶�����ɫҺ�壬��˵��Ӧ����ˮ��˫��ˮ��A�ܺͶ������̷�Ӧ������A��˫��ˮ��B��ˮ��C��������I��K�����Ԫ����ͬ��I�ڳ���������ɫ�ж����壬J�Ǻ�ɫ��ĩ��G��һ�ֺ�ɫ�������ʣ����I��CO��J������ͭ��G��ͭ��K��CO2��D��E�����Ԫ����ͬ�����D������NO,E��NO2������F�����ᡣ����DҲ�����Ƕ�������E����������F�����ᡣ
�����������Ǹ߿��еij������ͣ������е��Ѷȵ����⡣�����ۺ���ǿ���������С���Ҫ�ǿ���ѧ���������仯�������ʺ�ת������Ϥ���ճ̶ȣ�����������ѧ���������������淶����������Ҳ���������ѧ����Ӧ��������ѧϰЧ�ʡ�����������Ҫע����ǻ�ѧ�ƶ�����һ���ۺ��Խ�ǿ�����⣬��Ԫ�ؼ����������ʺ�������������������ѧ�����֪ʶ����������ѧ�Ƽ��ۺϡ��������ɿ���ѧ���Ի�ѧ֪ʶ������̶ȣ�����Ҫ��������ѧ�����ۺϷ���������˼ά���������ͼ��ķ�������ؼ�����Ѱ�ҡ�ͻ�ƿڡ�����ͻ�ƿڡ�����ץ���ء��֣�����������ɫ������״̬��������ζ�����ⷴӦ���������������Ʒ���������;�ȡ�
�����Ѷȣ�һ��