��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ����˵����ȷ���ǣ�? ��
A����Ҫ���ȵĻ�ѧ��Ӧ�������ȷ�Ӧ
B��CO2�����ں��м��Լ�������CO2�����Ǽ��Է���
C��ͬ���칹��֮���ת�����������仯
D��1mol�������辧���к�Si-O��Ϊ4mol
�ο��𰸣�D
���������
�����Ѷȣ�һ��
2������� ��11�֣�A��B��C��D��E��F���ֶ�����Ԫ�ص�ԭ��������������A�������к������Ԫ�أ�BԪ�ص�ԭ�Ӽ۵����Ų�Ϊnsnnpn��DԪ�ص�����������������Ӳ�����3����F������������Ӧˮ���������ԣ�������C��E������������Ӧˮ�����С��Իش�
��1��д��Cԭ�ӵļ۲���ӹ����ʾʽ��������������������������Dԭ�ӵļ۲�����Ų�ʽ��___________��E��ԭ�ӽṹʾ��ͼ��___________��
��2��Bλ��Ԫ�����ڱ��ĵ�?�壬A��B�γ�ԭ�Ӹ�����1:1��ֱ���η��ӵĽṹʽ����������������
��3��C�Ļ�̬ԭ�Ӻ������������ֲ�ͬ�˶�״̬�ĵ��ӣ�
��4��E�����ڿ�����ȼ��������ĵ���ʽ���������������������е��������������ӵĸ�������������������
��5��F�Ĺ�̬���������;��________������___��˵��һ�֣���F�ĵ��ʡ�ʯī�Ͷ������ѣ�TiO2����������ϣ������·�Ӧ�õ������ֻ������������Ԫ����ɣ��Ҷ��������մɲ��ϣ��ڻ���͵���������ҪӦ�ã����䷴Ӧ�Ļ�ѧ����ʽ��?����?��
�ο��𰸣���11�֣������һ��2�֣�����ÿ��1�֣�
��N��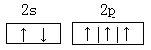 ��O��2s22p4��Na��
��O��2s22p4��Na��
�� IVA��H��C��C��H��
��7����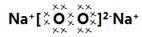 ��2:1��
��2:1��
���ͻ���ϣ�ש�����������ұ�����ȡ�4Al��3TiO2��3C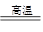 2Al2O3��3TiC
2Al2O3��3TiC
�������������Ԫ�ص����ʼ��ṹ��֪��A��B��C��D��E��F���ֶ�����Ԫ�طֱ���H��C��N��O��Na��Al��
��1�����ݹ���ԭ����֪����ԭ�ӵļ۲���ӹ����ʾʽΪ ����ԭ�ӵļ۵��ӵĵ����Ų�ʽΪ2s22p4����ԭ�ӵĽṹʾ��ͼΪ
����ԭ�ӵļ۵��ӵĵ����Ų�ʽΪ2s22p4����ԭ�ӵĽṹʾ��ͼΪ ��
��
��2��̼Ԫ��λ�ڵ� IVA��A��B�γ�ԭ�Ӹ�����1:1��ֱ���η�������Ȳ���ṹʽΪH��C��C��H��
��3����ԭ�Ӻ�����7�����ӣ�����7�ֲ�ͬ�˶�״̬�ĵ��ӡ�
��4����ȼ�����ɹ������ƣ�����ʽΪ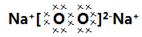 �����е��������������ӵĸ�����2�U1��
�����е��������������ӵĸ�����2�U1��
��5�����������۵�ߣ������ͻ���ϣ�ש�����������Ҳ��ұ�����ȡ�����ԭ���غ��֪������ʽΪ4Al��3TiO2��3C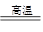 2Al2O3��3TiC��
2Al2O3��3TiC��
�����Ѷȣ�һ��
3��ѡ���� ���и����б�����ȷ����
[? ]
A��F-�Ľṹʾ��ͼ��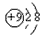
B��CO2�ķ���ģ��ʾ��ͼ��
C��NaCl�ĵ���ʽ��
D��N2�Ľṹʽ��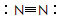
�ο��𰸣�A
���������
�����Ѷȣ���
4������� ��Ȼ������������������ȤҲʮ��������������±��г������ɻ�����Ľṹʽ������ʽ����Է��������ͷе㡣
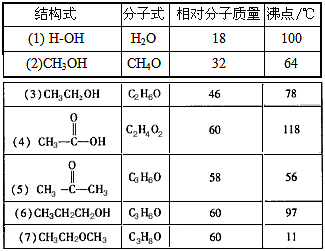
�ɱ������ʵķе���Եó�ʲô���ۣ�
_________________________________________
�ο��𰸣�(1)��ɺͽṹ���ƵĻ������Է�������Խ�е�Խ�ߣ�
(2)���Ӽ�����������ʹ�е����ߣ����Խǿ���е�Խ�ߡ�
���������
�����Ѷȣ�һ��
5������� ��5�֣���VSEPRģ�ͺ��ӻ�����������֪ʶ�����
���ӻ�����
| �¶Ե��Ӷ���
| VSEPRģ������
| ����ԭ���ӻ��������
| ���ӻ����ӵ����幹������
|
CH4
| 0
| ����������
| sp3
| ����������
|
BeCl2
| ?
| ?
| ?
| ?
|
SO2
| ?
| ?
| ?
| ?
|
CH3+
| ?
| ?
| ?
| ?
|
SO42��
| ?
| ?
| ?
| ?
|
NCl3
| ?
| ?
| ?
| ?
�ο��𰸣���5�֣�
���ӻ�����
�¶Ե��Ӷ���
VSEPRģ������
����ԭ���ӻ��������
���ӻ����ӵ����幹������
CH4
0
����������
sp3
����������
BeCl2
0
ֱ����
sp
ֱ����
SO2
1
ƽ��������
sp2
V��
CH3+
0
ƽ��������
sp2
ƽ��������
SO42��
0
����������
sp3
����������
NCl3
1
��������
sp3
������
������������ݼ۲���ӶԻ������ۿ�֪������֪̼ԭ�Ӻ��еŶԵ��Ӷ����ǣ�4��1��4����2��0�����Լ�����ӵĹ��������������Σ�����̼ԭ����sp3�ӻ���BeCl2��Beԭ�Ӻ��еŶԵ��Ӷ����ǣ�2��1��2����2��0�������ֱ���ͽṹ������sp�ӻ���SO2����ԭ�Ӻ��еŶԵ��Ӷ����ǣ�6��2��2����2��1����SO2��V�νṹ����sp2�ӻ���CH3+��̼ԭ�Ӻ��еŶԵ��Ӷ����ǣ�4�D1�D1��3����2��0�������ƽ�������νṹ������sp2�ӻ���SO42������ԭ�Ӻ��еŶԵ��Ӷ����ǣ�6��2��2��4����2��0�����������������Σ�����sp3�ӻ���NCl3�е�ԭ�Ӻ��еŶԵ��Ӷ����ǣ�5��1��3����2��1����˽ṹ�������Σ�����sp3�ӻ�
�����Ѷȣ�һ��
|