��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� �Ҷ����������ᣬij��ѧѧϰС���ͬѧ��̽���ⶨ���ᾧ�壨H2C2O4?xH2O����xֵ��ͨ���������ϸ�С��ͬѧͨ�������ѯ�ã�����������ˮ��ˮ��Һ����������KMnO4��Һ���еζ���
2MnO4-+5H2C2O4+6H+=2Mn2++10CO2��+8H2O
����ͬѧ����˵ζ��ķ����ⶨxֵ��
�ٳ�ȡ1.260g�����ᾧ�壬�������Ƴ�100.00mLˮ��ҺΪ����Һ��
��ȡ25.00mL����Һ������ƿ�У��ټ���������ϡH2SO4
����Ũ��Ϊ0.1000mol/L��KMnO4����Һ���еζ����ﵽ�յ�ʱ����10.00mL��
��ش�
��1���ζ�ʱ����KMnO4��Һװ����ͼ�е�______����ס����ҡ����ζ����У�
��2����ʵ��ζ��ﵽ�յ�ı�־��______��
��3��ͨ���������ݣ������x=______��
���ۣ������ζ��յ�ʱ���ӵζ��̶ܿȣ����ɴ˲�õ�xֵ��______���ƫ����ƫС�����䡱����ͬ����
�����ζ�ʱ���õ�KMnO4��Һ����ö�����Ũ�ȱ�С�����ɴ˲�õ�xֵ��______��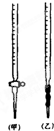
�ο��𰸣���1����ΪKMnO4����ǿ�����ԣ��ḯʴ�ܣ���Ӧ����ʽ�ζ���ʢװ���ʴ�Ϊ���ף�
��2��������KMnO4��Һ��������ɫ��Ϊָʾ���жϵζ��յ�ʱ���ٵμ�KMnO4��Һʱ����Һ������ɫ��Ϊ��ɫ��
�ʴ�Ϊ�����������һ��KMnO4��Һʱ����Һ����ɫ��Ϊ��ɫ���Ұ�����ڲ���ɫ������ζ��յ㣻
��3���������ѧ����ʽ�����ݿ�֪��1.260g�����ᾧ���к�H2C2O4�����ʵ���Ϊ��0.100 0 mol/L��10.00 mL��10-3 L/mL��52��100 mL25 mL=0.0100 mol��
��1.260 g H2C2O4?xH2O�к�H2O�����ʵ���Ϊ1.260 g-0.010 0 mol��90 g/mol18 g/mol=0.020 0 mol����x=2��
���ζ��յ�ʱ���ӵζ��ܶ�������������������KMnO4��Һ�����ƫС���ɴ�����n��H2C2O4��ƫС����n��H2O��ƫ��xƫ��
ͬ������KMnO4��Һ���ʣ������������ƫ������xֵƫС��
�ʴ�Ϊ��2��ƫ��ƫС��
���������
�����Ѷȣ�һ��
2������� �Ҷ��ᣨHOOC-COOH���������ᣬ������ˮ�����ڶ�Ԫ��ǿ�ᣬ�����Ϳ�ѧʵ�������Ź㷺����;�����ᾧ�����ɿ���H2C2O4-xH2O��ʾ��Ϊ�˲ⶨxֵ����������ʵ�飺��ȡWg���ᾧ�壬���100.00mLˮ��Һ����ȡ25.00mL�����ƵIJ�����Һ������ƿ�ڣ���������ϡH2SO4����Ũ��Ϊamol-L-1��KMnO4��Һ�ζ���
��1�����������ķ�Ӧ����ʽ��ɲ���ƽ���������Ļ�ѧ����ʽд�ڴ���ϣ�
? KMnO4+H2C2O4+______�TK2SO4+CO2��+MnSO4+______
��2������ʵ������в���Ҫ��������______������ţ���
a��������ƽ�������룬���ӣ�b����ʽ�ζ���?c����ƿ? d��100mL����ƿ?e���ձ�?f��©��?g����ƿ
h��������?i��ҩ��
��3��ʵ���У���KMnO4��ҺӦʢװ��______ʽ�ζ����У��ζ��յ�ʱ��Һ����ɫ�仯Ϊ______��
��4���ڵζ�����������ȥamol-L-1��KMnO4��ҺVmL���������ƵIJ�����Һ�����ʵ���Ũ��Ϊ______mol-L-1���ɴ˿ɼ���x��ֵ��______�����ú�W��a��V�Ĵ���ʽ��ʾ��
��5����С��ͬѧ��0.02mol���ᾧ�壨H2C2O4-2H2O�����뵽100mL0.2mol/L��NaOH��Һ�г�ַ�Ӧ����÷�Ӧ����Һ�����ԣ������Һ�и�����Ũ���ɴ�С��˳��Ϊ______��
�ο��𰸣���1����Ӧ�и�����������ʧ�����غ��֪�������ͻ�ԭ�����ʵ���֮��Ĺ�ϵΪ��2MnO4-��5H2C2O4���ڸ��ݵ���غ�������غ��д����Ӧ����ʽΪ��2KMnO4+5?H2C2O4+3H2SO4�TK2SO4+10CO2��+2?MnSO4+8H2O���ʴ�Ϊ��2KMnO4+5?H2C2O4+3H2SO4�TK2SO4+10CO2��+2?MnSO4+8H2O��
��2������Ϊ������ȷŨ�ȵIJ�����Һ������Ҫ��ʵ��������Ҫ����ƽ�������룩���ձ���ҩ�ס�100mL����ƿ����ͷ�ιܡ��������ȣ����ø��������Һ���еζ����������ʵ���������Ҫ��ʵ��������Ҫ���ձ�����ʽ�ζ��ܡ�����̨�����ζ��ܼУ�����ƿ�ȣ��ʴ�Ϊ��c��f��
��3��KMnO4��Һ����ǿ�����ԣ����Ը�ʴ��Ƥ�ܣ���KMnO4��ҺӦװ����ʽ�ζ����У��ζ�ʱ�����ֿ��Ƶζ��ܻ���������ҡ����ƿ���۾�ע����Һ��ɫ�ı仯��KMnO4��Һ����ɫ�����ᷴӦ��ϣ��������һ��KMnO4��Һ����ɫ����ȥ��˵���ζ����յ㣬����Ҫ���ָʾ�����ʴ�Ϊ�������Һ����ɫ��Ϊdz��ɫ�Ұ���Ӳ���ɫ��
��4��2KMnO4 ��5H2C2O4
?2mol? 5mol
aV��10-3mol? 0.025��Cmol
2molaV��10-3mol=5mol0.025��Cmol
��ã�C=0.1aVmol?L-1
H2C2O4?xH2O��H2C2O4 ��xH2O
? 1mol? 18xg
?0.1aV��0.1 ?w-0.1aV��0.1��90?
1mol0.1aV��0.1=18xgw-?0.1aV��0.1��90
���X=50w9av-5
�ʴ�Ϊ��0.1aV��50w9av-5��
��5����������1��1��Ӧ����NaHC2O4����Һ������˵��HC2O4-�ĵ���̶ȴ�����ˮ��̶ȣ�����Һ�л�������ˮ�ĵ��룬��H+��C2O42-���������ӵĵ���̶Ƚ�С������HC2O4-��H+������ȷ˳��ΪNa+��HC2O4-��H+��C2O42-��OH-���ʴ�Ϊ��C��Na+����c��HC2O4-����c��H+����c��C2O42-����c��OH-����
���������
�����Ѷȣ���
3��ѡ���� �ñ�������ζ�δ֪Ũ�ȵ�NaOH��Һʱ�����и������У��������ǣ�������
A��������ˮϴ����ʽ�ζ��ܺ�ע�����Һ������еζ�
B��������ˮϴ����ƿ������NaOH��Һ��ϴ������װ��һ�������NaOH��Һ���еζ�
C���ü�ʽ�ζ�����ȡ10.00mLNaOH��Һ����������ˮϴ�Ӻ����ƿ�У��ټ�����������ˮ��2�μ�����Һ����еζ�
D����������Һ��ȡ����Һ10.00mLNaOH��Һ������ƿ��������Һ�ܼ��촦��Һ�崵����ƿ�ڣ��ټ���1mL����ָʾ������еζ�
�ο��𰸣�C
���������
�����Ѷȣ���
4��ѡ���� ����֪Ũ�ȵ�����ζ�δ֪Ũ�ȵ�NaOH��Һʱ�����в�������ȷ����
[? ]
A. ��ʽ�ζ���������ˮϴ����ֱ�Ӽ�����֪Ũ�ȵ�����
B. ʢNaOH��Һ����ƿ�ζ�ǰ��NaOH��Һ��ϴ2��3��
C. ʵ���������ʽ�ζ��ܼ��������û�����
D. ����ʱ��������ζ�����Һ�尼Һ����ʹ�����ˮƽ
�ο��𰸣�D
���������
�����Ѷȣ�һ��
5��ѡ���� �����ǹ�������֪Ũ������ζ�δ֪Ũ������������Һ������к͵ζ�ʵ�������������
��ȡһ��ƿ���ô���NaOH��Һ��ϴ���Σ�
����һ��ƿ�м���25.00mL����NaOH��Һ��
�ۼ��뼸��ʯ���Լ���ָʾ����
��ȡһ֧��ʽ�ζ��ܣ�ϴ�Ӹɾ���
��ֱ������ʽ�ζ�����ע�������Һ�����еζ���
��������ת�ζ��ܵIJ������������ֲ�ͣҡ����ƿ��
������ע���ŵζ�����������ҺҺ���½���ֱ���ζ��յ㣮
�������������д�������Ϊ��������
A���٢ۢݢ�
B���٢ݢޢ�
C���ۢݢ�
D���ܢޢ�
�ο��𰸣�A
���������
�����Ѷȣ�һ��