��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ��ij�о�С��Ϊ��̽��һ����������X(��������Ԫ��)����ɺ����ʣ���Ʋ��������ʵ�飺
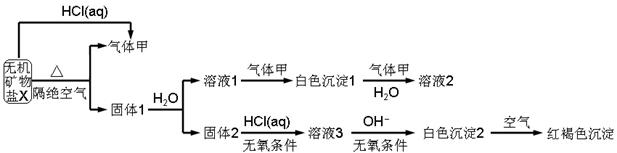
��ȡ10.80gX�ڶ��������м�������ȫ�ֽ⣬�õ�6.40g����1.��ش��������⣺
��1��������ɫ����1�н���Ԫ�ص�ԭ�ӽṹʾ��ͼ_______��д������ĵ���ʽ_______��
��2��X�Ļ�ѧʽ��______���ڶ��������м���X����ȫ�ֽ�Ļ�ѧ��Ӧ����ʽΪ_______��
��3����ɫ����2�ڿ����б�ɺ��ɫ������ԭ����_______(�û�ѧ��Ӧ����ʽ��ʾ)��
��4��һ�������£�����������1�е�ij�ֳɷֿ��ܷ���������ԭ��Ӧ��д��һ�����ܵĻ�ѧ��Ӧ����ʽ_______�������ʵ�鷽����֤�÷�Ӧ�IJ���_______��
�ο��𰸣���1�� ?
?
��2��CaFeC2O6(��CaCO3��FeCO3)��CaCO3��FeCO3��CaO+FeO+2CO2����
��3��4Fe(OH)2+O2+2H2O===4Fe(OH)3
��4��3FeO+CO2===Fe3O4+CO���鷽����Fe2O3����������������ܽ⣬�ٵ���KSCN��Һ����Һ��Ѫ��ɫ��CuO����������������ܽ⣬�ٵ��백ˮ��Һ����Һ������ɫ�������������백ˮ�������ܽ⣬��������ɫ��Һ��
�����������ɫ����2�ڿ����б�ɺ��ɫ����˵����ɫ����2��Fe(OH)2����Һ1��ͨ������壬�а�ɫ����1����ͨ�������(ע�⣺ˮ����ʱ)���ܽ⣬�����������������壬����X�����1������ȷ����CO2��
�����Ѷȣ�һ��
2��ѡ���� �����£�����Ƭ����������Һ�У������Թ۲쵽������������ǣ�������
A��Ũ����
B��ϡ����
C��ZnSO4��Һ
D��CuSO4��Һ
�ο��𰸣�A�������£�����Ƭ����Ũ����ᷢ���ۻ��������������γ�һ�������ܵ��������ֹ��Ӧ���У���A�����ϣ�
B�������£�����Ƭ����ϡ���ᷴӦ����������������������B���ϣ�
C�������£�����Ƭ����ZnSO4��Һ�У����ݽ����˳����жϣ���������Ӧ����C�����ϣ�
D�������£�����Ƭ����CuSO4��Һ�У���Ӧ����ͭ��������������D�����ϣ�
��ѡB��
���������
�����Ѷȣ���
3��ʵ���� ��12�֣�ʵ����������װ�òⶨFeO��Fe2O3����������Fe2O3��������Dװ�õ�Ӳ��˫ͨ�������еĹ���������FeO��Fe2O3�Ļ���
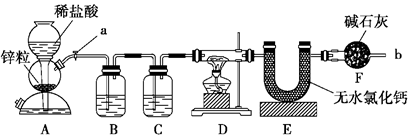
(1)��μ��װ��A�������ԣ�
?_
(2)װ��A�����ķ�Ӧ��ʱҪ�����м�������CuSO4��Һ����Ŀ����?��
��ԭ����?��
(3)Ϊ�˰�ȫ���ڵ�ȼD���ľƾ���֮ǰ����b���ڴ�����?��
(4)װ��B��������?��
װ��C��װ��Һ����?�������������?��
(5)����������ã����ҽ����˱�Ҫ�İ�ȫ������ȼD���ľƾ��ƣ���Ӳ��˫ͨ�������з�����Ӧ�Ļ�ѧ����ʽ��?��
(6)��FeO��Fe2O3�������������Ϊ23.2 g����Ӧ��ȫ��U�ܵ���������7.2 g����������Fe2O3������Ϊ?g��
(7)U�ι�E�ұ������Ӹ����F��Ŀ����?���������F�����Fe2O3��������?(�ƫ����ƫС������Ӱ�족)��
(8)����Ӧ��õ��IJ��������л�������FeO����õ�Fe2O3������?(�ƫ����ƫС������Ӱ�족)��
�ο��𰸣���12��,ÿ��1�֣� (1)�ر�a��������©���ڼ�ˮ����ˮ��©���������������е�ˮ���γ�һ��ˮ����ֹͣ��ˮ������Ƭ�̣���ˮ�����½���֤��������������
(2)�ӿ��������������ʡ���Zn����CuSO4��Ӧ����Cu������Zn���棬Zn(����)��Cu(����)��ϡ����(�������Һ)��ɺܶ�Сԭ��أ�����ԭ��ط�Ӧ���ӿ��˷�Ӧ����
(3)���������Ĵ���
(4)��ȥH2�л��е�HCl���塡Ũ���ᡡ��������
(5)Fe2O3��3H2 2Fe��3H2O��FeO��H2
2Fe��3H2O��FeO��H2 Fe��H2O
Fe��H2O
(6)16��(7)��ֹ�����е�ˮ�������������E�С�ƫ��(8)ƫС
�����������1��Aװ�������շ����������Լ��������Եķ����ǹر�a��������©���ڼ�ˮ��
��ˮ��©���������������е�ˮ���γ�һ��ˮ����ֹͣ��ˮ������Ƭ�̣���ˮ�����½���֤
�������������á�
��2������Zn����CuSO4��Ӧ����Cu������Zn���棬Zn(����)��Cu(����)��ϡ����(�������Һ)��ɺܶ�Сԭ��أ�����ԭ��ط�Ӧ���Ӷ��ӿ��˷�Ӧ���ʡ�
��3�������ǿ�ȼ�����壬��ȼ֮ǰ������������Ĵ��ȡ�
��4���������ɵ������к����Ȼ����ˮ�����������������ʶ��ܸ���ʵ��ģ�ʵ��B��ʢ�б���ʳ��ˮ��������ȥH2�л��е�HCl���壻��C��ʢ��Ũ���ᣬ��������������
��5���ڼ��ȵ�����С�������ܻ�ԭ�����������Ӧ�ķ���ʽ��Fe2O3��3H2 2Fe��3H2O��FeO��H2
2Fe��3H2O��FeO��H2 Fe��H2O��
Fe��H2O��
��6����FeO��Fe2O3��������ʵ����ֱ���x��y����72x��160y��23.2g��U�ι����ӵ��������Ƿ�Ӧ�����ɵ�ˮ�������������x��3y��7.2g��18g//mol�����x��y��0.1mol��ʵ����������������16g��
��7�����ڿ�����Ҳ����ˮ����������Fװ�õ������Ƿ�ֹ�����е�ˮ�������������E�С����û��Fװ�ã���U�ι����ӵ�������ƫ�����Բⶨ���ƫ�ߡ�
��8������Ӧ��õ��IJ��������л�������FeO����U�ι����ӵ�������ƫС�����Բⶨ���ƫС��
�����Ѷȣ�һ��
4��ѡ���� FeCl3��CuCl2����Һ�м������ۣ���ַ�Ӧ�����й�����ڣ������жϲ���ȷ���ǣ�?��
A������KSCN����Һһ�������ɫ
B����Һ��һ����Cu2+
C����Һ��һ������Fe2+
D��ʣ�������һ����ͭ
�ο��𰸣�B
���������
�𰸣�B
B������ȷ�������ԣ�Fe3��>Cu2�� �ȷ��� Fe��2Fe3��=3Fe2�� �ٷ���? Fe��Cu2��=Fe2����Cu����Һ�п��ܺ���Cu2�� ��A��Һ�п϶���Fe3�� ������Ҫ��Cu2�� ������Ӧ��C��ȷ����Һ��һ������Fe2+��D.��ȷ��ʣ�������һ����ͭ��
�����Ѷȣ�һ��
5������� ��ȸʯ��Ҫ��Cu2��OH��2CO3����������Fe��Si�Ļ����ʵ�����Կ�ȸʯΪԭ���Ʊ� CuSO4��5H2O�����ײ���G���������£�

��ش��������⣺
��1����ҺA�Ľ���������Cu2+��Fe2+��Fe3+�������������Լ���ѡ��ʵ�鲽�����Լ������Ϊ_____������ţ���
a��KMnO4? b����NH4��2S? c��H2O2? d��KSCN
����ҺB�м���CuO��������?��
��2������ҺC���CuSO4��5H2O����Ҫ����?����?�����˵Ȳ��������ձ���©���⣬���˲������õ���һ�����������������ڴ˲����е���Ҫ������ ��������
��3��д���Ʊ�G�Ļ�ѧ��Ӧ����ʽ����ʵ��������а����ݳ���Ӧѡ����������������װ�û��գ�����ţ���

��4�����ⶨ��ҺA��Fe2+����Һ������KMnO4����Һ�ζ���ȡ��KMnO4����ҺӦʹ��?��ȡA��Һϡ��һ����������KMnO4����Һ�ζ����յ�����Ϊ?��
�ο��𰸣���1��cd?��2�� �� ������Һ��pHֵ���ٽ�Fe3+ˮ��?��2�֣�
��2��������������ȴ�ᾧ��2�� ��?����?��2�֣�
��3��2NH3+CO2+CaCl2+H2O=CaCO3��+2NH4Cl?��2�� ��? b?��2�֣�
��4����ʽ�ζ���?��2�� �� ��Һ����Ϻ�ɫ�����ְ���Ӳ���ɫ?��2�֣�
�����������1����ʵ��Ҫ��ȥFe2+��Fe3+�����ӣ��ȼ�����ʵ�������ʱ���������µ����ʣ��ɼ���H2O2�������ķ�ӦΪ��2H2O2+2Fe2++2H+�T2Fe3++4H2O����Fe3+��KSCN��Һ��ΪѪ��ɫ�������KSCN����Fe3+���ʴ�Ϊ��c��d������ҺB�м���CuO�������ǵ�����Һ��pHֵ���ٽ�Fe3+ˮ�⡣��2������Һ��Ҫ�������壬������ȴ�ᾧ����Ȼ����й��˵Ȳ����������õ����������ձ�����������©������ֽ�����������в������ڹ���ʱ�����������ã�������ʱ��������ã��ʴ�Ϊ����ȴ�ᾧ�������������衢��������3��CaCl2��Һ������CO2��Ӧ��������ܷ�Ӧ�����ֲ����������ʣ�Ӧͨ��NH3��ʵ�����ռ�����ʱҪע���ֹ��������Ϊ������������ˮ������ʱ���ܲ��ܲ��뵽Һ�����£����õ��õ�©�����ʴ�Ϊ��2NH3+CO2+CaCl2+H2O=CaCO3��+2NH4Cl?��b����4��������ؾ���ǿ�����ԣ���ֻ������ʽ�ζ���ʢװ���������Һ���յ�����Ϊ��Һ����Ϻ�ɫ�����ְ���Ӳ���ɫ ��
�����Ѷȣ�һ��