| �߿�ʡ������ | |
|
|
| �߿�ʡ������ | |
|
|
|
�߿���ѧ֪ʶ���ܽᡶ�����Ļ�ѧ��Դ����Ƶ������ѵ��2017�����°棩(��)
�ο��𰸣�C ���������A���Ҳ�缫����������˵��NԪ�صĻ��ϼ۴�+5�۽��͵�0�ۣ�������ԭ��Ӧ��������ԭ��ص������������Ϊ�������������������ƶ����м���Cl���������ң���ȷ��B�����Ϊ����������������Ӧ�����л���ˮ�е�CԪ�صĻ��ϼ����ߣ�����������������ת��Ϊ������̼���壬��ȷ��C�����������ķ�Ӧ��2NO3-+12H++10e-=N2+6H2O�����Դ�����ķ�ˮ������Ũ�ȼ�С����pH���ߣ�����D��������������ӷ�Ӧ�ĵ缫��Ӧʽ��ÿͨ��1mol���ӣ�������0.1mol��������״���µ������2.24L����ȷ����ѡC�� �����Ѷȣ�һ�� 2��ѡ���� ��֪�����ڷŵ�ʱ��ԭ��ص�����,�ڳ��ʱ����ص����á��������õ�Ǧ��������һ���������״��Ǧ��Ǧ�����һ��ṹ���Ƶij���������Ǧ��Ǧ����ɡ������缫��ϡ�������������Һ���ڷŵ�ʱ,���������ķ�Ӧ�ɷֱ��ʾΪ: |
�ο��𰸣�B
���������Ǧ�Ļ��������ɻ�����Ⱦ,��A����,B��ȷ;�ɵ�ط�Ӧ��֪,1 molǦ��Ӧ����2 mol H2SO4,��C����;�ڵ�ص�ʹ�ù�����,������Һ��Ũ�Ȼ�����,�ܶ���С,��D����
�����Ѷȣ�һ��
3������� (10��)����������ɴ���ʹ�õ�������ȼ�ϵ�أ������ܷ�ӦΪ��2H2��O2===2H2O.�Իش��������⣺
(1)���������ҺΪKOH��Һ������ȼ�ϵ�أ���
�ٸ�����ӦʽΪ________________��
�ڹ���һ��ʱ�����ҺpH________(�����С�����䡱)��
(2)���KOH��ΪϡH2SO4������ʣ���
��������ӦʽΪ________________��
�ڹ���һ��ʱ�����ҺpH________(�����С�����䡱)��
(3)���H2��Ϊ���飬KOH������ʣ���������ӦʽΪ____________________��
�ο��𰸣�(1)��2H2��4OH����4e��===4H2O?�ڼ�С
(2)��?O2��4H����4e��===2H2O�ڡ�������������(3)O2��2H2O��4e��===4OH��
�����������
��1���ٸ÷�Ӧ������ʧ���ӱ�����������ʧ�������������ӣ������Ӻ���Һ�е���������������ˮ�����Ե缫��ӦʽΪ2H2+4OH--4e-=4H2O��
�����ŷ�Ӧ�Ľ��У����ɵ�ˮԽ��Խ�࣬�����������ص������䣬���Ե�����Һ��Ũ�Ƚ��ͣ�������Һ��pHֵ��С��
��2���÷�Ӧ������ʧ���ӱ�����������ʧ�������������ӣ����Ե缫��ӦʽΪ2H2-4e-�T4H+��
�������õ��ӱ���ԭ�������õ��Ӻ���Һ�е�����������ˮ�����Ե缫��ӦʽΪO2+4H++4e-�T2H2O�����ŷ�Ӧ�Ľ��У����ɵ�ˮԽ��Խ�࣬��������������䣬���Ե�����Һ��Ũ�Ƚ��ͣ�������Һ��pHֵ����
��3�������ϼ���ȼ�����ɶ�����̼��ˮ������ʧ���ӷ���������Ӧ���ɶ�����̼��������̼����Һ�е��������ط�Ӧ����̼��غ�ˮ�������������õ��Ӻ�ˮ��Ӧ�������������ӣ����Ե缫��ӦʽΪ��O2+2H2O+4e-�T4OH-��
�����Ѷȣ�һ��
4��ѡ���� ��4��ȼ�ϵ�أ�
A������������ȼ�ϵ�أ�
B����������ȼ�ϵ�أ�
C�����ӽ���Ĥȼ�ϵ�أ�
D��������ȼ�ϵ�ء������ǹ���ԭ��ʾ��ͼ������������Ӧ�IJ���Ϊˮ����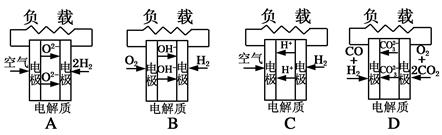
�ο��𰸣�C
���������A���ڸù���������ȼ�ϵ���У����������������ʣ�������O2+4e-=2O2-����A����B������ȼ�ϵ���У������Ϸ���O2+2H2O+4e-=4OH-����B����C�����ӽ���Ĥȼ�ϵ�أ������Ϸ���4H++O2+4e-=2H2O����C��ȷ��D��������ȼ�ϵ���У�������Ӧ��2CO2+O2+4e-=2CO32-����D����ѡ��C��
���㣺����ȼ�ϵ�ص�Ӧ��
�����Ѷȣ�һ��
5��ѡ���� ����ȼ�ϵ�������ں���ɻ��������Բ����缫��KOH��Һ������ʣ�������������ȷ���ǣ�?��
A��H2�ڸ�������������Ӧ
B��ȼ�ϵ�ص�����ת���ʿɴ�100%
C������Ϊ����Ⱦ��ˮ�����ڻ����Ѻõ��
D������ʱ���ܷ�ӦΪ��2H2 + O2 = 2H2O
�ο��𰸣�B
�����������������ȼ�ϵ�ص��ܷ�ӦΪ��2H2 + O2 = 2H2O����������Ⱦ������Ѻõ��
������O2��2H2O��4e��=4OH������ԭ��Ӧ��?������H2��2e����2OH��=2OH����������Ӧ��
���κ�����ת��������ģ�ת���ʲ����ܴ�100%���ʴ�ΪB
�����Ѷȣ���
| ���� �� С������ӡ�� �������� ���ر��� �����ض����� | |
| ��һƪ�����л�ѧ֪ʶ����ɡ����塷��Ƶ.. | |
| �����Ŀ |