微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 几种短周期元素的原子半径和主要化合价见下表,下列有关说法中,正确的是(?)
元素符号
| X
| Y
| Z
| L
| M
| Q
|
原子半径/nm
| 0.160
| 0.143
| 0.102
| 0.099
| 0.077
| 0.066
|
主要化合价
| +2
| +3
| +6、-2
| +7、﹣1
| +4、﹣4
| -2
|
A.离子半径大小:r(X2+)>r(Q2—)
? B.Y与Q形成的化合物不能跟氢氧化钠溶液反应
? C.Z的单质可在氧气中燃烧生成ZO3
? D.M元素与L元素形成的一种化合物是常见的有机溶剂
参考答案:D
本题解析:考查元素周期律的应用。根据元素原子的半径和主要化合价可判断,X是Mg,Y是Al,Z是S,L是Cl,M是C,Q是O。核外电子排布相同的微粒,其微粒半径随原子序数的增大而减小,A不正确。氧化物是两性氧化物,能溶于氢氧化钠溶液中,B不正确。硫燃烧的生成物只能是SO2,而不是三氧化硫,C不正确。四氯化碳是常用的一种有机溶剂,D正确。答案选D。
本题难度:一般
2、填空题 (12分)短周期元素的单质X、Y、Z在通常状况下均为气态,并有下列转化关系(反应条件略去):
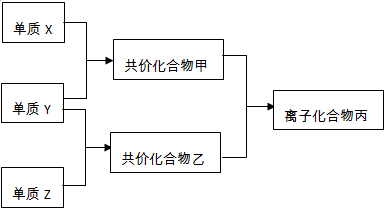
已知: a.常见双原子单质分子中,X分子含共价键最多。
b.甲分子中含10个电子,乙分子含有18个电子。
(1)X的电子式是?。
(2)实验室可用下图所示装置(缺少收集装置,夹持固定装置略去)制备并收集甲

①在图中方框内绘出用烧瓶收集甲的仪器装置简图。
②试管中的试剂是(填写化学式)?。
③烧杯中溶液由无色变为红色,其原因是(用电离方程式表示)?
(3)磷在Z中燃烧可生成两种产物,其中一种产物丁分子中各原子最外层不全是8电子结构,丁的化学式是?。
(4)nmol丁与nmol丙在一定条件下反应,生成4nmol乙和另一化合物,该化合物蒸气的密度是相同状况下氢气的174倍,其化学式是_? ___。
参考答案:(1)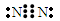 (2)
(2)
①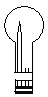
②NH4Cl与Ca(OH)2?③NH3·H2O≒NH4+ +OH-
(3) PCl5?(4)P3N3Cl6
本题解析:(1)短周期中气体单质只有五种:氢气、氮气、氧气、氟气、氯气;常见双原子单质分子中,X分子含共价键最多,可知X为N2;甲分子中含10个电子,可知甲为含有N原子的NH3,那么单质Y为氢气;乙分子含有18个电子,可知为含有H元素的HCl,即Z为氯气。
(2)考查了氨气的制取和收集及碱性
(3)P在氯气中燃烧产物有两种:PCl3和PCl5。
(4)由原子守恒知:nPCl5+nNH4Cl===(PNCl2)n +4nHCl,再由分子量为348知n=3
本题难度:一般
3、选择题 下列各微粒,具有相同的质子数和电子数的是(?)
A.CH4 NH3 H2O Ar
B.OH- F- O2- Ne
C.H3O+ NH4+ Na+ H2F+
D.O2- F- Mg2+ Al3+
参考答案:C
本题解析:根据微粒的化学式可知,A中质子数和核外电子数分别是10和10、10和10、10和10、18和18;B中质子数和核外电子数分别是9和10、9和10、8和10、10和10;C中质子数和核外电子数分别是11和10、11和10、11和10、11和10;D中质子数和核外电子数分别是8和10、9和10、12和10、13和10,答案选C。
点评:该题是高考中的常见题型,属于中等难度的试题。该题的关键是明确质子数和核外电子数的计算依据,有利于培养学生的逻辑思维能力和灵活应变能力。
本题难度:一般
4、选择题 A元素的阳离子与B元素的阴离子具有相同的电子层结构,有关两元素有以下叙述:①原子半径A<B;②离子半径A>B;③原子序数A>B;④原子最外层电子数A≤B;⑤A的正价与B的负价绝对值一定相等。其中正确的是
A.①②
B.③④
C.③⑤
D.③④⑤
参考答案:B
本题解析:A元素的阳离子与B元素的阴离子具有相同的电子层结构,所以A的原子序数大于B的,原子半径A大于B,但离子半径是B的大于A的。其中A是金属,B是非金属位于A的上一周期的右侧。所以答案选B。
本题难度:一般
5、选择题 应用元素周期律和元素周期表,判断下列说法正确的是(?)
A.碱金属单质的熔点随原子序数的增大而降低
B.砹(At)是VIIA族元素,HAt的稳定性大于HCl
C.第2周期非金属的气态氢化物溶于水后所得溶液均为酸性
D.铊(TI)与铝同主族,其单质既能与盐酸反应又能与NaOH溶液反应
参考答案:A
本题解析:A.碱金属单质的熔点随原子序数的增大而降低,正确;B.砹(At)是VIIA族元素,HAt的稳定性小于HCl,错误;C.第2周期非金属的气态氢化物溶于水后所得溶液除氨水显碱性外其余的均为酸性,错误;D.铊(TI)与铝同主族,由于去金属性比Al强,所以其单质只能与盐酸反应而不能能与NaOH溶液反应,错误。
本题难度:一般