微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 X、Y、Z三种短周期元素,原子半径的大小关系为r(Y)>r(X)>r(Z),原子序数之和为16。X、Y、Z三种元素的常见单质在在适当条件下可发生如下变化,其中B和C均为10电子分子。下列说法中不正确的是?
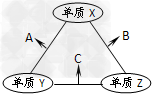
[? ]
A.X元素位于ⅥA?
B.B的沸点大于C的沸点
C.A能溶解于B中?
D.A和C不可能发生氧化还原反应
参考答案:CD
本题解析:
本题难度:一般
2、选择题 硒是人体必需的重要微量元素之一,同样也是其他动植物新陈代谢必不可少的生命元素.某同学查看元素周期表得知硒(Se)第34号元素,位于周期表的第四周期VIA族,以下关于硒的说法错误的是( )
A.Se原子最外层有6个电子
B.Se元素最高价氧化物的水化物呈强碱性
C.Se的原子半径比S的原子半径小
D.Se常温下为固体
参考答案:A、Se在第VIA族,则Se原子最外层有6个电子,故A正确;
B、Se为非金属元素,非金属性S>Se,则Se元素最高价氧化物的水化物呈酸性,且酸性小于硫酸,故B错误;
C、同主族元素,从上到下原子半径在增大,则Se的原子半径比S的原子半径大,故C错误;
D、常温下S为固体,则Se常温下为固体,故D正确;
故选BC.
本题解析:
本题难度:简单
3、填空题 表是周期表中的一部分,根据A-I在周期表中的位置,用元素符号或化学式回答下列问题:
| 族周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0
1
A
2
D
E
G
I
3
B
C
F
H
|
(1)表中元素,化学性质最不活泼的是______,只有负价而无正价的是______,氧化性最强的单质是______,还原性最强的单质是______;
(2)最高价氧化物的水化物碱性最强的是______,酸性最强的是______,呈两性的是______;
(3)A分别与D、E、F、G、H形成的化合物中,最稳定的______;
(4)在B、C、D、E、F、G、H中,原子半径最大的是______;
(5)A和E形成化合物的化学式______.
参考答案:根据元素周期表的结构,表中A、B、C、D、E、F、G、H、I元素分别是H、Na、Al、C、N、P、F、Cl、Ne.
(1)根据同周期元素金属性递变规律可知,金属性最强的应该是Na,即还原性最强的单质是Na;其中H、C、N、P、F、Cl是非金属元素,根据同周期、同主族元素非金属性递变规律可知,非金属性最强的应该是F,即氧化性最强的单质是F2,F元素只有负价没有正价,化学性质最不活泼的应是惰性气体,即Ne,故答案为:Ne;F;F2;Na;
(2)由(1)分析,金属性最强的是Na,最高价氧化物的水化物碱性最强的是NaOH;非金属性最强的是F,但是F无最高正价,则酸性最强的是应是HClO4,氢氧化铝是两性氢氧化物,
故答案为:NaOH;HClO4;Al(OH)3;
(3)元素周期表中同周期元素从左到右氢化物的稳定性逐渐增强,同主族从上到下氢化物的稳定性逐渐减弱,所以CH4、NH3、H2O、HF中最稳定的是HF,故答案为:HF;
(4)第三周期元素原子半径大于第二周期元素的原子半径,同周期原子半径从左到右逐渐减小,所以半径最大的是Na,故答案为:Na;
(5)氮元素和氢元素形成的化合物是氨气,故答案为:NH3.
本题解析:
本题难度:一般
4、简答题 某同学为了验证碳和硅两种元素非金属性的相对强弱,用下图所示装置进行实验(夹持仪器已略去,气密性已检验).
实验操作步骤:
Ⅰ.打开弹簧夹1,关闭弹簧夹2,并打开活塞a,滴加盐酸.
Ⅱ.A中看到白色沉淀时,…,关闭活塞a.
请回答:
(1)B中反应的离子方程式是______.
(2)通过步骤Ⅰ得知盐酸具有的性质是______(填字母).
A.挥发性?B.还原性?C.氧化性?D.酸性
(3)C装置的作用是______,X是______(写化学式).
(4)为了验证碳的非金属性强于硅,步骤Ⅱ中未写的操作和现象是______,D中反应的化学方程式是______.
(5)碳、硅的非金属性逐渐减弱的原因是______(从原子结构角度加以解释).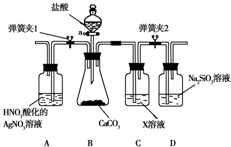
参考答案:(1)B中发生盐酸与碳酸钙的反应,生成氯化钙、水、二氧化碳,该离子反应为CaCO3+2H+=Ca2++CO2↑+H2O,
故答案为:CaCO3+2H+=Ca2++CO2↑+H2O;
(2)A中看到白色沉淀,盐酸能与盐反应,可知盐酸具有的酸性、挥发性,故答案为:AD;
(3)X为碳酸氢钠溶液,与挥发的盐酸反应,可除去二氧化碳中混有的HCl,C装置的作用是除HCl气体,
故答案为:除HCl气体;NaHCO3;
(4)D中发生二氧化碳与硅酸钠溶液的反应,该反应为Na2SiO3+CO2+H2O=H2SiO3(胶体)+Na2CO3,步骤Ⅱ中未写的操作和现象是关闭弹簧夹1,打开弹簧夹2,当D中出现白色胶状沉淀后,
故答案为:关闭弹簧夹1,打开弹簧夹2,当D中出现白色胶状沉淀后;Na2SiO3+CO2+H2O=H2SiO3(胶体)+Na2CO3;
(5)碳、硅的非金属性逐渐减弱的原因是碳和硅位于同一主族,从上到下,原子半径逐渐增大,得电子的能力减弱,非金属性减弱,故答案为:碳和硅位于同一主族,从上到下,原子半径逐渐增大,得电子的能力减弱,非金属性减弱.
本题解析:
本题难度:一般
5、选择题 已知元素周期表前三周期元素的离子aW3+、bX+、cY2-、dZ-都具有相同的电子层结构,下列关系正确的是
A.离子还原性Y2->Z-
B.质子数c>b
C.氢化物稳定性H2Y>HZ
D.原子半径X<W
参考答案:A
本题解析:试题分析:元素周期表前三周期元素的离子aW3+、bX+、cY2-、dZ-具有相同电子层结构,则核外电子数相等, Y、Z为非金属,应处于第二周期,故Y为O元素,Z为F元素,W、X为金属元素,应处于第三周期,W为Al元素,X为Na元素。
A、非金属性F>O,非金属性越强,对应的单质的氧化性越强,则阴离子的还原性越弱,故还原性Y2->Z-,正确;B、由以上分析可知c=8,b=11,则质子数c<b,错误;C、非金属性F>O,非金属性越强其氢化物越稳定性,氢化物稳定性为HZ>H2Y,错误;D、W为Al元素,X为Na元素,原子半径Na>Al,错误。
考点:考查结构与位置关系、元素周期律等知识。
本题难度:一般