微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 第七周期为不完全周期,若将来的发现可把这一周期元素排满,则下列有关第七周期元素的推论正确的是
[? ]
A.第七周期排满时,最后一种元素的单质将很稳定
B.第七周期排满时,应该有32种元素
C.第七周期ⅡA族元素的氢氧化物性质与Al(OH)3相似
D.第七周期最后一种元素的原子序数为118
参考答案:BD
本题解析:
本题难度:简单
2、简答题 现有A、B、C、D、F六种短周期元素,在化学反应中均能形成简单的阴离子或阳离子,且A、B、C、D离子具有相同的电子层结构.
已知:①常温下,F的单质是一种有色气体,常用于杀菌、消毒;
②A的单质以溶于NaOH溶液,向生成的溶液中通入CO2气体有白色沉淀生成;
③C的氢化物分子G是具有10电子微粒,且以发生下列转化:G
?P ?Q ?M+P;
④E和D是同一主族的元素,二者能形成微粒的个数比为1:2和1:3的化合物T和K;
⑤B和D可形成微粒个数比为1:1和2:1的离子化合物X和Y.
请回答下列问题:
(1)B元素的名称是______;
(2)E元素的原子结构示意图是______.
(3)请将A、C的元素符号填在如图所示部分元素周期表的适当位置上.
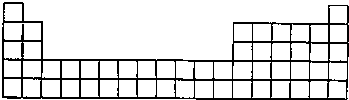
(4)G的电子式为______.化合物X所含化学键类型有______.
(5)T与F单质的水溶液反应的离子方程式为______;G与D的单质反应的化学方程式为______;M与铜反应的化学方程式为______.
参考答案:现有A、B、C、D、F六种短周期元素,在化学反应中均能形成简单的阴离子或阳离子,且A、B、C、D离子具有相同的电子层结构.
①常温下,F的单质是一种有色气体,常用于杀菌、消毒,推断为Cl2;
②A的单质溶于NaOH溶液,向生成的溶液中通入CO2气体有白色沉淀生成,Si不能形成简单离子,则A为Al;
③C的氢化物分子G是具有10电子的微粒,在化学反应中均能形成简单的阴离子或阳离子,且A、B、C、D离子具有相同的电子层结构,可以发生下列转化:G D的单质
本题解析:
本题难度:一般
3、选择题 在元素周期表中金属元素和非金属元素的分界线附近的一些元素能用于制
[? ]
A.合金
B.半导体
C.催化剂
D.农药
参考答案:B
本题解析:
本题难度:简单
4、选择题 下列对一些实验事实的理论解释不正确的是( )
| 选项 | 客观事实 | 理?论?解?释
A
在水中,NaCl的溶解度比I2的溶解度大
NaCl晶体中C1-与Na+间的作用力大于碘晶体中分子间的作用力
B
酸性:HClO<H2CO3
非金属:C>Cl
C
原子半径:Cl<S
Cl、S原子电子层数相同,但氯原子核电荷数较硫多,对核外电子吸引能力比硫强
D
水分子比H2S分子稳定
H-O键比H-S键稳定
|
A.A
B.B
C.C
D.D
参考答案:A.氯化钠为离子晶体,易溶于极性分子水,而碘为非极性分子,不易溶于水,故A正确;
B.非金属性越大,最高价氧化物的水化物的酸性越强,非金属性Cl>C,故B错误;
C.电子层相同时,核电荷数越大,半径越小,则原子半径Cl<S,故C正确;
D.稳定性与化学键有关,O-H键能大,则水比硫化氢温度,故D正确;
故选B.
本题解析:
本题难度:一般
5、选择题 下表是元素周期表的一部分,有关说法正确的是( )
? 族
周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅤⅡA
2
c
d
3
a
b
e
f
|
A.e的氢化物比d的氢化物稳定
B.a、b、e三种元素的原子半径e>b>a
C.六种元素中,e元素单质的化学性质最活泼
D.c、e、f的最高价氧化物对应的水化物的酸性依次增强
参考答案:A、d和e属于同一主族,由上到下,元素非金属性逐渐减弱,对应氢化物的稳定性逐渐减弱,即H2O>H2S,故A错;
B、a、b、e属于同一周期,从左到右核电荷数依次增多,原子半径逐渐减小,因此a、b、e三种元素的原子半径大小为a>b>e,故B错;
C、此题表达不明确,是金属性最强,还是非金属性最强,故C错;
D、同一周期中,从左到右核电荷数依次增多,原子得电子能力逐渐增强,同一主族,由上到下,原子得电子能力逐渐减弱,因此c、e、f的最高价氧化物对应的水化物酸性增强,故D对;故选:D.
本题解析:
本题难度:简单